Clear Sky Science · fr
Irisine régule le métabolisme lipidique et la ferroptose dans les cellules du cancer de l’ovaire en modulant l’axe ALOX5–5‑HETE–PD‑L1
Pourquoi cette molécule végétale compte pour le cancer de l’ovaire
Le cancer de l’ovaire est l’un des cancers les plus meurtriers chez les femmes, car il est généralement détecté tard et récidive fréquemment après le traitement. Cette étude examine si un composé naturel nommé tectorigénine, présent dans la plante Belamcanda chinensis, peut ralentir le cancer de l’ovaire en privant les cellules tumorales de certaines graisses et en les poussant vers un type particulier de mort cellulaire dépendante du fer. Elle analyse aussi comment ce composé pourrait affaiblir la « cape d’invisibilité » que les tumeurs utilisent pour se cacher du système immunitaire.
Une source d’énergie cachée à l’intérieur des cellules tumorales
Comme beaucoup de cancers, les tumeurs ovariennes reconfigurent leur gestion des lipides. Plutôt que de se contenter d’utiliser les graisses comme carburant, les cellules cancéreuses les accumulent comme éléments de construction pour de nouvelles membranes et comme tampons contre les dommages. Dans des cellules de cancer de l’ovaire cultivées en laboratoire, l’ajout d’acides gras monoinsaturés a entraîné une accumulation d’acides gras libres, de triglycérides et de cholestérol — formes clés de graisses stockées. Cet excès lipidique a favorisé la croissance et l’invasion des cellules et les a aidées à résister à un processus destructeur appelé ferroptose, où le fer et les lipides oxydés s’associent pour rompre les membranes cellulaires. Autrement dit, un métabolisme lipidique anormal a conféré à la tumeur un avantage de croissance et un bouclier de survie.
Forcer les cellules cancéreuses vers l’autodestruction
Les chercheurs ont ensuite testé la tectorigénine sur des cellules ovariennes normales et plusieurs lignées de cellules de cancer de l’ovaire. À des doses allant jusqu’à 200 microgrammes par litre, le composé n’a pas endommagé les cellules normales mais a nettement ralenti la croissance des cellules cancéreuses, réduit leur capacité d’invasion à travers une membrane et augmenté leur taux de mort cellulaire programmée. Lorsque les cellules cancéreuses étaient prétraitées par un médicament bloquant la ferroptose, elles devenaient plus agressives. L’ajout de tectorigénine a inversé ces effets : les réserves lipidiques ont diminué, les marqueurs liés au fer et à l’oxydation ont augmenté, et davantage de cellules sont mortes. Chez des souris porteuses de tumeurs ovariennes humaines, des injections de tectorigénine ont réduit la taille des tumeurs, diminué la teneur en lipides des tissus tumoraux et augmenté les signes chimiques de ferroptose, suggérant encore que le composé oriente les cellules cancéreuses vers cette voie de mort dépendante du fer.
Un interrupteur moléculaire clé reliant lipides et fuite immunitaire
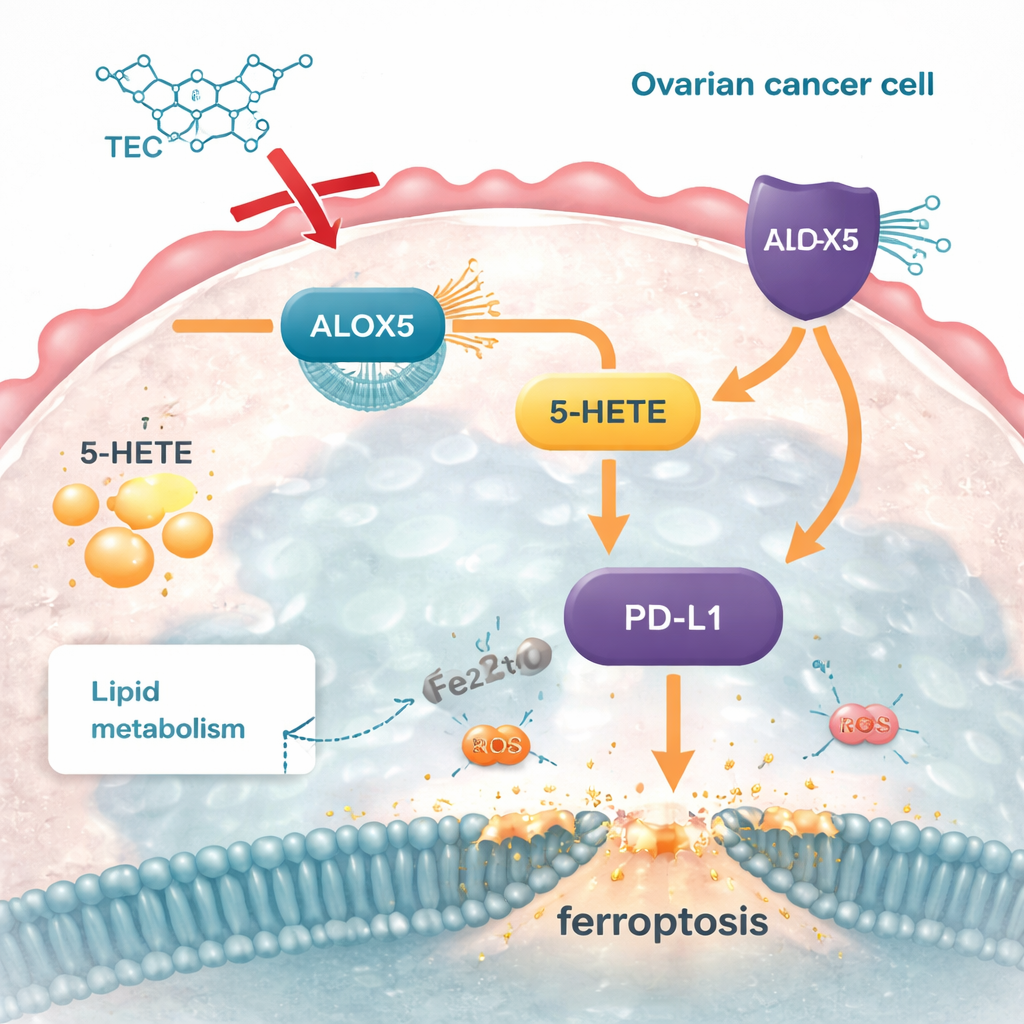
Pour comprendre le mécanisme moléculaire de la tectorigénine, l’équipe a combiné l’exploitation de grandes bases de données et la modélisation informatique des interactions médicament‑protéine. Ils ont focalisé leur attention sur une enzyme appelée ALOX5, qui convertit un acide gras courant en une molécule de signalisation nommée 5‑HETE. Dans les cellules de cancer de l’ovaire et les échantillons tumoraux, les niveaux d’ALOX5 étaient bien supérieurs à ceux des tissus normaux. Le docking informatique et les simulations de dynamique moléculaire ont montré que la tectorigénine peut se lier de manière stable à ALOX5, agissant comme un frein interne. Lorsque les chercheurs ont augmenté artificiellement ALOX5 dans les cellules cancéreuses, les réserves lipidiques ont augmenté, les marqueurs de ferroptose ont diminué et les cellules sont devenues plus invasives. Le traitement par tectorigénine a annulé ces changements. L’inhibition d’ALOX5 a eu l’effet inverse — moins de lipides, plus de ferroptose et une croissance amoindrie — plaçant fermement cette enzyme au centre de l’action du composé.
Comment les tumeurs perdent leur bouclier contre le système immunitaire
L’étude a aussi relié cette voie lipidique à une molécule de point de contrôle immunitaire importante, PD‑L1, que les tumeurs utilisent pour désactiver les cellules immunitaires attaquantes. Le produit d’ALOX5, le 5‑HETE, augmentait les niveaux de PD‑L1, renforçant ce bouclier. Lorsque ALOX5 a été silencée, à la fois 5‑HETE et PD‑L1 ont diminué ; lorsque le 5‑HETE a été réintroduit, PD‑L1 est remonté et les cellules cancéreuses ont retrouvé une partie de leur protection contre la ferroptose. La tectorigénine a réduit ALOX5, abaissé le 5‑HETE et, par conséquent, diminué PD‑L1 dans les cultures cellulaires et les tumeurs de souris. Cela suggère qu’en ciblant une seule enzyme métabolique, le composé peut à la fois perturber les défenses lipidiques du cancer et affaiblir sa capacité à se cacher de l’attaque immunitaire.
Ce que cela pourrait signifier pour les traitements futurs
En bref, ce travail montre que la tectorigénine agit comme une clé bien placée dans la machinerie lipidique des cellules cancéreuses. En bloquant ALOX5, elle coupe la production de 5‑HETE, réduit les excès de réserves lipidiques, rend les cellules vulnérables aux dommages induits par le fer et enlève une partie de leur camouflage immunitaire. Bien que ces résultats proviennent d’études sur cellules et sur souris — et que de nombreux tests restent à mener chez l’humain — ils pointent vers une stratégie prometteuse : cibler l’axe ALOX5–5‑HETE–PD‑L1 pour à la fois affamer les tumeurs ovariennes et faciliter leur élimination par les défenses naturelles de l’organisme ou par de futures immunothérapies.
Citation: Cai, H., Huang, C. & Zhang, Z. Irisin regulates lipid metabolism and ferroptosis in ovarian cancer cells by modulating the ALOX5-5-HETE-PD-L1 axis. Sci Rep 16, 7223 (2026). https://doi.org/10.1038/s41598-026-36816-4
Mots-clés: cancer de l’ovaire, métabolisme lipidique, ferroptose, ALOX5, thérapie par composé naturel