Clear Sky Science · fr
Système de défense de type RexAB encodé par un prophage chez Pseudomonas putida
Garde du corps cachés vivant à l’intérieur des bactéries
Les bactéries sont constamment chassées par des virus appelés phages, capables d’anéantir des populations microbiennes entières. Cette étude examine comment des virus « endormis » déjà dissimulés dans l’ADN d’une bactérie peuvent agir en secret comme des gardes du corps, sacrifiant les cellules infectées pour sauver le reste. Comprendre ces mécanismes de défense naturels est important pour les thérapies à base de phages, la biotechnologie, et pour garantir la fiabilité des microbes industriels.
Des virus qui deviennent des alliés
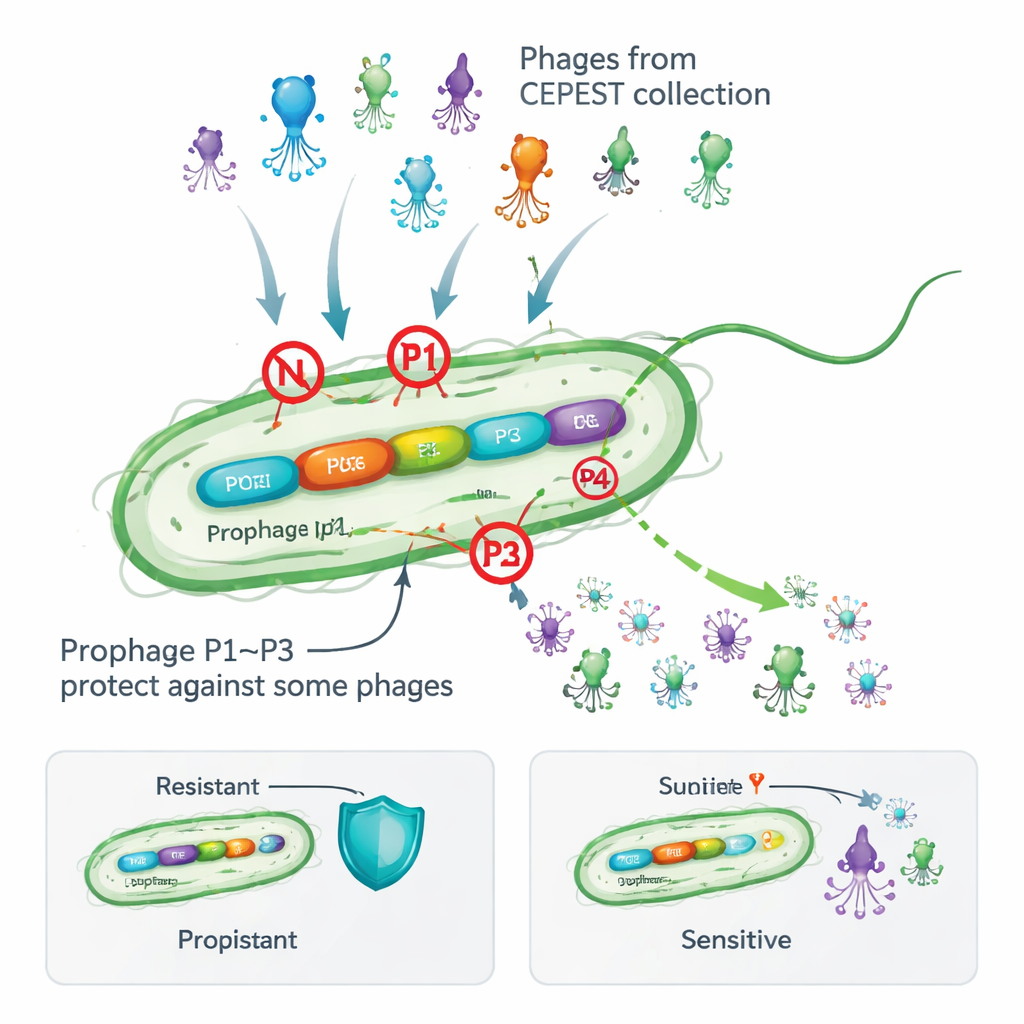
Beaucoup de bactéries portent des phages tempérés sous une forme dormante appelée prophage, intégrée dans leur chromosome. À première vue, cela semble risqué : ces passagers viraux peuvent se réveiller et endommager la cellule hôte, et ils alourdissent le génome. Pourtant, des relevés de milliers de génomes bactériens montrent que la plupart des espèces conservent de tels prophages, ce qui suggère qu’ils apportent des avantages. Des travaux antérieurs sur la bactérie du sol Pseudomonas putida ont montré que la suppression de ses quatre prophages cryptiques (non productifs) rendait les cellules plus vulnérables à une collection expérimentale de phages appelée CEPEST. Cela suggérait que les prophages portent des armes anti‑phages, mais les gènes et mécanismes exacts restaient inconnus.
Trois virus résidents offrent une protection ciblée
Les auteurs ont disséqué la contribution de chaque prophage en les supprimant un par un et en testant la capacité de 26 phages différents de CEPEST à former des plages de lyse sur des nappes bactériennes. Ils ont découvert que les prophages nommés P1, P2 et P3 fournissent chacun une protection, mais seulement contre des groupes particuliers de phages, tandis que P4 semble neutre. P1 seul peut réduire l’infection par certains phages d’environ mille fois, P2 offre une protection plus modeste, et P3 est spectaculairement efficace — mais uniquement contre certains phages géants « jumbo ». Dans la plupart des cas, un seul prophage explique le profil de résistance observé, bien que pour quelques phages plusieurs prophages semblent coopérer. Ces résultats montrent que même des prophages « silencieux » peuvent agir comme un bouclier personnalisé adapté à des menaces virales spécifiques.
À la recherche d’une alarme moléculaire en deux parties
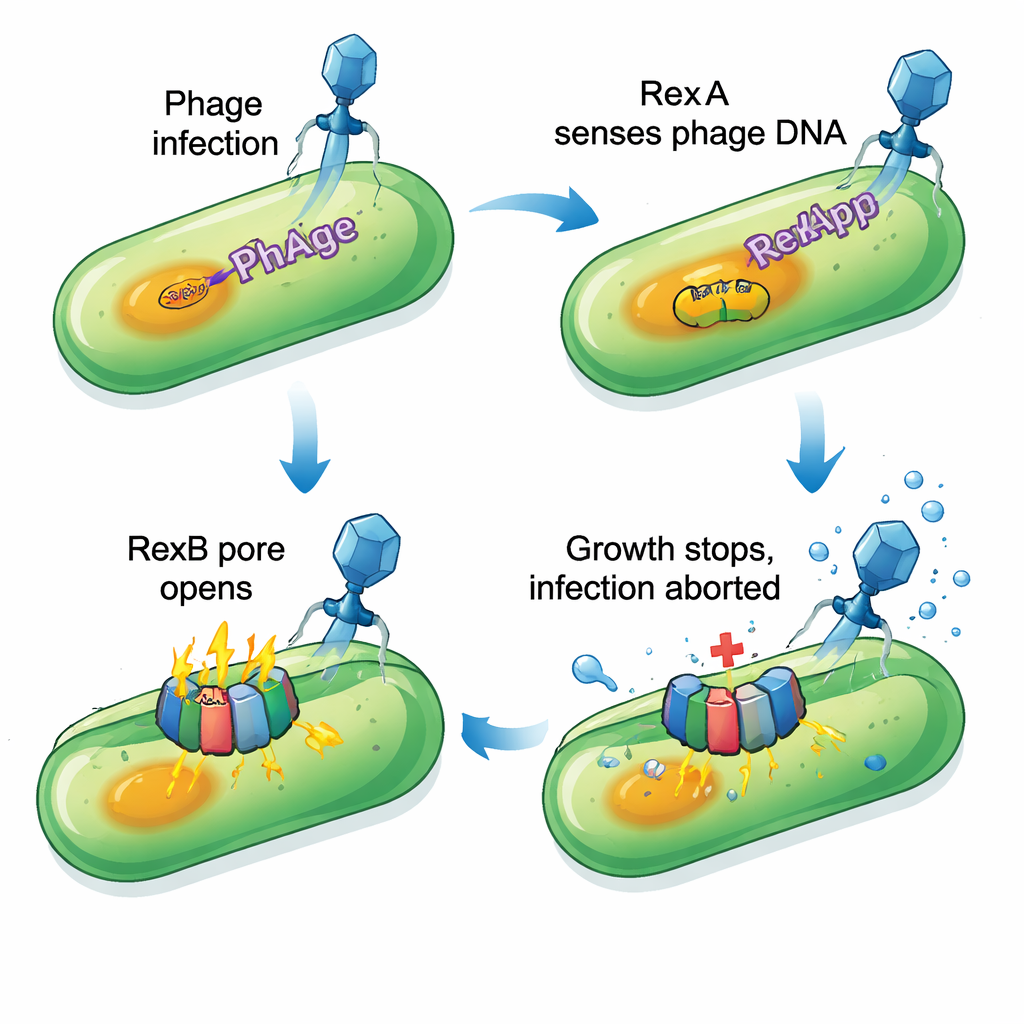
En se concentrant sur la protection forte et relativement large fournie par P1, l’équipe a supprimé systématiquement des blocs de gènes de P1 jusqu’à la disparition de la défense. En affinant la recherche, ils ont découvert que la perte de seulement deux gènes voisins, PP_5643 et PP_5644, rendait les cellules aussi sensibles que si le prophage P1 entier avait été supprimé. Des outils bioinformatiques ont révélé que PP_5643 ressemble à RexA, une protéine liée à l’ADN issue des études classiques sur le phage lambda, tandis que PP_5644 ressemble à une protéine membranaire avec plusieurs hélices pouvant former un pore, similaire à RexB. Ensemble, cette paire correspond à un type bien connu de système d’« infection abortive » : une fois qu’un phage spécifique est détecté, la cellule infectée arrête délibérément sa croissance pour empêcher le virus de se multiplier et de se propager aux voisins.
Comment la défense sabote les cellules infectées
Les expériences ont confirmé que la version P1 de RexA (appelée RexApp) se lie à l’ADN sans grande préférence pour une séquence exacte, ce qui la rend bien adaptée à détecter des structures d’ADN inhabituelles créées durant la réplication virale. La protéine partenaire RexBpp s’insère dans la membrane cellulaire. Lorsque RexApp est surexprimée artificiellement, les cellules qui conservent encore le gène rexBpp montrent un arrêt sévère de la croissance et des signes de dommages membranaires : des colorants qui normalement ne traversent pas une membrane intacte pénètrent soudainement, et de faibles quantités d’une enzyme cytoplasmique fuient. Si rexBpp est manquant ou muté, la surexpression de RexApp ne nuit plus aux cellules. Cela indique que RexApp agit comme déclencheur, tandis que RexBpp est l’effecteur qui endommage l’enveloppe cellulaire. Fait intéressant, la plupart des cellules affectées n’éclatent pas complètement ; elles entrent plutôt dans un état profondément ralenti, presque stationnaire, incompatible avec la multiplication du phage.
Pourquoi sacrifier quelques cellules peut sauver la population
Le tableau qui se dégage est celui d’une défense altruiste : lorsqu’un phage sensible infecte P. putida, RexApp détecte probablement des complexes ADN–protéines viraux et active RexBpp, qui compromet la membrane et arrête brusquement la croissance. La cellule infectée paie le prix, mais le cycle de vie du phage est avorté et la communauté bactérienne élargie est protégée. Des systèmes de type RexAB n’ont été trouvés que chez un petit nombre de phages différents, mais ils partagent la même logique de base — un senseur intracellulaire lié à un effecteur membranaire capable de transformer rapidement une cellule productive en impasse pour le virus. Pour les bactéries, conserver des prophages cryptiques portant de tels modules de défense peut compenser les coûts de l’hébergement d’ADN viral, les aidant à survivre dans un monde où les phages sont omniprésents.
Citation: Rosendahl, S., Kängsep, A., Ainelo, A. et al. Prophage-encoded RexAB-type phage defense system in Pseudomonas putida. Sci Rep 16, 5898 (2026). https://doi.org/10.1038/s41598-026-36734-5
Mots-clés: défense contre les bactériophages, prophage, Pseudomonas putida, infection abortive, système RexAB