Clear Sky Science · fr
Réduction de l'isoforme longue de la kinase WNK1 atténue la glomérulonéphrite anti-membrane basale glomérulaire chez la souris
Pourquoi cela compte pour la santé rénale
Les maladies rénales rapidement progressives peuvent détruire les minuscules filtres de l'organe en quelques semaines, conduisant souvent à la dialyse ou à une transplantation. Cette étude examine si la diminution d'une seule protéine, appelée L-WNK1, peut ralentir cette destruction chez la souris. Comme des médicaments ciblant cette protéine sont déjà développés pour des problèmes de tension artérielle, les résultats suggèrent une voie possible pour protéger les reins en détresse.
Un contrôleur de trafic à l'intérieur des filtres rénaux
Chaque rein contient des centaines de milliers de filtres microscopiques, ou glomérules, qui épurent le sang. Dans ces filtres, deux types cellulaires clés collaborent : les podocytes, qui entourent les vaisseaux sanguins comme des doigts imbriqués, et les cellules épithéliales pariétales (PEC), qui tapissent l'enveloppe externe. Dans une affection dangereuse appelée glomérulonéphrite rapidement progressive (RPGN), les podocytes sont lésés et les PEC deviennent hyperactives, s'accumulant en « croissants » qui obstruent la filtration. La protéine L-WNK1, un interrupteur de signalisation surtout connue pour aider à l'équilibre du sel et de la pression artérielle, est en réalité fortement exprimée dans ces cellules glomérulaires. Les auteurs se sont demandé si un excès de L-WNK1 aggrave la RPGN, et si sa réduction peut en atténuer les effets.
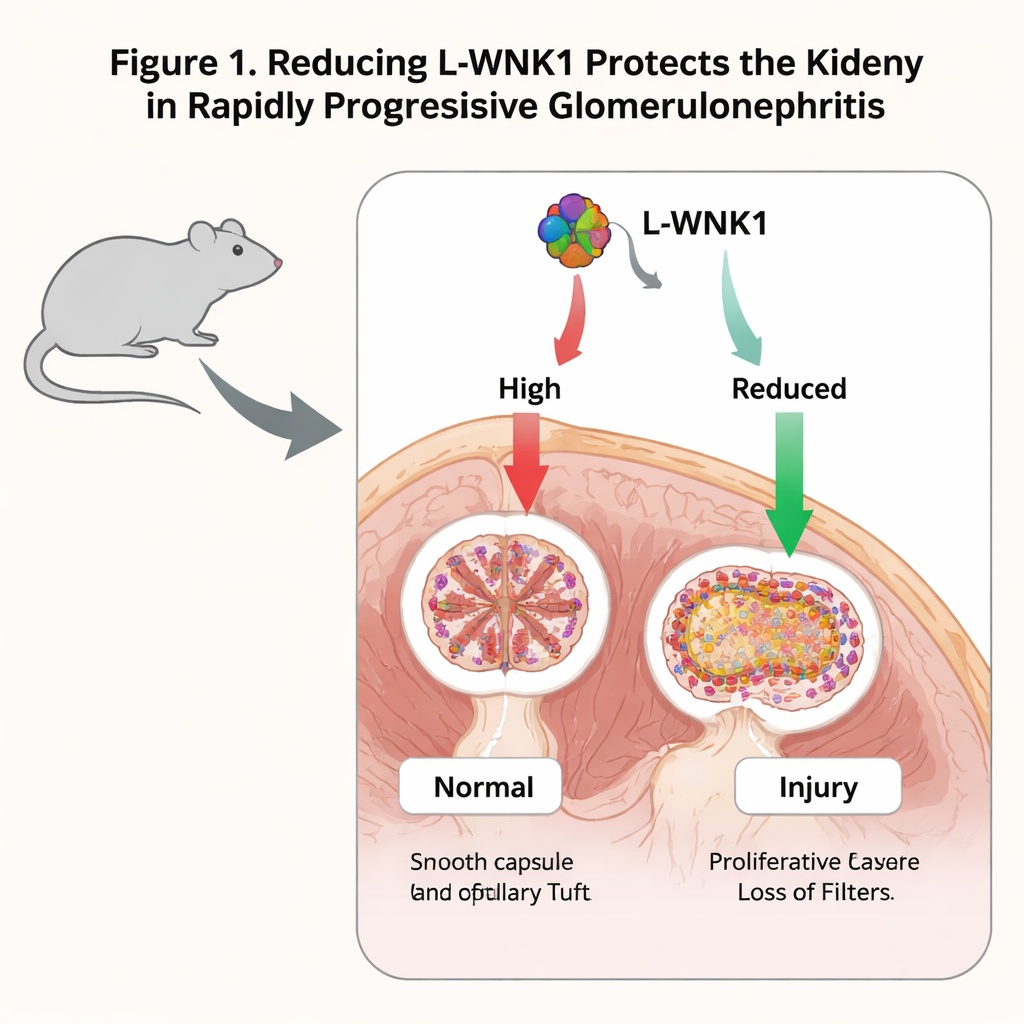
Réduire L-WNK1 atténue les lésions rénales chez la souris
Les chercheurs ont d'abord utilisé un modèle murin classique de RPGN déclenché par des anticorps qui attaquent la membrane basale glomérulaire, un composant clé du filtre. Ils ont constaté que les niveaux de L-WNK1 augmentaient dans les glomérules après la lésion, non seulement chez la souris mais aussi dans des biopsies rénales de patients atteints de maladies apparentées. Pour tester la causalité, ils ont étudié des souris nées avec une seule copie fonctionnelle du gène L-WNK1. Ces animaux ont développé une insuffisance rénale après l'attaque par les anticorps, mais leurs marqueurs sanguins d'atteinte étaient moins élevés et leurs tissus rénaux montraient moins de croissants et moins de cicatrisation que chez les souris normales. Des marqueurs d'inflammation et de fibrose, tels que les molécules de signalisation MCP-1, TGF-β1 et les gènes du collagène, étaient également réduits. Ensemble, ces éléments suggèrent qu'une perte partielle de L-WNK1 rend la maladie moins sévère plutôt que plus grave.
Approfondissement sur les podocytes et leurs voisins
Étant donné que les podocytes sont centraux pour la santé glomérulaire et expriment fortement L-WNK1, l'équipe a ensuite supprimé WNK1 spécifiquement dans ces cellules à l'aide d'un procédé génétique. Dans des conditions normales, ces souris avaient des reins sains, montrant que les podocytes n'ont pas besoin de L-WNK1 pour se développer ou fonctionner au quotidien. Lorsque la RPGN a été induite, les souris avec suppression spécifique aux podocytes s'en sont à nouveau mieux sorties que les témoins : leurs analyses sanguines étaient améliorées et elles avaient tendance à présenter moins de croissants et moins de PEC exprimant CD44, un marqueur d'activation. Cependant, la protection était moins marquée que chez les souris avec une réduction plus large de L-WNK1 dans tout l'organisme, et les niveaux de certains marqueurs inflammatoires n'ont pas diminué. Cela indique un rôle de L-WNK1 non seulement dans les podocytes mais aussi dans d'autres cellules glomérulaires ou immunitaires qui participent à la maladie.
Ralentir les mouvements cellulaires nuisibles
Pour explorer comment L-WNK1 pourrait favoriser la formation de croissants, les investigateurs se sont tournés vers des cultures cellulaires. En utilisant une petite molécule qui bloque les kinases WNK, ils ont traité des podocytes humains cultivés en laboratoire et observé la vitesse à laquelle ils colonisaient un « puit » artificiel créé dans la culture. Le blocage de l'activité de L-WNK1 a nettement ralenti leur déplacement. Ils ont observé un effet similaire dans des PEC en culture : lorsqu'un facteur de croissance était ajouté, les PEC se déployaient normalement pour remplir l'écart, mais cette réponse était atténuée en présence de l'inhibiteur de WNK. Fait intéressant, le médicament n'a pas perturbé de façon notable l'ossature interne des podocytes dans leur système, malgré des travaux antérieurs sur des cellules murines suggérant des problèmes structurels majeurs. Cela étaye l'idée que, au moins chez l'animal vivant, le rôle principal de L-WNK1 ici pourrait être de contrôler la mobilité et la réponse des cellules glomérulaires et immunitaires lors de la lésion plutôt que de maintenir l'architecture de base du filtre.
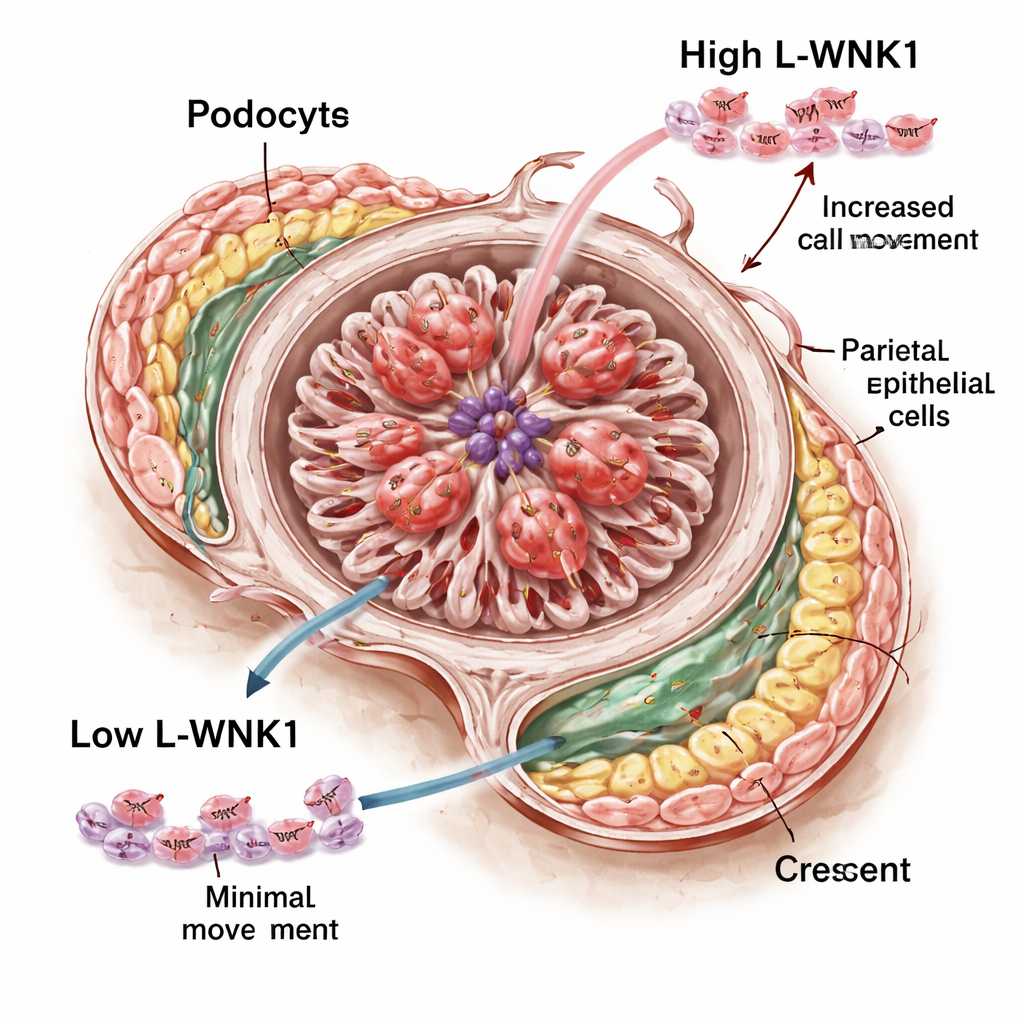
Ce que cela signifie pour les traitements futurs
Dans l'ensemble, l'étude met en évidence L-WNK1 comme un accélérateur nocif dans une forme violente d'inflammation rénale : lorsque cette protéine est suractivée, les cellules clés du glomérule se déplacent et prolifèrent de manière à obstruer et fibroser les filtres ; lorsque son activité est réduite, les lésions sont atténuées. Comme L-WNK1 est déjà étudiée comme cible médicamenteuse pour l'hypertension, ces résultats ouvrent la possibilité que des inhibiteurs finement dosés puissent un jour contribuer à protéger les patients atteints de maladies rénales rapidement progressives. Il reste beaucoup de travail pour traduire des résultats de souris et de cultures cellulaires en thérapies sûres, mais L-WNK1 apparaît désormais comme un nouveau point d'appui prometteur sur une affection par ailleurs dévastatrice.
Citation: Mousseaux, C., Migeon, T., Frère, P. et al. Knock-down of the long isoform of the WNK1 kinase mitigates the anti-glomerular basement membrane glomerulonephritis in mice. Sci Rep 16, 7335 (2026). https://doi.org/10.1038/s41598-026-36715-8
Mots-clés: glomérulonéphrite rapidement progressive, inflammation rénale, podocytes, crêtes glomérulaires, inhibition de WNK1