Clear Sky Science · fr
Application d’une Lactococcus exprimant la protéine de type collagène 1 du streptocoque du groupe A comme nouvelle immunothérapie contre l’adénocarcinome canalaire pancréatique
Transformer des bactéries amies en combattantes contre le cancer
Le cancer du pancréas fait partie des cancers les plus meurtriers, en partie parce qu’il se protège derrière des défenses puissantes qui neutralisent le système immunitaire. Cette étude explore un allié inattendu dans la lutte contre cette maladie : une bactérie « bénéfique » courante issue du monde laitier, ré‑ingénierée pour cibler les tumeurs pancréatiques et aider le système immunitaire à les attaquer plus efficacement. En empruntant une protéine de surface adhésive à un streptocoque pathogène, les chercheurs ont transformé un microbe inoffensif en un outil anti‑cancer ciblé chez la souris.
Un cancer coriace qui dupe le système immunitaire
L’adénocarcinome canalaire pancréatique est notoirement létal, avec seulement environ un patient sur huit vivant cinq ans après le diagnostic. Une raison majeure est son microenvironnement tumoral : une coque dense, quasi cicatricielle, riche en cellules et en molécules de soutien qui atténuent les attaques immunitaires et bloquent de nombreux médicaments. Parmi les coupables figurent les filets extracellulaires de neutrophiles, ou NETs — des enchevêtrements d’ADN et de protéines que les globules blancs projettent alentour. Dans le cancer du pancréas, ces filets adhésifs font plus de mal que de bien : ils favorisent la croissance tumorale, empêchent les cellules T tueuses d’agir et sont associés à un pronostic plus mauvais. Neutraliser les NETs tout en réveillant l’immunité anti‑tumorale est devenu une stratégie séduisante.
Emprunter une protéine adhésive, sans le germe dangereux
Des travaux antérieurs ont montré qu’une protéine de surface du streptocoque du groupe A, appelée Scl1, peut à la fois se lier aux fibres associées aux tumeurs et réduire la formation des NETs, ralentissant ainsi la croissance des tumeurs pancréatiques chez la souris. Mais le streptocoque du groupe A est aussi la bactérie responsable de l’angine et d’infections invasives graves, ce qui la rend inadaptée comme thérapie vivante. Pour conserver la protéine utile tout en évitant le germe dangereux, l’équipe a modifié Lactococcus lactis — un probiotique largement utilisé dans l’alimentation et considéré comme sûr — pour afficher Scl1 à sa surface. Cette nouvelle souche, baptisée Lactococcus::620, a été testée chez des souris porteuses de tumeurs pancréatiques, à la fois sur des tumeurs implantées en sous‑cutané (flanc) et sur des tumeurs plus réalistes se développant directement dans le pancréas.
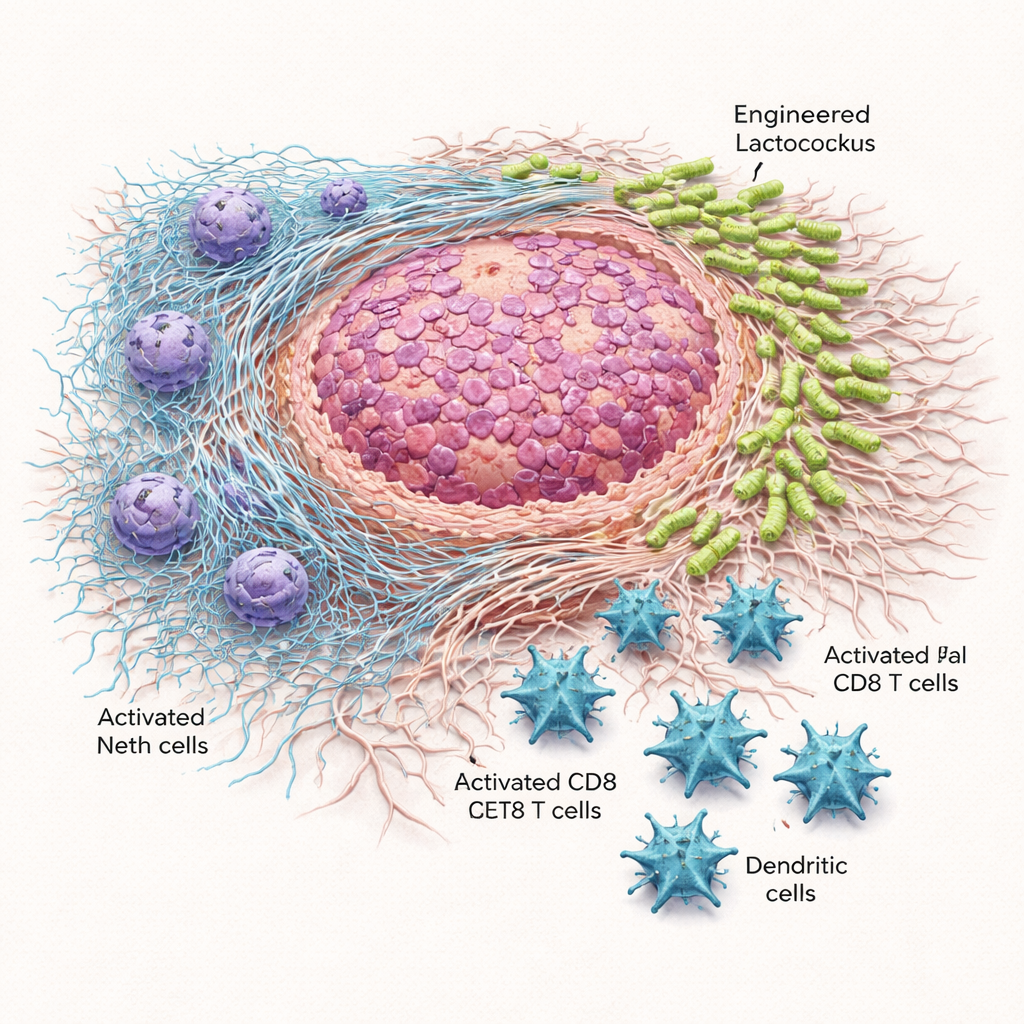
Des bactéries guidées réduisent la croissance tumorale et prolongent la survie
Lorsqu’une seule dose des bactéries modifiées a été injectée directement dans des tumeurs du flanc, ou administrée dans la cavité abdominale, les tumeurs ont crû plus lentement et pesé moins que chez les souris ayant reçu Lactococcus ordinaire ou un témoin salin. Dans le modèle pancréatique plus exigeant, des doses répétées tous les trois jours ont été nécessaires, mais les bénéfices furent nets. Lactococcus::620 a réduit la taille et le poids des tumeurs et prolongé la survie des animaux sans entraîner de décès liés au traitement. La microscopie et la culture des tissus tumoraux ont montré que les bactéries porteuses de Scl1 s’accumulaient de manière fiable dans la zone tumorale, en particulier dans la matrice fibreuse déposée par les fibroblastes associés aux cancers, tout en épargnant dans une large mesure la rate. En revanche, Lactococcus non modifié se diffusait plus largement dans l’organisme et était parfois toxique lorsqu’il était administré par voie systémique.
Désarmer les filets nocifs et laisser entrer les cellules immunitaires
Les bactéries modifiées ont aussi remodelé le paysage immunitaire autour des tumeurs. Les tumeurs des souris traitées par Lactococcus::620 contenaient davantage de lymphocytes T CD8 « tueurs » et de cellules dendritiques — acteurs clés de la reconnaissance et de la destruction des cellules cancéreuses — et ces lymphocytes affichaient moins de marqueurs d’épuisement et plus de molécules liées à l’activité. Parallèlement, les indicateurs d’activité des NETs ont diminué. En tests de laboratoire, les neutrophiles exposés à Lactococcus::620 ont libéré moins d’ADN libre et montré une activité réduite de la myéloperoxydase, une enzyme nécessaire à la mise en place des NETs. Chez les animaux traités, l’ADN circulant associé aux NETs a été réduit. De manière cruciale, lorsque les mêmes expériences ont été réalisées chez des souris génétiquement incapables de former des NETs, les bactéries modifiées n’ont plus ralenti la croissance tumorale. Cette perte d’efficacité suggère fortement que l’inhibition des NETs est au cœur du pouvoir thérapeutique.
Ce que cela pourrait signifier pour les soins du cancer à l’avenir
Globalement, les résultats esquissent un nouveau concept : utiliser une bactérie sûre, de qualité alimentaire, comme vecteur programmable pour déposer une protéine homing qui bloque les NETs directement dans l’environnement hostile du cancer pancréatique. Chez la souris, cette approche a réduit la charge tumorale, amélioré la survie et permis aux cellules immunitaires d’agir plus efficacement. Bien qu’il reste beaucoup à faire avant d’envisager un essai chez l’humain — y compris des tests sur des modèles de maladie métastatique et des combinaisons avec les immunothérapies modernes — l’étude montre que des bactéries « bonnes » soigneusement modifiées pourraient un jour contribuer à inverser la tendance face à l’un de nos cancers les plus résistants.
Citation: Godfrey, E.A., Choi, S.J., Sestito, M. et al. Application of group A streptococcal collagen-like protein 1-expressing Lactococcus as a novel immunotherapeutic against pancreatic ductal adenocarcinoma. Sci Rep 16, 5911 (2026). https://doi.org/10.1038/s41598-026-36657-1
Mots-clés: cancer du pancréas, thérapie probiotique, <keyword>modulation immunitaire, filets extracellulaires de neutrophiles