Clear Sky Science · fr
Effets combinés des nitrates et des composés antimicrobiens sur des biofilms sous‑gingivaux in vitro
Pourquoi vos gencives et les médicaments agissant sur l’intestin sont liés
Les gencives qui saignent et les maladies parodontales sont généralement attribuées à des bactéries « nuisibles ». Pour les combattre, les dentistes ont souvent recours à des bains de bouche puissants et à des antibiotiques. Cette étude pose une question plus large : et si certains de ces traitements endommageaient discrètement les bactéries utiles dont nous avons besoin, tandis qu’un simple nutriment présent dans les légumes à feuilles orientait nos microbes buccaux vers un état de santé ?
La maladie des gencives comme problème communautaire
La parodontite est une infection prolongée autour des dents qui détruit les tissus qui les maintiennent en place et est associée aux maladies cardiaques, au diabète et même à des troubles cérébraux. Plutôt que d’être causée par un germe unique, elle survient lorsque l’ensemble de la communauté bactérienne buccale bascule vers un état nuisible, appelé dysbiose. Le traitement moderne repose encore largement sur des médicaments à large spectre : des antibiotiques comme l’amoxicilline et le métronidazole, et des bains antiseptiques tels que la chlorhexidine. Ces produits peuvent éliminer les agents pathogènes — mais ils peuvent aussi anéantir les bactéries amies et encourager l’apparition de résistances aux médicaments.
Un regard détaillé sur des biofilms issus de patients réels
Pour voir ce que ces traitements font réellement aux bactéries des gencives, les chercheurs ont prélevé du tartre dans des poches profondes autour des dents de 12 personnes atteintes de parodontite. En laboratoire, ils ont cultivé ces échantillons sous forme de fines couches bactériennes, ou biofilms, pendant huit heures dans huit conditions différentes : sans traitement, avec nitrate seul, avec chaque médicament seul, et avec chaque médicament combiné au nitrate. Le nitrate, un composé naturel abondant dans les épinards, la laitue et la betterave, peut être transformé par certaines bactéries buccales en oxyde nitrique, un gaz qui aide les vaisseaux sanguins à se détendre et peut ralentir la croissance des microbes liés à la maladie. L’équipe a mesuré la quantité de biofilm formée, l’efficacité de conversion du nitrate et quelles espèces bactériennes prospéraient sous chaque traitement.
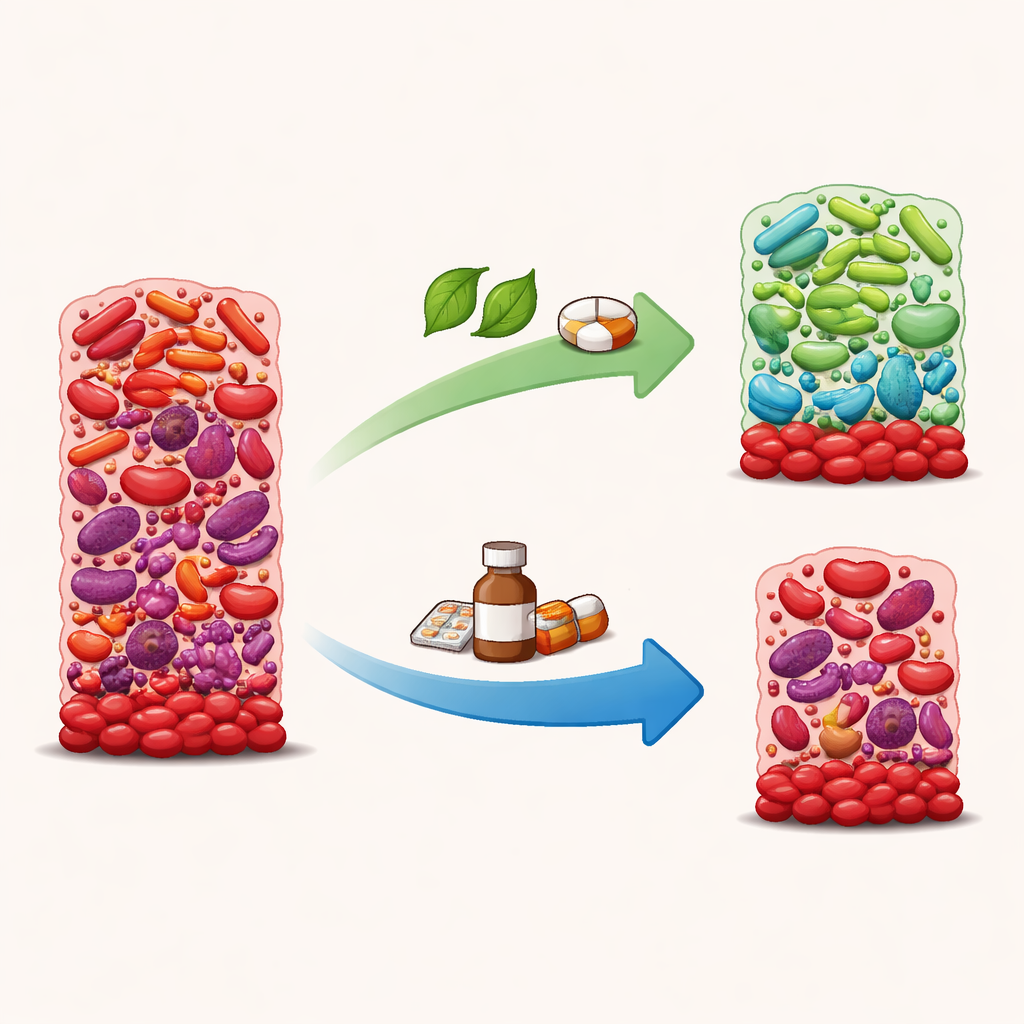
Des médicaments qui réduisent la croissance mais peuvent aggraver l’équilibre
De faibles doses de chlorhexidine et d’amoxicilline ont réduit la croissance du biofilm d’environ moitié et ont fortement diminué la capacité des bactéries à traiter le nitrate. Mais il ne s’agissait pas d’un « nettoyage sélectif ». Le séquençage de l’ADN a montré que, dans ces conditions, des bactéries associées à la santé comme Rothia, Gemella et Kingella avaient tendance à décliner, tandis que plusieurs espèces liées à la maladie des gencives — notamment Fusobacterium, Treponema et Eubacterium — restaient présentes ou devenaient plus dominantes. Un indice évaluant à quel point une communauté paraît « malade » était plus élevé avec la chlorhexidine et l’amoxicilline qu’avec le nitrate, ce qui suggère que ces médicaments peuvent pousser le biofilm vers un état plus nocif et déséquilibré même s’ils répriment la croissance globale.
Un carburant tiré des légumes à feuilles et un antibiotique plus doux
Le nitrate raconte une autre histoire. Lorsque le tartre a été cultivé avec du nitrate seul, les bactéries spécialisées dans la transformation du nitrate en produits utiles, telles que Neisseria et certaines espèces d’Aggregatibacter, ont augmenté. Le score de dysbiose a diminué par rapport aux conditions avec chlorhexidine ou amoxicilline, indiquant une communauté plus saine. Le métronidazole, à un niveau comparable à ce qui atteint réellement les poches gingivales chez les patients, n’a pas fortement réduit la croissance ni l’utilisation du nitrate lorsqu’il était utilisé seul. Mais combiné au nitrate, il semblait faire pencher la balance de manière favorable : des espèces associées à la maladie comme Fusobacterium et Treponema ont diminué, tandis que des nitrateréductrices telles que Neisseria et Kingella ont augmenté. Cette association a semblé élaguer les pires coupables sans éliminer des fonctions clés.
Ce que cela signifie pour les soins quotidiens
Pour les personnes atteintes de maladies des gencives, ces résultats suggèrent que « le plus fort » n’est pas toujours « le mieux » en matière d’antimicrobiens. Dans ce modèle de laboratoire, de faibles doses de chlorhexidine et d’amoxicilline ont ralenti la croissance bactérienne mais ont aussi affaibli une voie naturelle basée sur le nitrate qui soutient à la fois la santé buccale et générale, et elles étaient associées à des profils microbiens plus proches de la maladie. Le nitrate, notamment lorsqu’il était associé au métronidazole, favorisait des bactéries liées à des gencives plus saines et préservait le métabolisme du nitrate. Bien que la bouche réelle soit plus complexe que la boîte de Pétri, ce travail soutient l’idée de stratégies plus douces et respectueuses du microbiome — telles qu’un régime riche en nitrates et des antibiotiques choisis avec soin — pour gérer la parodontite sans compromettre les bactéries qui nous aident à rester en bonne santé.
Citation: Moran, S.P., Nadal-Ruiz, M., Mira, A. et al. Combined effects of nitrate and antimicrobial compounds on in vitro subgingival biofilms. Sci Rep 16, 6686 (2026). https://doi.org/10.1038/s41598-026-36588-x
Mots-clés: maladie des gencives, microbiome buccal, nitrate, bain de bouche, antibiotiques