Clear Sky Science · fr
Diagnostic de la maladie d’Alzheimer avec haute précision via la modélisation par réseaux de Petri des voies de signalisation
Pourquoi la détection précoce des maladies cérébrales nous concerne tous
La maladie d’Alzheimer érode lentement la mémoire et l’autonomie, souvent bien avant l’apparition de symptômes évidents. Les outils diagnostiques actuels, comme les scanners cérébraux et les tests cognitifs, peuvent être coûteux, difficiles d’accès et peu sensibles aux tout premiers stades. Cette étude propose une nouvelle manière d’examiner le « câblage » moléculaire du corps à partir d’échantillons sanguins ou cérébraux en utilisant un cadre mathématique appelé réseau de Petri. L’objectif est simple mais important : déterminer, avec une très grande précision, si le profil d’activité génique d’une personne ressemble davantage à celui d’une personne saine ou à celui d’une personne atteinte d’Alzheimer — idéalement suffisamment tôt pour infléchir la trajectoire de la maladie.
Lire la maladie dans les « circuits » de signalisation du corps
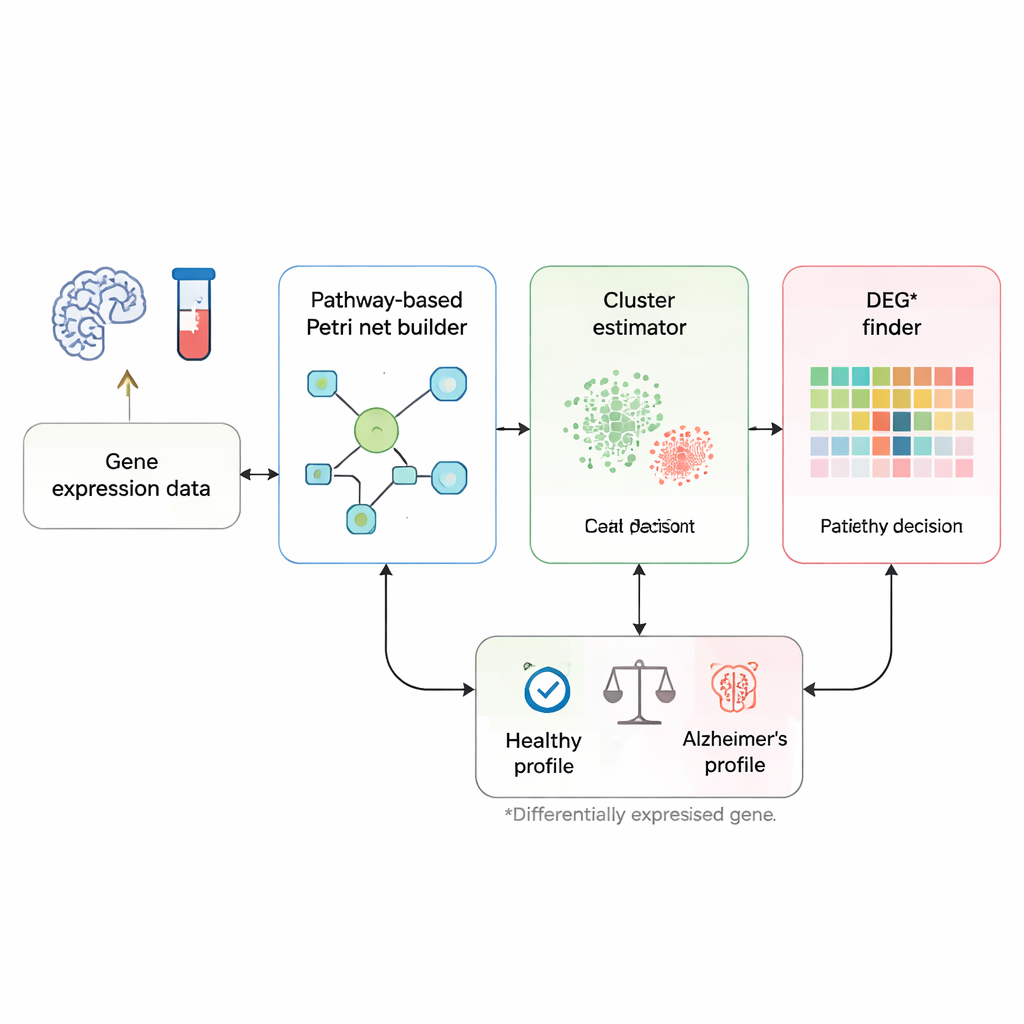
Plutôt que de considérer chaque gène comme un marqueur isolé, les chercheurs se concentrent sur la façon dont les gènes communiquent entre eux via des voies de signalisation biologiques connues et liées à la maladie d’Alzheimer. Ils partent d’une carte de voie soigneusement répertoriée dans la base KEGG, qui énumère les gènes et les relations d’activation ou d’inhibition entre eux. Cette voie est transformée en réseau de Petri — une sorte de diagramme de flux où les cercles représentent des gènes, les rectangles des interactions, et de petits jetons des signaux se déplaçant dans le réseau. Lorsqu’un jeton parcourt la voie jusqu’à des nœuds « maladie » finaux, il symbolise une chaîne d’événements géniques pouvant conduire à la mort des cellules cérébrales et à la démence.
D’un échantillon sanguin à une réponse oui/non
La méthode commence par des profils d’expression génique : des mesures indiquant l’activité de milliers de gènes dans le sang ou le tissu cérébral d’une personne. D’abord, un « estimateur de cluster » personnalisé compare un nouvel échantillon à des échantillons étiquetés auparavant (sains et malades), en se concentrant sur les gènes déjà connus pour différer entre ces groupes. Pour chaque gène, l’outil identifie les échantillons d’entraînement ayant des niveaux d’expression les plus semblables et utilise une forme de vote de voisinage pour attribuer au nouvel échantillon une étiquette initiale, probablement sain ou probablement malade. Cette étape forme deux groupes de travail, ou clusters, d’échantillons : l’un représentant les profils typiques sains et l’autre les profils typiques d’Alzheimer.
Identifier les gènes les plus révélateurs pour chaque personne
Vient ensuite une étape plus personnalisée. Pour une personne donnée, la méthode examine gène par gène où ses niveaux d’expression se situent réellement. Pour chaque gène, elle compare la valeur individuelle à l’étendue observée dans le cluster sain et dans le cluster patient, en utilisant des statistiques robustes qui atténuent l’influence des valeurs aberrantes bruyantes. Si l’expression d’un gène se trouve clairement dans la plage « malade » et en dehors de la plage saine, il est signalé comme DEG*, un gène particulièrement informatif pour cet individu. Ces gènes DEG* reçoivent des jetons initiaux dans le réseau de Petri, marquant les points où l’activité anormale apparaît en premier dans le circuit de signalisation.
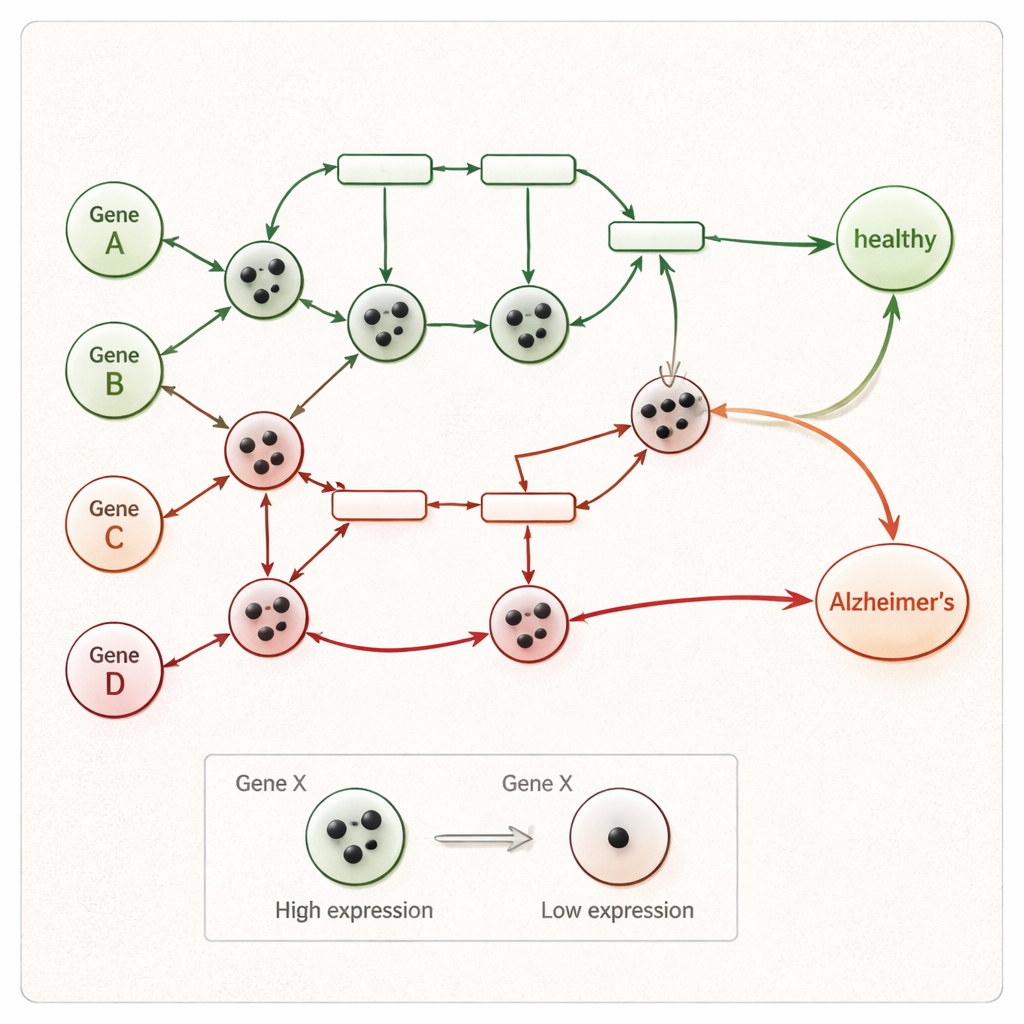
Laisser le réseau évoluer jusqu’au diagnostic
Une fois les jetons placés, le réseau de Petri s’exécute étape par étape. À chaque étape, chaque interaction dont les gènes d’entrée ont suffisamment de jetons « déclenche », déplaçant des jetons vers les gènes en aval tout en respectant les règles d’activation et d’inhibition. Cela continue jusqu’à ce qu’aucun mouvement supplémentaire ne soit possible. Si, à la fin, au moins un jeton atteint le nœud final de maladie du réseau — représentant des processus tels que la mort neuronale ou la neurodégénérescence — l’échantillon est classé comme Alzheimer ; sinon, il est étiqueté sain. Parce que chaque étape de déclenchement est enregistrée, les chercheurs peuvent retracer un chemin clair depuis l’activité génique inhabituelle d’une personne jusqu’à un résultat sain ou malade, plutôt que de s’appuyer sur un score statistique opaque.
Quelle est la précision de cette approche en pratique ?
L’équipe a testé leur cadre sur plusieurs grands jeux de données publics d’expression génique provenant du sang et du tissu cérébral. Sur deux jeux de données sanguines largement utilisés, leur méthode a correctement distingué les patients Alzheimer des personnes saines dans environ 98–99 % des cas, dépassant largement les approches d’apprentissage automatique antérieures qui atteignaient souvent seulement 65–81 % de précision. Ils ont également montré de solides performances sur d’autres jeux de données cérébrales et sanguines, même lorsque le nombre d’échantillons était faible. Fait important, contrairement à de nombreux concurrents, leur méthode n’a pas écarté les échantillons bruyants ou difficiles à interpréter ; elle utilise au contraire sa conception interne pour gérer la variabilité tout en conservant toutes les données dans l’analyse.
Ce que cela signifie pour les tests Alzheimer à venir
Pour le grand public, le message principal est que l’étude transforme la complexité génétique et les diagrammes de voies en un processus décisionnel clair et séquentiel capable de lire les signes précoces de la maladie d’Alzheimer à partir d’un simple échantillon, potentiellement même du sang. En modélisant la façon dont les gènes anormaux agissent ensemble, et pas seulement individuellement, le cadre des réseaux de Petri offre à la fois une haute précision diagnostique et une « histoire » compréhensible de la façon dont la maladie peut se dérouler chez chaque personne. Bien que ce travail reste de la recherche et ne soit pas encore un test clinique, il ouvre la voie à des outils futurs capables de détecter Alzheimer plus tôt, d’orienter les choix thérapeutiques et, éventuellement, d’être adaptés à d’autres maladies cérébrales et cancers en utilisant la même idée de base.
Citation: Ebrahimian, H., Asadzadeh, F., Rahgozar, M. et al. Diagnosis of Alzheimer’s disease with high accuracy via Petri net modeling of signaling pathways. Sci Rep 16, 6457 (2026). https://doi.org/10.1038/s41598-026-36585-0
Mots-clés: Diagnostic de la maladie d’Alzheimer, expression génique, voies de signalisation, modélisation par réseaux de Petri, biomarqueurs sanguins