Clear Sky Science · fr
Le microenvironnement tumoral dans le cancer de l’œsophage et son association avec les caractéristiques cliniques et la réponse au traitement néoadjuvant
Pourquoi le voisinage de la tumeur compte
Le cancer de l’œsophage fait partie des cancers les plus meurtriers au monde, et même avec des protocoles modernes de chimiothérapie et de radiothérapie, de nombreux patients ne répondent pas aussi bien qu’espéré. Cette étude pose une question apparemment simple mais aux grandes implications : que se passe-t-il dans le « voisinage » de la tumeur — le microenvironnement tumoral — et sa composition peut‑elle aider à expliquer pourquoi certains patients répondent au traitement alors que d’autres non ? En examinant de près les cellules immunitaires et les marqueurs associés avant et après la thérapie, les chercheurs commencent à cartographier comment l’organisme et la tumeur interagissent, et comment ce dialogue caché pourrait orienter des traitements futurs plus personnalisés.
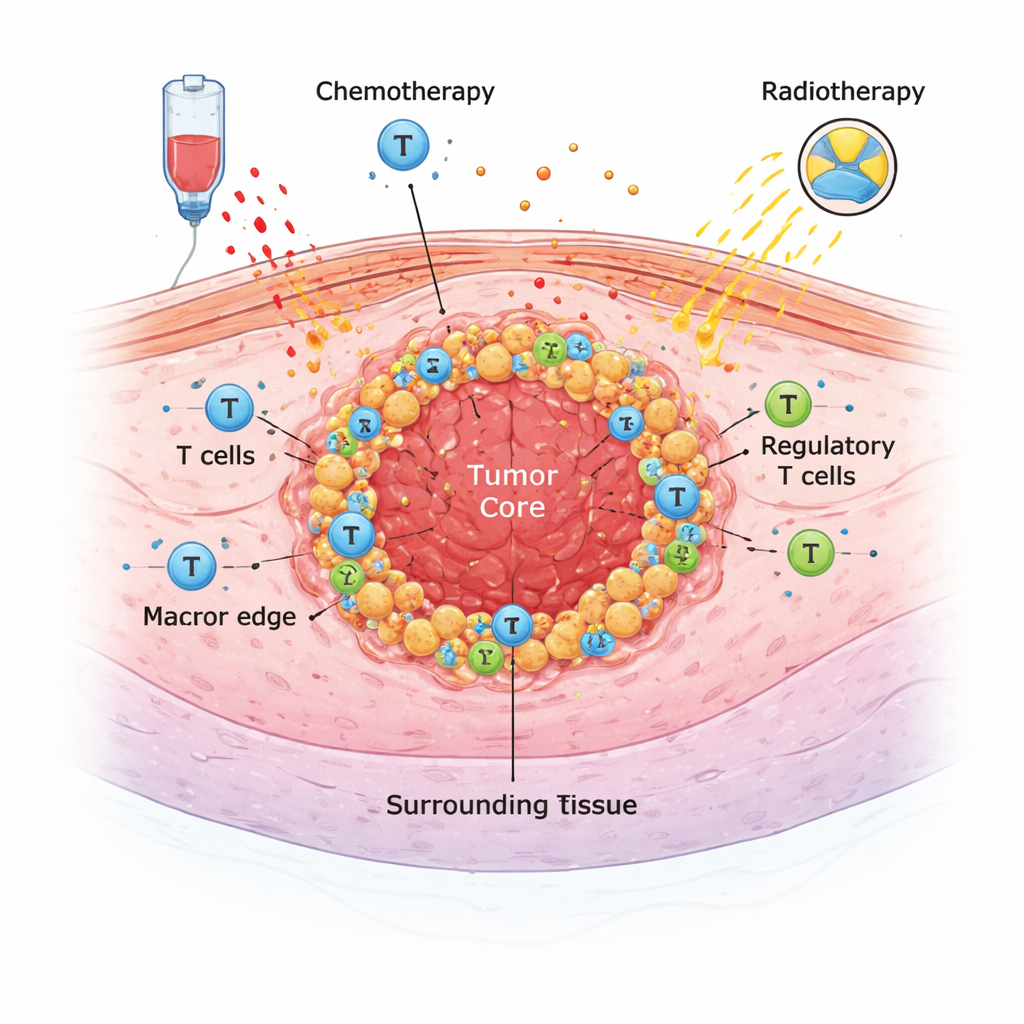
L’écosystème caché autour d’une tumeur
Les tumeurs solides ne croissent pas isolément. Elles évoluent au sein d’un écosystème complexe de cellules immunitaires, de cellules de soutien et de molécules de signalisation connu sous le nom de microenvironnement tumoral. Dans cette étude, des médecins et des pathologistes de Lausanne ont examiné des échantillons tumoraux de 68 patients ayant subi une chirurgie pour cancer de l’œsophage entre 2009 et 2021. La plupart avaient reçu un traitement puissant avant l’intervention — chimiothérapie, radio‑chimiothérapie ou les deux — pour réduire la tumeur. À l’aide de colorations spécifiques sur des lames de tissu, l’équipe a compté plusieurs types clés de cellules immunitaires (incluant les lymphocytes T en général, les lymphocytes T cytotoxiques et différents types de macrophages) et a mesuré des marqueurs pouvant prédire la réponse à l’immunothérapie, tels que PD‑L1 et HER2.
Qui étaient les patients et ce qui a été mesuré
Les patients de cette série étaient majoritairement des hommes d’une soixantaine d’années, et la majorité présentait un adénocarcinome, le type de cancer œsophagien souvent lié au reflux acide chronique et à l’œsophage de Barrett. Un plus petit groupe avait un carcinome épidermoïde, une forme différente qui prend naissance dans les cellules squameuses de la muqueuse œsophagienne. Les chercheurs ont soigneusement relié ce qu’ils observaien t au microscope aux données cliniques telles que le stade de la maladie, le statut tabagique, la perte de poids et le type de traitement préopératoire reçu. Ils ont également suivi l’ampleur de la réponse tumorale à la thérapie, en employant un système de gradation qui distingue la disparition complète des cellules cancéreuses d’une réponse faible ou absente.
Mode de vie, type tumoral et une présence immunitaire plus discrète
Plusieurs facteurs liés au quotidien et à la maladie se sont révélés associés à une présence immunitaire moindre autour de la tumeur. Les patients fumeurs actifs présentaient moins de macrophages au total et moins de macrophages dits de type M2, souvent associés au support tumoral et à l’immunosuppression. Les personnes avec des tumeurs plus avancées, une perte de poids préopératoire importante ou des carcinomes épidermoïdes avaient tendance à avoir moins de lymphocytes T et de macrophages infiltrant leurs tumeurs. En revanche, les tumeurs avec des scores PD‑L1 élevés — un indicateur souvent utilisé pour sélectionner des patients pour l’immunothérapie — étaient « plus chaudes », avec davantage de lymphocytes T et de macrophages, mais ce profil a déjà été lié à de moins bons résultats, probablement parce que la tumeur utilise activement PD‑L1 pour désactiver l’attaque immunitaire.
Comment le traitement reconfigure le voisinage tumoral
Le traitement néoadjuvant (avant chirurgie) a profondément remodelé le microenvironnement tumoral. La chimiothérapie comme la radio‑chimiothérapie ont augmenté le nombre de macrophages, y compris de cellules de type M2, tout en réduisant nettement les lymphocytes T régulateurs, un groupe qui atténue normalement les réponses immunitaires. Les effectifs totaux de lymphocytes T et de lymphocytes T cytotoxiques ont varié de façon moins cohérente. Fait intéressant, la radio‑chimiothérapie tendait à diminuer les niveaux de PD‑L1 sur les cellules tumorales et environnantes, réduisant la proportion de patients avec des scores PD‑L1 élevés après le traitement. Cela suggère que le traitement standard peut rendre les tumeurs moins adaptées, au regard d’un seul prélèvement post‑traitement, aux immunothérapies ciblant la voie PD‑1/PD‑L1.
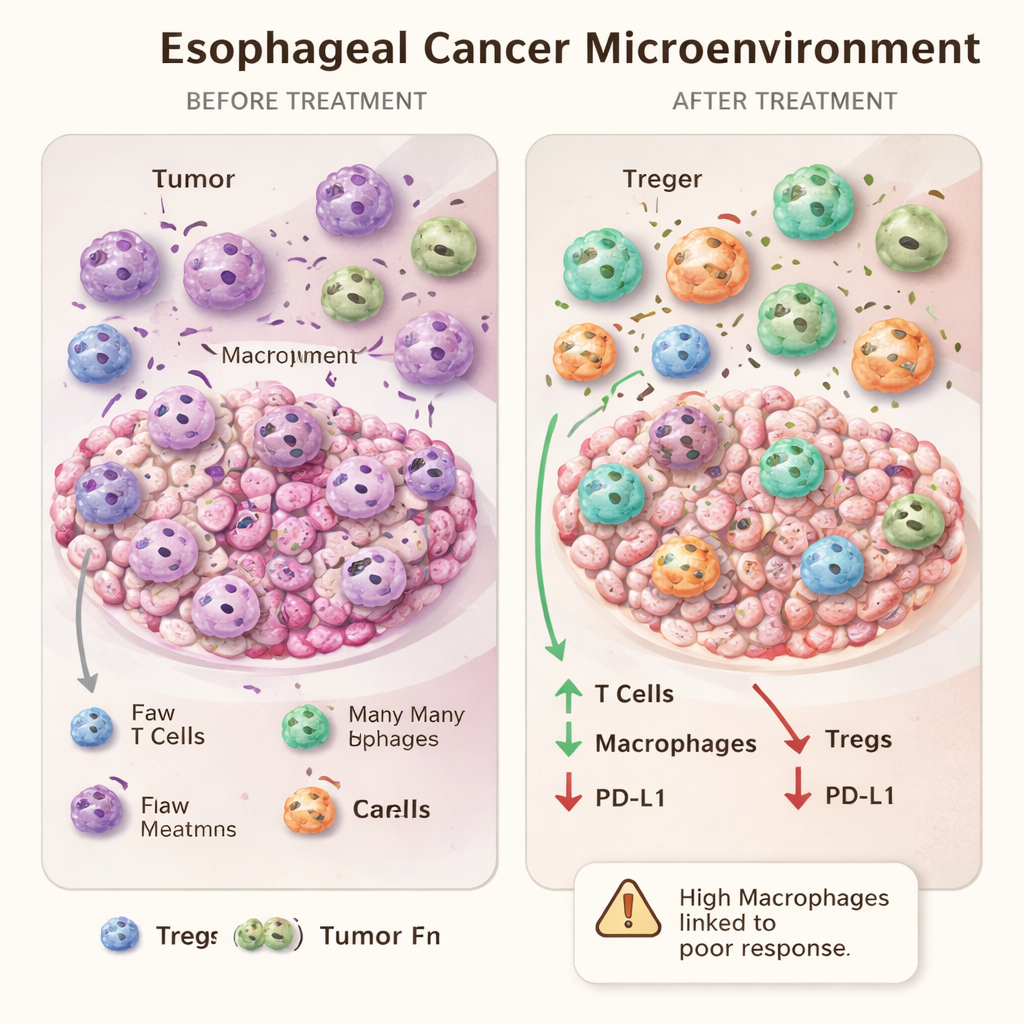
Quand davantage de cellules immunitaires peut signaler une résistance
Une des observations les plus intrigantes est venue de la comparaison des extrêmes de réponse au traitement. Les patients dont les tumeurs avaient disparu complètement au microscope ne différaient pas, au départ, des mauvais répondeurs en ce qui concerne les cellules immunitaires entourant leur cancer. Cependant, après traitement, les mauvais répondeurs présentaient un nombre plus élevé de macrophages dans les zones tumorales que les répondeurs complets. Plutôt que d’être un simple signe d’immunité vigoureuse, une abondance de macrophages après thérapie peut marquer une réponse épuisée ou biaisée que la tumeur a appris à exploiter. Cela renforce l’idée que certains macrophages, en particulier de type M2, peuvent en réalité favoriser la survie tumorale et la résistance.
Ce que cela implique pour les soins futurs
Pour les patients et les cliniciens, la conclusion est que la biologie entourant une tumeur œsophagienne — son microenvironnement — est façonnée par le tabagisme, le type tumoral, la gravité de la maladie et par les traitements eux‑mêmes. La chimiothérapie et la radio‑chimiothérapie standard ne se contentent pas de réduire la taille des tumeurs ; elles recrutent et reconfigurent aussi les cellules immunitaires de manières qui peuvent aider ou entraver le contrôle à long terme de la maladie. L’étude suggère que le comptage de certaines cellules immunitaires, en particulier les macrophages, avant et après la thérapie pourrait un jour aider à identifier qui est susceptible de résister au traitement et qui pourrait bénéficier de médicaments supplémentaires ciblant ces cellules ou la voie PD‑1/PD‑L1. Bien que des études plus larges soient nécessaires, ce travail nous rapproche d’un traitement du cancer de l’œsophage adapté non seulement à la génétique de la tumeur mais aussi à l’écosystème dynamique qui l’entoure.
Citation: Fasquelle, F., Teixeira Farinha, H., Sempoux, C. et al. The tumor microenvironment in esophageal cancer and its association with clinical features and neoadjuvant treatment response. Sci Rep 16, 5664 (2026). https://doi.org/10.1038/s41598-026-36537-8
Mots-clés: cancer de l’œsophage, microenvironnement tumoral, cellules immunitaires, chimiothérapie-radiothérapie, immunothérapie