Clear Sky Science · fr
Construction et validation initiale d’un réseau génique clé de la résistance au progestatif dans le cancer de l’endomètre basée sur un criblage CRISPR à l’échelle du génome
Pourquoi certains cancers utérins cessent d’écouter les hormones
Pour de nombreuses personnes atteintes d’un cancer de l’endomètre au stade précoce qui souhaitent encore avoir des enfants, des comprimés hormonaux mimant la progestérone naturelle peuvent réduire les tumeurs tout en préservant l’utérus. Pourtant, jusqu’à un tiers de ces cancers ne répondent jamais ou deviennent rapidement résistants, obligeant les patient·e·s à envisager une chirurgie ou des traitements plus agressifs. Cette étude utilise un puissant outil d’édition génique pour cartographier les gènes qui font que les cellules du cancer de l’endomètre ignorent la progestérone, ouvrant la voie à des tests et des médicaments futurs susceptibles de prolonger l’efficacité de cette thérapie.
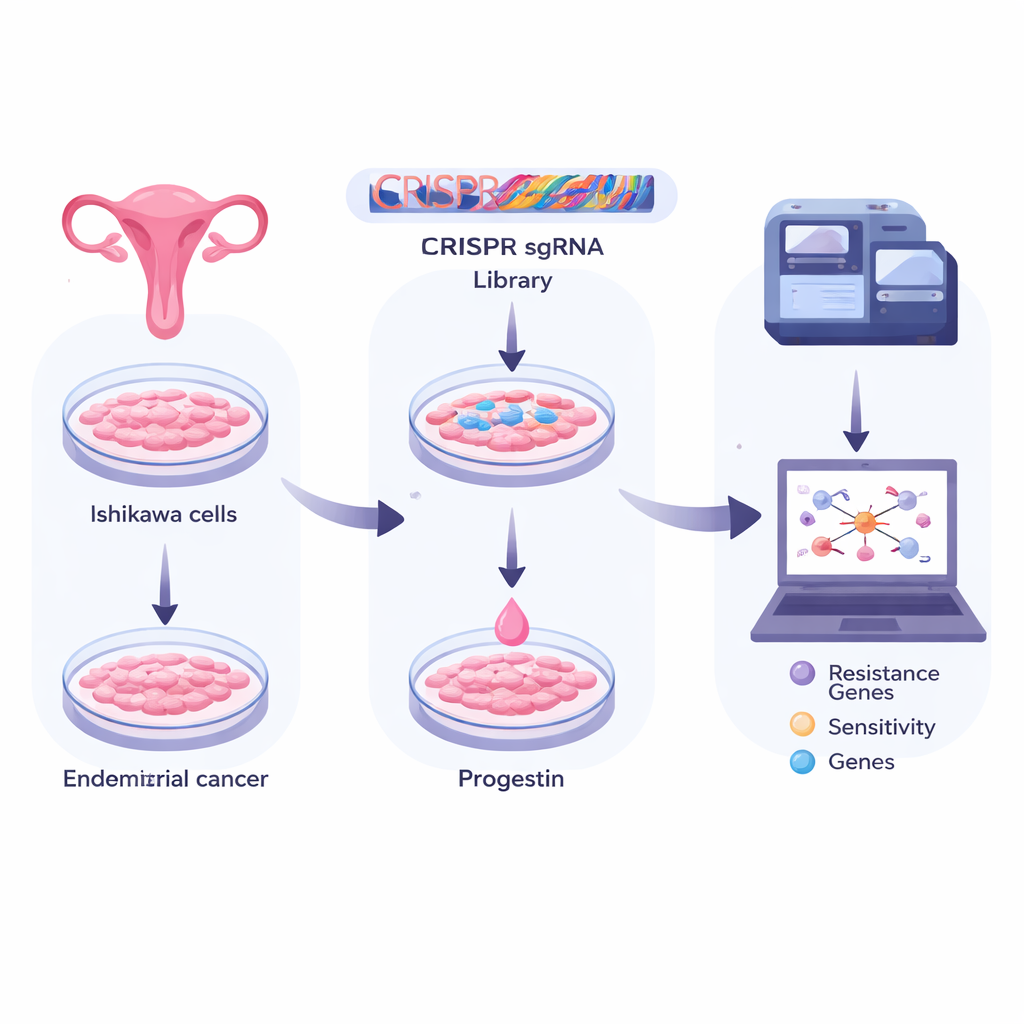
Utiliser des ciseaux génétiques pour sonder le génome entier
Les chercheurs ont travaillé avec des cellules Ishikawa, un modèle couramment utilisé du cancer de l’endomètre. Ils ont infecté des millions de ces cellules avec une bibliothèque de « ciseaux » CRISPR, chacun programmé pour couper un gène humain différent. Cela a créé une vaste population où, en principe, chaque cellule avait un gène unique désactivé. L’équipe a ensuite séparé les cellules en groupes : un conservé comme ligne de base, un exposé uniquement à un solvant inerte, et un traité pendant de nombreux jours avec un progestatif synthétique courant (méthylprednisolone n’est pas correct ici — medroxyprogestérone, ou MPA). En séquençant en profondeur les balises CRISPR présentes dans chaque groupe, ils ont pu voir quelles inactivations géniques aidaient les cellules à survivre ou les rendaient vulnérables sous traitement progestatif.
Distinguer les gènes qui aident ou entravent la réponse au médicament
L’analyse de ce flux massif de données a nécessité des statistiques sophistiquées. L’équipe a appliqué deux méthodes complémentaires, RRA et MLE, pour classer les gènes selon la force avec laquelle ils protégeaient les cellules de la progestérone (gènes de résistance) ou rendaient les cellules plus susceptibles de mourir (gènes de sensibilité). Ils ont trouvé des centaines de candidats dans chaque catégorie. Beaucoup de ces gènes se regroupaient dans des voies impliquées dans la réplication et la réparation de l’ADN, la synthèse et le traitement de l’ARN, et le métabolisme cellulaire général. Autrement dit, la machinerie de base qui permet aux cellules de lire, maintenir et exploiter l’information génétique semble étroitement liée à la question de savoir si les cellules du cancer de l’endomètre obéissent au signal « arrêter de croître » de la progestérone.
Réduire la liste aux acteurs les plus importants
Pour éviter de poursuivre des pistes erronées, les scientifiques ont recoupé les hits CRISPR avec un ancien jeu de données de leur laboratoire, dans lequel ils avaient comparé des cellules cancéreuses ordinaires avec une lignée devenue résistante à la progestérone au fil du temps. En recherchant des gènes apparus dans les deux écrans et montrant des changements cohérents, ils ont réduit la liste à cinq gènes qui semblent favoriser la résistance et vingt qui semblent la contrer. Les bases de données publiques sur le cancer ont montré que de nombreux gènes bloquant la résistance sont plus actifs dans le type le plus courant de cancer de l’endomètre, tandis que plusieurs gènes favorisant la résistance corrèlent avec de moins bons résultats chez les patient·e·s, suggérant que ces signaux comptent dans de vraies tumeurs, et pas seulement en culture.
Tester des gènes clés dans des cellules et chez la souris
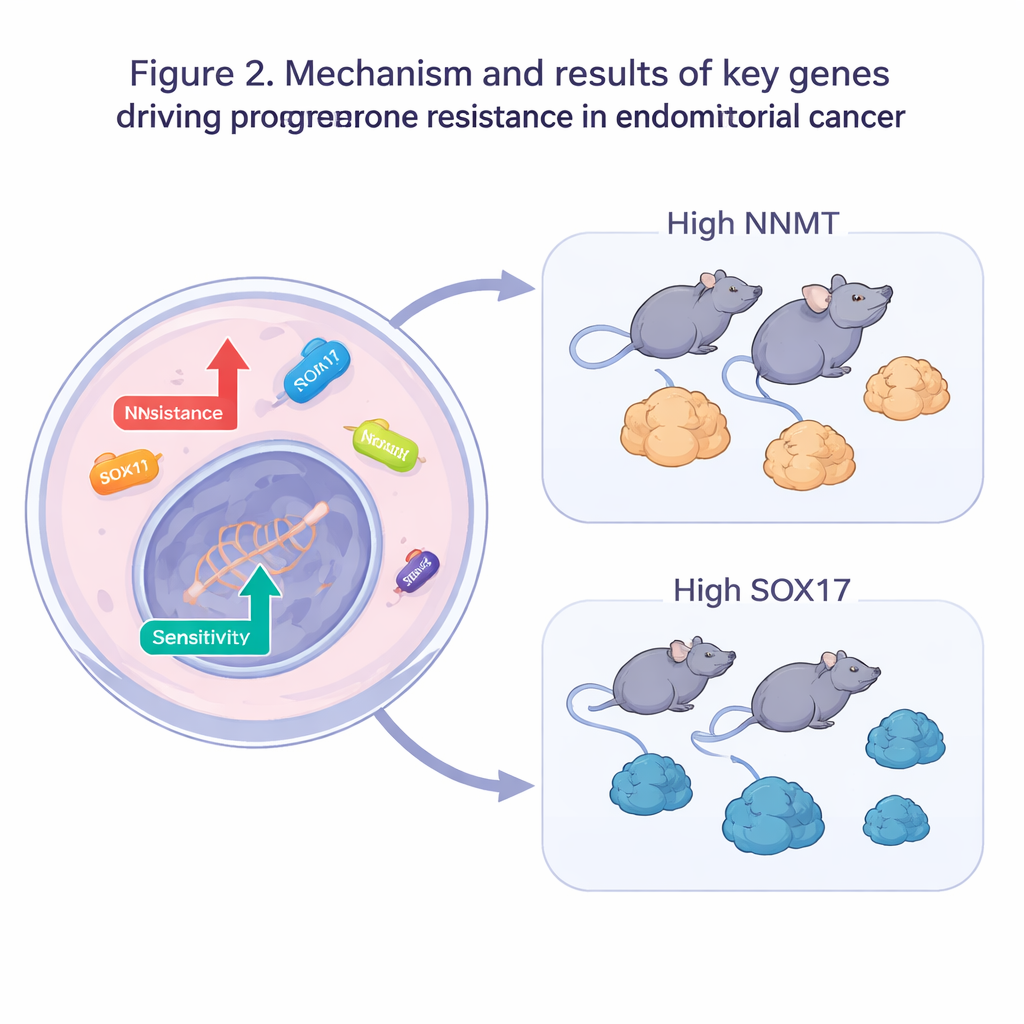
L’équipe est ensuite passée des grandes données aux expériences pratiques. Dans des cellules résistantes à la progestérone, ils ont éteint chacun des cinq gènes suspectés de conférer la résistance ou augmenté l’expression des cinq gènes suspectés de conférer la sensibilité. Lorsqu’on a exposé ces cellules modifiées à la progestérone, beaucoup plus sont mortes et des doses bien plus faibles du médicament étaient nécessaires pour ralentir la croissance, confirmant que modifier un seul gène pouvait restaurer la sensibilité hormonale. Deux gènes se sont démarqués : NNMT, impliqué dans le métabolisme cellulaire, et SOX17, un gène qui aide à contrôler le développement et le comportement cellulaire. Dans des modèles tumoraux murins, surexprimer NNMT a rendu les tumeurs moins réceptives à la progestérone, tandis qu’augmenter SOX17 a rendu les tumeurs résistantes plus sensibles au même traitement.
Ce que ces résultats pourraient signifier pour les patient·e·s
En termes simples, l’étude construit un premier « schéma de câblage » montrant comment les cellules du cancer de l’endomètre décident d’écouter ou non la progestérone. Elle suggère que la résistance ne se résume pas à la perte du récepteur de la progestérone, mais implique aussi des changements profonds dans la gestion de l’ADN et de l’ARN et dans des gènes de contrôle clés tels que NNMT et SOX17. À l’avenir, des tests sanguins ou tissulaires lisant ce réseau génique pourraient aider les médecins à prédire qui bénéficiera d’un traitement hormonal préservant la fertilité. Encore plus prometteur, des médicaments qui atténuent les gènes de résistance ou renforcent les gènes de sensibilité pourraient un jour être associés à la progestérone pour maintenir cette option thérapeutique plus douce efficace pour un plus grand nombre de personnes et plus longtemps.
Citation: Li, X., Wang, S., Qiu, Z. et al. Construction and initial validation of key gene network for progesterone resistance in endometrial cancer based on genome-wide CRISPR screening. Sci Rep 16, 8030 (2026). https://doi.org/10.1038/s41598-026-36534-x
Mots-clés: cancer de l’endomètre, résistance au progestatif, criblage CRISPR, réseaux géniques, hormonothérapie