Clear Sky Science · fr
Les modifications m6A de l’hôte façonnent le microbiote qui induit une ferroptose spécifique aux cellules comme voie causale des maladies respiratoires chroniques
Pourquoi vos microbes comptent pour vos poumons
Les problèmes respiratoires chroniques, comme l’asthme et la bronchopneumopathie chronique obstructive (BPCO), sont généralement attribués au tabagisme, à la pollution ou aux allergies. Cette étude suggère un acteur moins évident : les trillions de microbes vivant dans notre intestin et sur notre peau. À partir de vastes jeux de données génétiques, les auteurs montrent que certains microbes ne se contentent pas d’accompagner la maladie pulmonaire, ils peuvent contribuer à la provoquer — en agissant par de subtiles modifications chimiques dans nos cellules et par une forme de lésion cellulaire dépendante du fer. Comprendre ce réseau caché pourrait à terme conduire à des moyens nouveaux de prévenir ou traiter les maladies respiratoires chroniques en orientant nos microbes et leurs voies moléculaires vers des états plus sains.
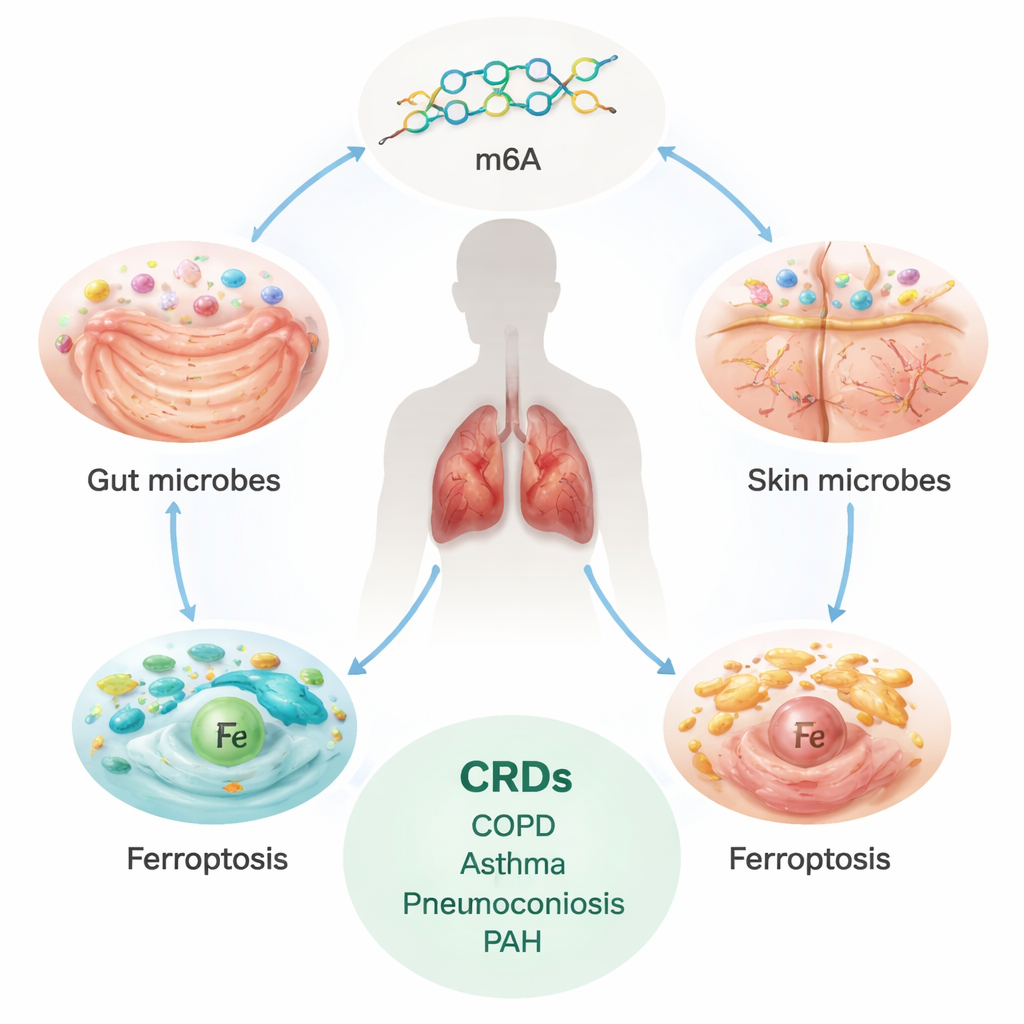
Le fardeau méconnu des maladies pulmonaires chroniques
Les maladies respiratoires chroniques, y compris la BPCO, l’asthme, les maladies pulmonaires interstitielles (MPI), les pneumoconioses et l’hypertension artérielle pulmonaire (HAP), touchent des centaines de millions de personnes dans le monde et causent des millions de décès chaque année. Ces affections évoluent souvent lentement mais inexorablement, entraînant cicatrisation ou remodelage des poumons et des vaisseaux sanguins, et laissant les personnes essoufflées. Les traitements actuels gèrent principalement les symptômes ; ils ne stoppent ni ne renversent totalement les dommages sous-jacents. Cela a poussé les scientifiques à rechercher des causes plus profondes, des facteurs de départ susceptibles d’être modifiés avant l’apparition d’une maladie sévère.
Voisins microbiens dans l’intestin et sur la peau
On sait aujourd’hui que l’intestin et la peau abritent des communautés microbiennes complexes qui aident à entraîner le système immunitaire, à façonner le métabolisme et à maintenir les défenses barrières. Mais ces microbes déclenchent-ils réellement la maladie pulmonaire, ou changent-ils simplement lorsque les gens tombent malades ? Pour démêler cause et effet, les chercheurs ont utilisé une méthode appelée randomisation mendélienne, qui exploite les différences génétiques naturelles entre les individus comme une sorte d’« expérience » à long terme. Ils ont combiné des données génétiques sur des centaines d’espèces microbiennes intestinales et cutanées avec des données sur cinq grandes maladies pulmonaires chroniques issues de vastes études européennes, afin de tester si des prédispositions héréditaires à des niveaux plus élevés ou plus faibles de microbes spécifiques sont liées au risque de chaque maladie.
Microbes qui aident ou nuisent aux poumons
L’analyse a identifié des dizaines de microbes intestinaux qui augmentent ou diminuent le risque de chaque maladie respiratoire, souvent selon des profils spécifiques à la maladie. Par exemple, certaines bactéries intestinales semblaient protéger contre la BPCO, l’asthme ou l’HAP, tandis que d’autres augmentaient les chances de MPI ou de BPCO. Les microbes cutanés montraient des liens plus modestes mais néanmoins détectables, certaines espèces étant associées à un risque plus élevé et d’autres à un risque plus faible selon les affections. L’équipe a aussi inversé le sens de l’analyse, constatant que le risque génétique pour la BPCO, l’asthme et d’autres maladies pulmonaires prédisait à son tour des changements du microbiote intestinal et cutané. Ce trafic bidirectionnel suggère une boucle de rétroaction : les microbes peuvent contribuer à façonner la maladie pulmonaire, et la maladie pulmonaire peut remodeler nos écosystèmes microbiens.
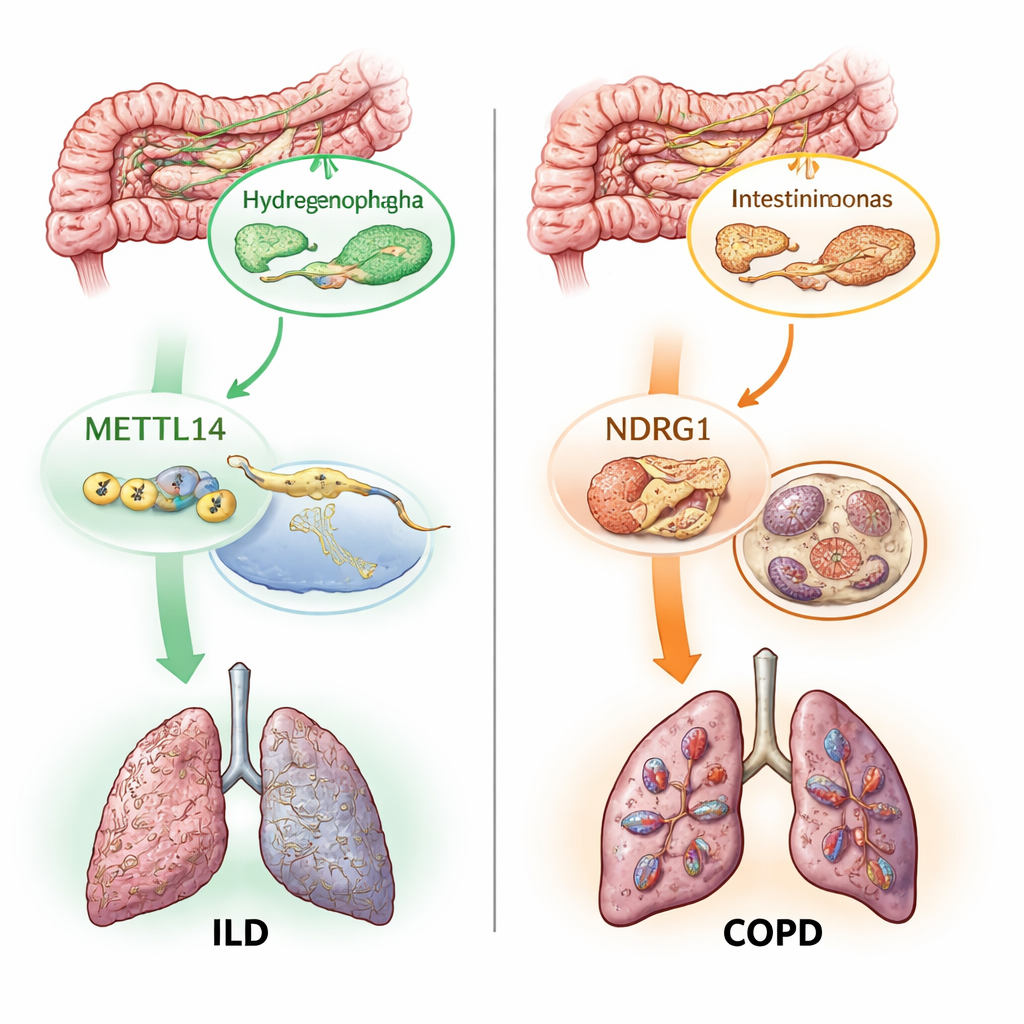
Deux interrupteurs moléculaires : marques d’ARN et mort cellulaire dépendante du fer
Au-delà de la cartographie des microbes importants, les auteurs ont cherché à comprendre comment ces partenaires microscopiques pourraient influencer les tissus pulmonaires. Ils se sont concentrés sur deux processus moléculaires déjà suspectés dans les lésions pulmonaires. Le premier, appelé modification m6A, est une petite étiquette chimique ajoutée à l’ARN qui module l’expression des gènes. Le second, la ferroptose, est une forme de mort cellulaire dépendante du fer, provoquée par une oxydation incontrôlée des lipides membranaires. En utilisant des proxys génétiques pour 19 gènes liés à la m6A et des centaines de gènes liés à la ferroptose, ils ont testé si des altérations de ces voies sont causalement liées aux maladies pulmonaires. Ils ont trouvé qu’un gène « écrivain » de la m6A, METTL14, était associé à un risque réduit de MPI, et que plusieurs gènes de la ferroptose, dont NDRG1, étaient liés à un risque accru de BPCO, MPI et asthme.
Relier les points : des microbes aux cellules jusqu’à la maladie
La partie la plus nouvelle du travail a consisté à retracer comment ces éléments s’insèrent dans des chaînes de cause à effet. Des analyses de médiation statistique ont suggéré qu’une partie de l’effet protecteur de METTL14 sur les MPI passe par des modifications qu’il induit chez un microbe intestinal particulier nommé Hydrogenophaga. Dans une autre voie, une bactérie intestinale spécifique, Intestinimonas massiliensis, semblait influencer le risque de BPCO en activant en partie NDRG1 et le programme de mort par ferroptose. L’équipe a ensuite vérifié des données issues de tissus pulmonaires humains et a confirmé que METTL14 et NDRG1 sont exprimés différemment dans les échantillons malades par rapport aux échantillons sains. Enfin, en utilisant des cartes génétiques unicellulaires des cellules immunitaires, ils ont localisé l’effet délétère de NDRG1 sur la BPCO à un sous-ensemble cellulaire immunitaire, un type de monocyte, ce qui suggère que des médicaments futurs visant ce gène pourraient devoir agir de manière spécifique à certains types cellulaires.
Ce que cela signifie pour les traitements futurs
Pour les non-spécialistes, le message essentiel est que la santé pulmonaire ne dépend pas seulement de ce que nous respirons, mais aussi des microbes qui vivent en nous et sur nous et des interrupteurs moléculaires qu’ils activent à l’intérieur de nos cellules. Cette étude ne prouve pas expérimentalement chaque maillon de la chaîne, et elle est principalement limitée aux personnes d’ascendance européenne, mais elle fournit des indices génétiques solides que les microbes intestinaux, les marques d’ARN comme la m6A et la mort cellulaire induite par le fer forment une voie connectée menant aux lésions pulmonaires chroniques. À long terme, cette ligne de recherche pourrait inspirer de nouvelles stratégies combinant des thérapies basées sur le microbiome et des médicaments ciblant METTL14, NDRG1 ou la ferroptose, visant non seulement à soulager les symptômes mais à interrompre les circuits biologiques qui font progresser les maladies respiratoires chroniques.
Citation: Zhang, J., Liu, X., Liu, X. et al. Host m6A modifications shape microbiota that drives cell specific ferroptosis as a causal pathway to chronic respiratory diseases. Sci Rep 16, 5809 (2026). https://doi.org/10.1038/s41598-026-36513-2
Mots-clés: microbiote intestinal, maladie pulmonaire chronique, asthme et BPCO, épigénétique de l’ARN, voies de mort cellulaire