Clear Sky Science · fr
Association du statut mutationnel de RAS avec les résultats cliniques dans le cancer colorectal métastatique traité par trifluridine/tipiracil ou regorafénib
Pourquoi cette étude compte pour les patients et leurs proches
Le cancer colorectal métastatique — cancer du côlon ou du rectum qui s’est étendu — est une des principales causes de décès par cancer dans le monde. Lorsque les traitements standards cessent d’être efficaces, patients et médecins doivent faire des choix difficiles sur les options suivantes. Cette étude pose une question très concrète : des tests génétiques simples sur la tumeur peuvent‑ils aider à orienter les patients vers deux médicaments largement utilisés en dernier recours, le trifluridine/tipiracil et le regorafénib, afin d’allonger la vie et d’améliorer la qualité de vie ?
Regarder les gènes pour guider des choix thérapeutiques difficiles
Les soins contre le cancer modernes commencent souvent par l’analyse de l’ADN tumoral. Un groupe de gènes clé, appelé RAS, régule la croissance et la division cellulaires. Des altérations, ou mutations, de ces gènes peuvent rendre les cellules cancéreuses prolifératives et résistantes à certains traitements. Les chercheurs ont passé en revue les dossiers médicaux de 263 adultes atteints de cancer colorectal métastatique traités dans un centre oncologique taïwanais entre 2018 et 2023. Tous avaient déjà reçu chimiothérapies et thérapies ciblées standards et ont ensuite été traités soit par trifluridine/tipiracil seul, soit par trifluridine/tipiracil associé à un autre médicament ciblé, soit par regorafénib. Avant le début de ces traitements, chaque patient a eu un test des gènes RAS et a été classé dans l’un des trois groupes : RAS normal (RAS de type sauvage), une mutation fréquente en un point du gène KRAS (KRAS G12), ou d’autres mutations RAS moins fréquentes.
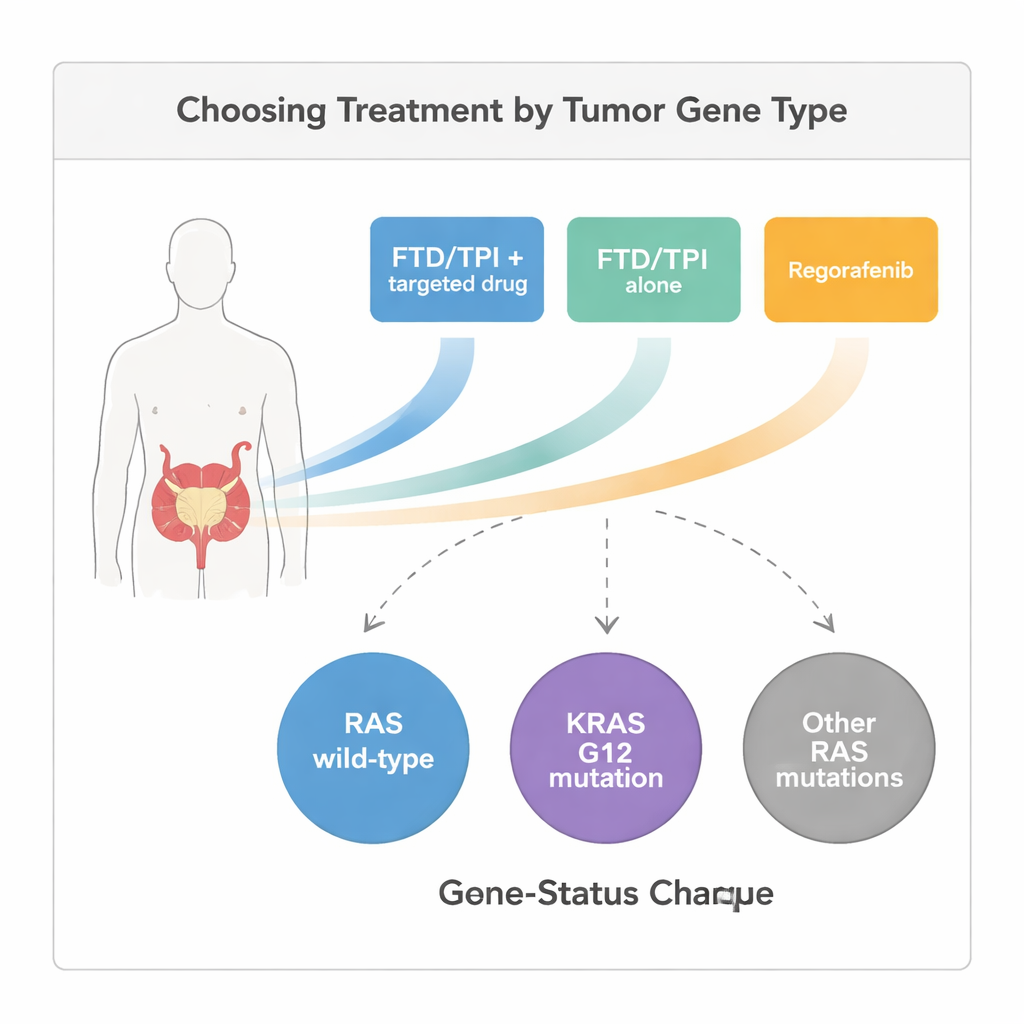
Trois parcours thérapeutiques dans la pratique
Le trifluridine/tipiracil est un comprimé de chimiothérapie, et le regorafénib est un comprimé qui bloque plusieurs voies de signalisation liées à la croissance des cellules cancéreuses et des vaisseaux sanguins. Certains patients de cette étude ont reçu le trifluridine/tipiracil seul, tandis que d’autres l’ont pris en combinaison avec un médicament ciblé supplémentaire qui bloque l’angiogenèse ou des signaux de croissance. Parce qu’il s’agissait d’une étude rétrospective en conditions réelles et non d’un essai randomisé, les médecins ont choisi le traitement en fonction des effets secondaires antérieurs, de la charge tumorale et de l’état général de chaque patient. Les investigateurs ont ensuite suivi la durée pendant laquelle les patients ont vécu sans aggravation de la maladie (survie sans progression) et la survie globale, ainsi que la fréquence de régression ou au moins de stabilisation tumorale.
Les différences génétiques influencent l’efficacité des traitements
Sur l’ensemble du groupe, la combinaison trifluridine/tipiracil plus un médicament ciblé a clairement donné les meilleurs résultats. Les patients sous cette combinaison ont généralement eu environ cinq mois avant l’aggravation de la maladie et une médiane de survie globale légèrement supérieure à 15 mois après le début du traitement — plus longue que celle des patients traités par trifluridine/tipiracil seul ou par regorafénib. Les tumeurs étaient également plus susceptibles de régresser ou de se stabiliser avec la combinaison. En examinant de plus près les groupes RAS, des schémas importants sont apparus. Pour les patients dont les tumeurs avaient un RAS normal ou l’une des mutations RAS plus rares, le trifluridine/tipiracil seul surpassait encore le regorafénib en termes de survie. En revanche, pour les patients dont les tumeurs portaient la mutation fréquente KRAS G12, le regorafénib offrait une meilleure survie que le trifluridine/tipiracil seul, bien que la combinaison reste l’option la plus efficace de toutes.
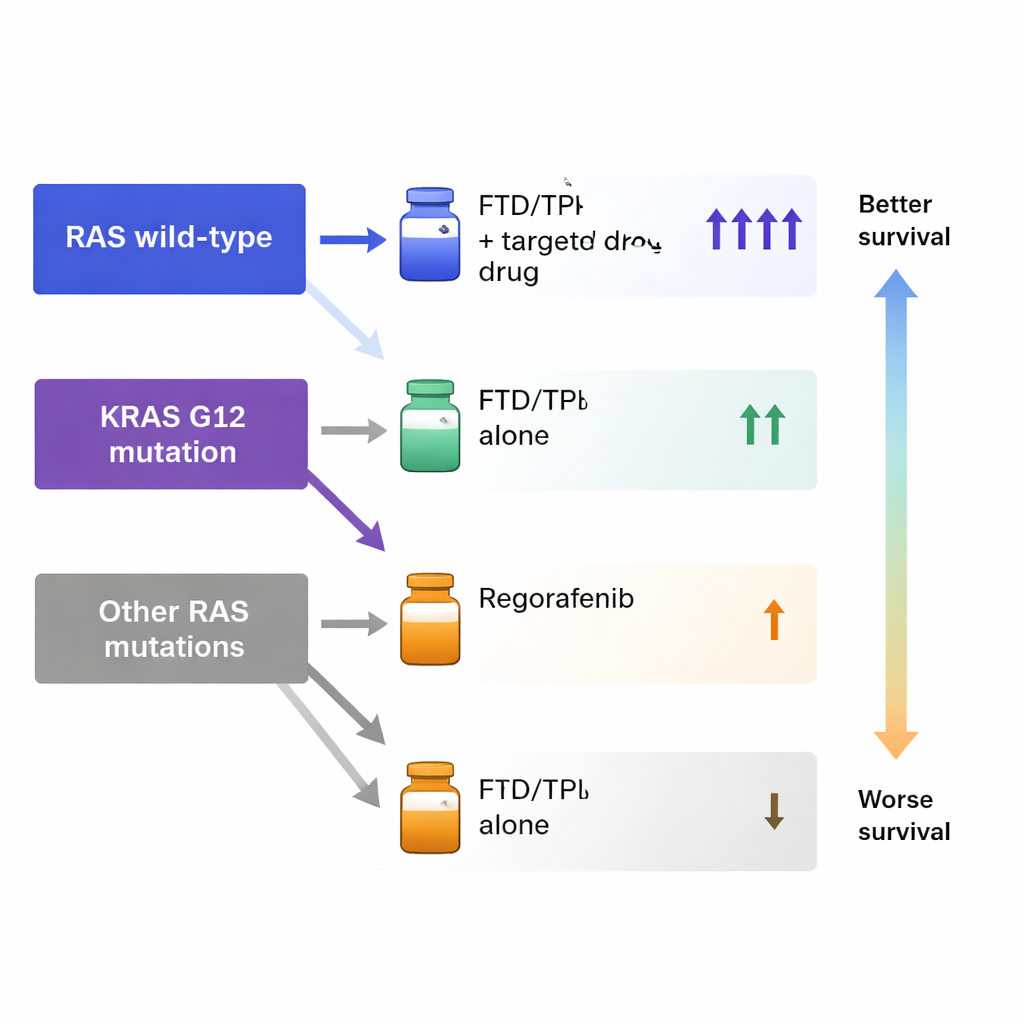
Ce que cela signifie pour la médecine de précision
Ces résultats suggèrent qu’un test génétique relativement simple — déjà réalisé de façon routinière pour de nombreux patients atteints de cancer colorectal — pourrait aider à choisir entre deux options thérapeutiques difficiles en phase avancée. Plutôt que de considérer le trifluridine/tipiracil et le regorafénib comme interchangeables après l’échec des traitements standards, les médecins pourraient privilégier le trifluridine/tipiracil, en particulier en association avec un médicament ciblé, pour la majorité des patients. Pour le sous‑groupe porteur de la mutation KRAS G12, le regorafénib pourrait être la meilleure option en monothérapie si la thérapie combinée n’est pas possible. L’étude suggère aussi que d’autres caractéristiques cliniques, comme le stade initial du cancer et certains marqueurs de réparation de l’ADN, pourraient affiner encore ces décisions.
Message à retenir pour les non‑spécialistes
Pour les personnes vivant avec un cancer colorectal avancé, cette recherche apporte une nouvelle prudente mais encourageante : l’empreinte génétique d’une tumeur, en particulier les altérations des gènes RAS, peut aider à orienter vers le traitement le plus susceptible de gagner du temps. Dans cette étude, l’ajout d’un médicament ciblé au trifluridine/tipiracil a donné la survie la plus longue pour presque tous les patients, quel que soit leur statut RAS. Parmi ceux porteurs d’une mutation spécifique KRAS G12, le regorafénib semblait être un choix préférable au trifluridine/tipiracil en monothérapie. Étant donné qu’il s’agit d’une analyse rétrospective monocentrique, ces résultats doivent être confirmés par des essais randomisés plus vastes. Néanmoins, l’étude propose une feuille de route pragmatique basée sur les gènes que les médecins peuvent considérer dès aujourd’hui pour individualiser le traitement de dernier recours du cancer colorectal métastatique.
Citation: Hsieh, MC., Rau, KM., Liu, KW. et al. Association of RAS mutational status with clinical outcomes in metastatic colorectal cancer treated with trifluridine/tipiracil or regorafenib. Sci Rep 16, 5294 (2026). https://doi.org/10.1038/s41598-026-36509-y
Mots-clés: cancer colorectal métastatique, mutation RAS, KRAS G12, trifluridine tipiracil, regorafénib