Clear Sky Science · fr
La phosphorylation de la cortactine par NEK7 module la capacité migratoire des cellules exprimant EML4-ALK V3
Pourquoi le mouvement cellulaire importe en cas de cancer du poumon
Le cancer devient menaçant lorsque les cellules apprennent à se déplacer. Dans le cancer du poumon non à petites cellules, certaines tumeurs se disséminent plus rapidement que d’autres, et un coupable est une protéine de fusion défaillante appelée EML4-ALK. Une version particulière, connue sous le nom de variant 3 (V3), est associée à une maladie particulièrement agressive et à de mauvaises réponses aux thérapies ciblées. Cette étude pose une question simple mais essentielle : qu’est-ce qui permet à ces cellules cancéreuses pilotées par V3 de modifier leur forme et de se déplacer si efficacement, et peut-on identifier les éléments moléculaires qui rendent cela possible ?
Un variant pulmonaire hyper-migratoire
Les cliniciens savent depuis longtemps qu’une minorité des cancers du poumon porte la fusion EML4-ALK, mais les patients dont les tumeurs expriment la forme V3 ont tendance à évoluer défavorablement par rapport à ceux portant d’autres variants. Au microscope, les cellules exprimant V3 ont une apparence distincte : au lieu d’être compactes et en forme de pavé, elles s’allongent en formes fines et étirées avec des prolongements étendus, ressemblant à des cellules en mouvement. Des travaux antérieurs ont montré que ce comportement dépend de deux enzymes, NEK9 et NEK7, qui agissent comme des interrupteurs moléculaires dans la cellule. Cependant, les cibles en aval cruciales de ces interrupteurs — celles qui remodelent directement le squelette interne de la cellule — restaient mal comprises.
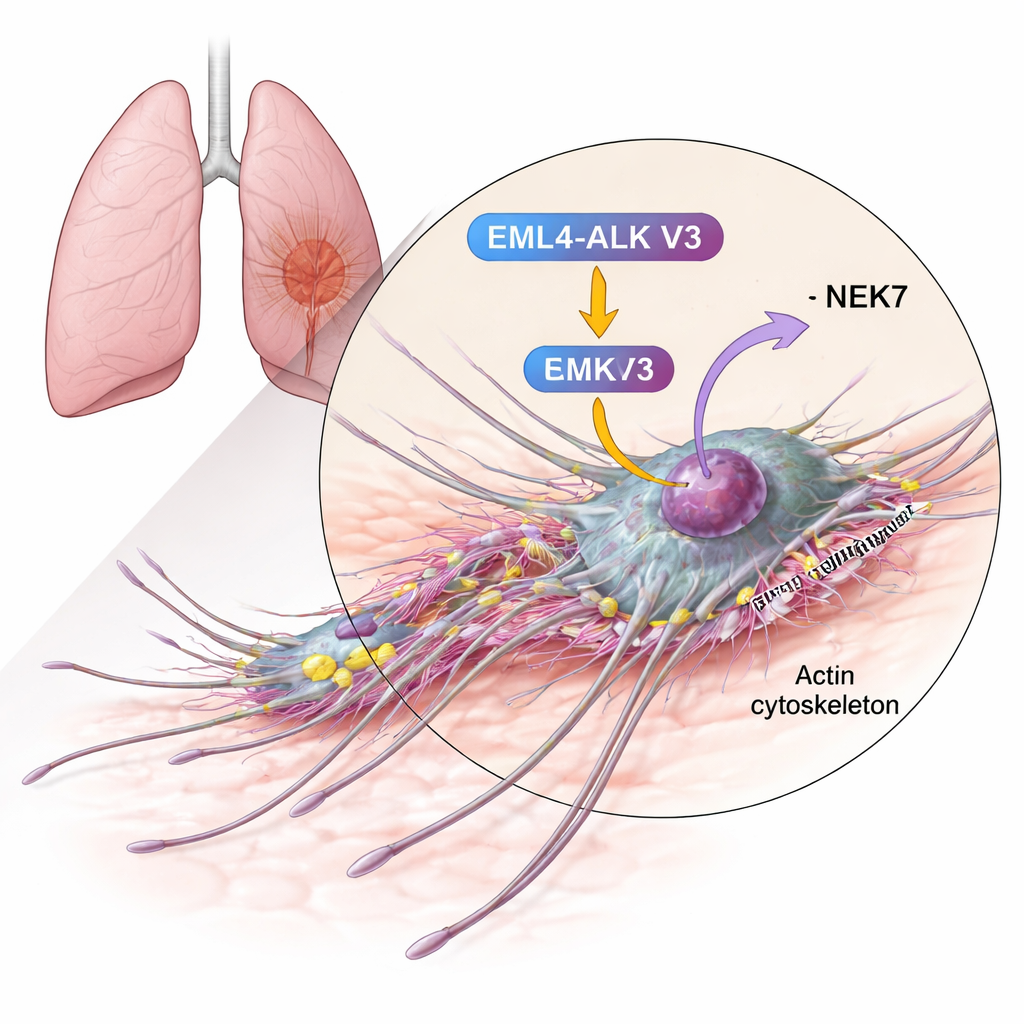
Relier une protéine de mouvement à une fusion agressive
Les auteurs se sont focalisés sur la cortactine, une protéine déjà connue pour être abondante dans de nombreux cancers invasifs et pour aider à construire les réseaux de filaments d’actine qui poussent la membrane cellulaire vers l’avant. Grâce à des tests biochimiques, ils ont montré que la cortactine peut être modifiée chimiquement (phosphorylée) par NEK6 et, de façon encore plus marquée, par NEK7. Les enzymes ajoutent des groupes phosphate à des résidus sérine spécifiques dans la région de la cortactine qui lie l’actine — précisément l’étendue qui saisit les fibres d’actine et stabilise les réseaux branchés. En présence de NEK7, la cortactine était plus fortement phosphorylée et en davantage de sites que sous l’action de NEK6, ce qui suggère que NEK7 est le régulateur principal dans ce contexte.
Inhiber la cortactine stoppe la migration des cellules cancéreuses
Pour comprendre le rôle effectif de la cortactine dans des cellules vivantes, les chercheurs l’ont diminuée via l’interférence ARN dans des cellules conçues pour activer NEK9 ou NEK7, ou pour exprimer EML4-ALK V3. Dans ces trois contextes, les formes allongées remarquables de type mésenchymateux s’effondrèrent : les cellules devinrent plus plates et rondes, perdirent leurs longs prolongements et formèrent à la place des « fibres de stress » épaisses et droites d’actine traversant la cellule. Plusieurs essais de migration — de la fermeture de « plaies » artificielles dans une couche cellulaire au suivi de cellules individuelles et à la mesure du déplacement vers un signal chimique — montrèrent que sans cortactine, ces cellules hautement mobiles ralentissaient considérablement. Des effets similaires furent observés dans des lignées cellulaires de cancer du poumon établies portant naturellement EML4-ALK V3, soulignant la pertinence clinique de la voie.
Fins filaments et pointes aiguës en bord d’attaque
Des images à haute résolution dans des cellules épithéliales bronchiques ont révélé un tableau encore plus détaillé. Les cellules exprimant EML4-ALK V3 produisaient de nombreuses extensions fines, parfois branchées et semblables à des filopodes, hérissant leurs protrusions. Aux extrémités et aux points de branchement de ces structures, la cortactine, EML4-ALK V3, NEK7 et une forme phosphorylée de la cortactine se rassemblaient. Cette co-localisation serrée suggère un « chantier » focalisé où NEK7 modifie la cortactine pour construire et maintenir les réseaux d’actine délicats et branchés qui aident à diriger la cellule. Lorsque la cortactine était supprimée, ces extensions complexes disparaissaient et la croissance invasive depuis des sphéroïdes tumoraux 3D vers le gel environnant était fortement diminuée.
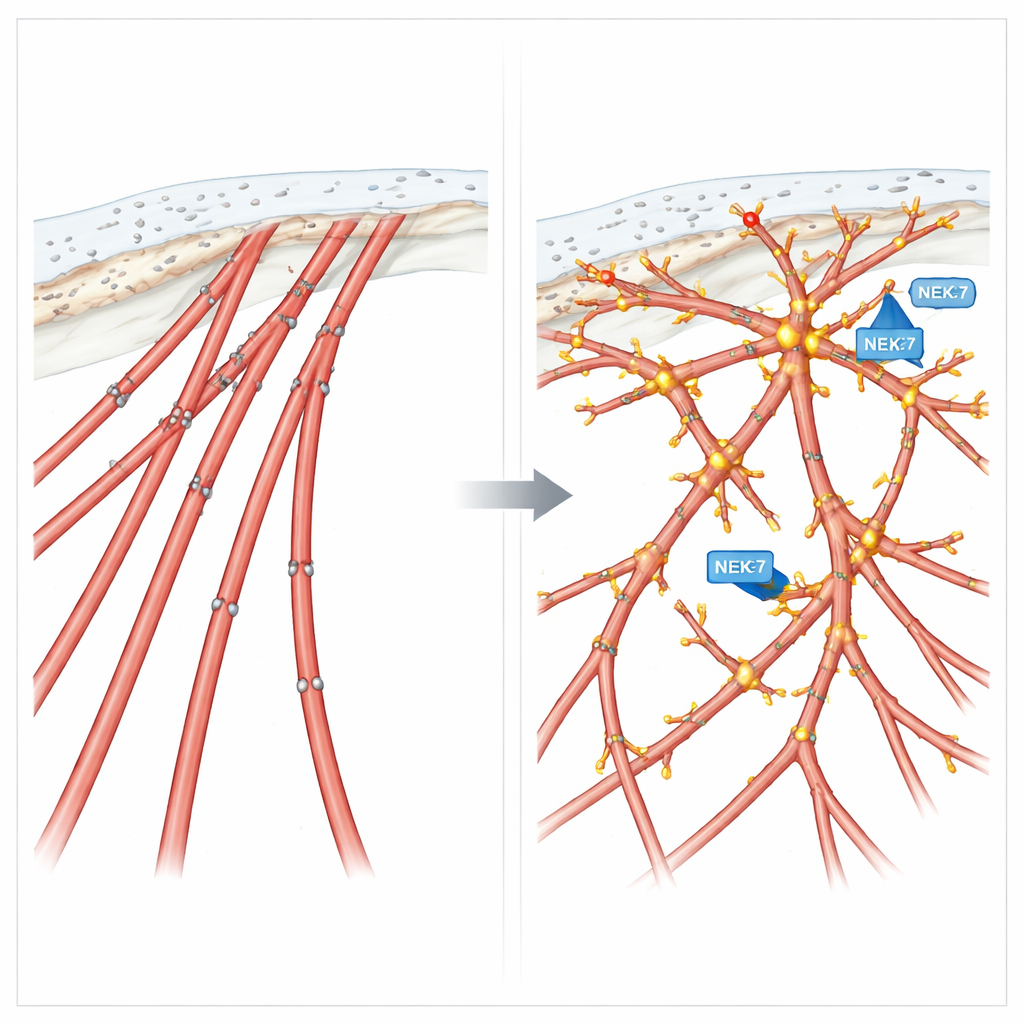
La phosphorylation comme un réglage de migration
Pour tester comment ces marques chimiques sur la cortactine influent sur le comportement, l’équipe a créé deux versions conçues de la protéine : une forme phospho-mimétique qui imite une phosphorylation constante à quatre sites clés, et une forme non phosphorylable qui ne peut pas être phosphorylée à ces positions. Les cellules exprimant la version mimétique développèrent de nombreux prolongements de type filopode et montrèrent une migration directionnelle renforcée, similaire aux cellules avec NEK7 actif ou EML4-ALK V3. En revanche, les cellules exprimant la version non phosphorylable formèrent des fibres de stress rigides, perdirent ces fines extensions et se déplacèrent de façon rapide mais sans direction — bonnes pour errer, mauvaises pour suivre un signal. En culture tridimensionnelle, cette cortactine phospho-nulle induisit des excroissances invasives désorganisées plutôt que finement guidées.
Ce que cela signifie pour comprendre — et cibler — la dissémination
En bref, l’étude montre que le variant agressif EML4-ALK V3 du cancer du poumon détourne un système normal de modelage cellulaire. En activant NEK7, il provoque la phosphorylation de la cortactine sur des sites spécifiques de sa région de liaison à l’actine. Cette modification règle la cortactine pour qu’elle puisse bâtir des structures d’actine finement branchées et des prolongements de type filopode qui soutiennent une migration et une invasion cellulaires rapides et dirigées. Perturber la cortactine ou sa phosphorylation inverse le système : les cellules bougent à peine ou se déplacent de manière chaotique sans direction. Ces conclusions révèlent une chaîne moléculaire concrète — depuis une fusion oncogénique, via NEK7, jusqu’à la cortactine et le cytosquelette d’actine — qui aide à expliquer pourquoi certains cancers du poumon métastasent si efficacement, et indiquent de nouvelles voies pour ralentir ou détourner leur mouvement.
Citation: Richardson, E.L., Knebel, A., Straatman, K.R. et al. NEK7 phosphorylation of cortactin modulates the migratory capacity of cells expressing EML4-ALK V3. Sci Rep 16, 6407 (2026). https://doi.org/10.1038/s41598-026-36484-4
Mots-clés: cancer du poumon non à petites cellules, EML4-ALK V3, migration cellulaire, cortactine, cytosquelette d’actine