Clear Sky Science · fr
ATF4 régule la dysfonction mitochondriale et la mitophagie, contribuant à l’apoptose de l’endothélium cornéen
Pourquoi la fenêtre de l’œil peut devenir trouble
Nos cornées — les fenêtres claires à l’avant des yeux — restent transparentes grâce à une fine couche de cellules laborieuses située sur leur surface interne. Dans la dystrophie endothéliale de Fuchs (FECD), des millions de personnes perdent lentement ces cellules, entraînant un gonflement, une vision trouble et souvent des greffes de cornée. Cette étude pose une question fondamentale mais cruciale : qu’est‑ce qui pousse ces cellules à déclencher leur mort, et couper un seul « interrupteur » moléculaire pourrait‑il permettre de les sauver ?
Une couche cellulaire fragile qui maintient la vision claire
L’endothélium cornéen est une nappe unique de cellules hexagonales qui pompe en permanence le liquide hors de la cornée pour la garder transparente. Dans la FECD, ces cellules subissent un stress et disparaissent progressivement, tandis que des excroissances de matériel anormal, appelées guttas, s’accumulent sur la membrane sous‑jacente. En l’absence de médicaments approuvés pour la FECD et avec la greffe de cornée comme traitement principal, les chercheurs cherchent à comprendre précisément comment le stress intracellulaire pousse ces cellules vers la mort. Des travaux antérieurs ont mis en évidence séparément une tension dans deux compartiments cellulaires clés — le réticulum endoplasmique (l’usine de pliage des protéines) et les mitochondries (les centrales énergétiques de la cellule) — mais la manière dont ces deux réponses au stress communiquent restait floue.
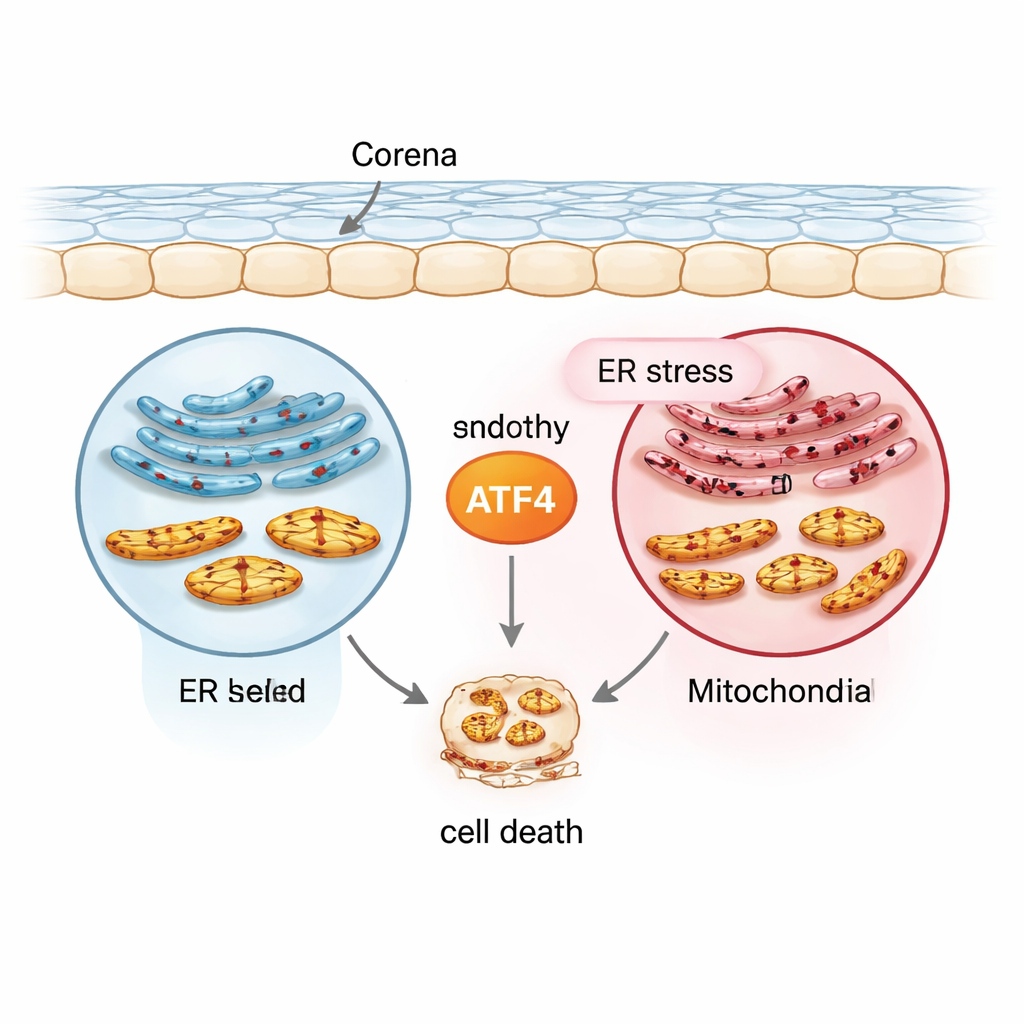
Le messager du stress au centre : ATF4
L’équipe s’est concentrée sur une protéine nommée ATF4, un facteur de transcription qui active ou réprime de nombreux gènes de réponse au stress. En utilisant une lignée cellulaire endothéliale cornéenne humaine normale (21T), une lignée de type FECD portant l’expansion répétée liée à la maladie du gène TCF4 (F35T), des cellules endothéliales cornéennes humaines primaires et des modèles murins exposés aux ultraviolets A (UVA), ils ont créé une gamme de conditions mimant le stress chronique. Ils ont induit le stress du réticulum endoplasmique avec un médicament appelé tunicamycine puis mesuré ATF4 et d’autres marqueurs. Par rapport aux cellules normales, les cellules de type FECD présentaient déjà des niveaux plus élevés d’ATF4 et de protéines de stress associées, et ATF4 augmentait encore davantage sous stress chronique, tant dans les cultures cellulaires que dans les tissus cornéens humains. Ce schéma place ATF4 au carrefour entre des réponses protectrices précoces et des signaux autodétruisants tardifs.
De la panne d’énergie à la mort programmée
Ensuite, les chercheurs ont examiné comment ce stress affectait les mitochondries. Dans les cellules de type FECD, les mitochondries produisaient moins d’ATP, perdaient leur potentiel de membrane électrique et se fragmentaient, passant de longues structures en réseau à de nombreux petits fragments. Ces altérations s’aggravaient lorsque le stress du réticulum endoplasmique se prolongeait. Parallèlement, des protéines classiques de la mort cellulaire — comme des caspases activées et la protéine de réparation de l’ADN PARP sous sa forme clivée pro‑mort — devenaient plus abondantes, tandis que des protéines protectrices comme Bcl‑2 diminuaient. Ensemble, ces changements indiquent que les cellules de l’endothélium cornéen stressées dans la FECD sont poussées vers une apoptose d’origine mitochondriale, une forme ordonnée mais irréversible de suicide cellulaire programmé.
Le système de nettoyage cale sous stress chronique
Normalement, les mitochondries fortement endommagées sont éliminées par un processus de recyclage appelé mitophagie, au cours duquel elles sont marquées et enfermées dans de petites vésicules pour être éliminées. L’équipe a constaté que les molécules « initiatrices » précoces de la mitophagie (Parkin et LC3) étaient activées tant dans les cellules normales que dans les cellules de type FECD, en particulier après le stress. Mais des protéines de soutien clés étaient réduites, et la microscopie électronique montrait une accumulation de mitochondries partiellement digérées piégées dans des vésicules. Cela suggère que, bien que le processus de nettoyage démarre, il échoue à se terminer, laissant les cellules encombrées de centrales énergétiques défectueuses qui alimentent davantage le stress et la mort plutôt que la récupération.
Désactiver ATF4 pour sauver les cellules
Pour tester si ATF4 entraînait cette spirale, les chercheurs ont utilisé de petits ARN interférents pour silencier partiellement ATF4 dans des cellules endothéliales cornéennes en culture. Sous le même stress chronique, les cellules avec ATF4 réduit présentaient des niveaux plus faibles de protéines pro‑mort, un potentiel de membrane mitochondriale plus sain, moins de fragmentation et une meilleure survie aux tests de viabilité. De manière importante, le nombre de structures de mitophagie bloquées avait diminué, suggérant que l’abaissement d’ATF4 aidait à rétablir un meilleur équilibre entre dommage et nettoyage. Chez des souris génétiquement modifiées pour ne posséder qu’un exemplaire fonctionnel du gène ATF4, l’exposition aux UVA provoquait moins d’activation d’une protéine partenaire pro‑mort, CHOP, et préservait davantage de cellules endothéliales de forme normale comparé aux souris pleinement pourvues en ATF4.
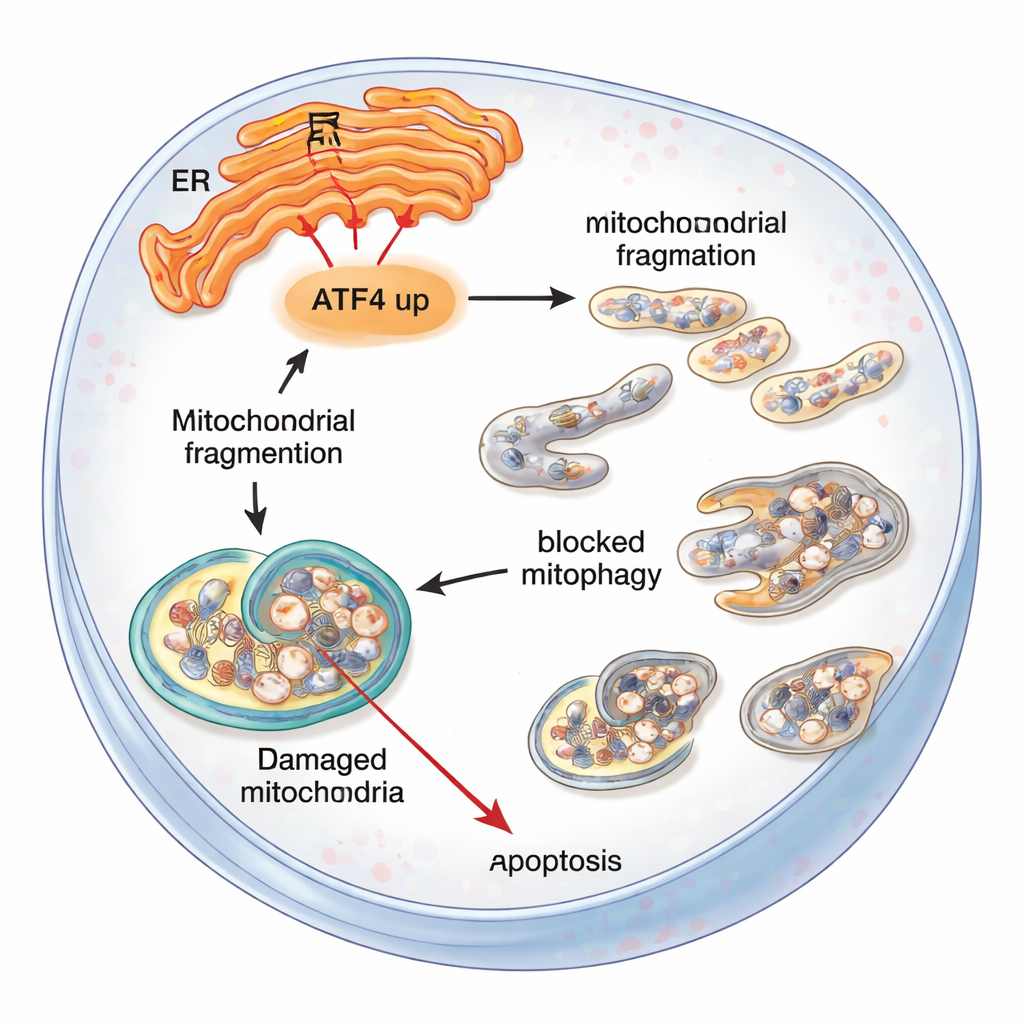
Ce que cela signifie pour les personnes atteintes de FECD
Pour un public non spécialiste, le message est qu’un messager du stress, ATF4, peut faire basculer les cellules endothéliales cornéennes de l’adaptation à l’effondrement. Lorsque le stress du réticulum endoplasmique est prolongé, ATF4 contribue à perturber les mitochondries, bloque la machinerie de nettoyage de la cellule et, en fin de compte, encourage ces cellules vitales à s’autodétruire. Diminuer ATF4 — soit génétiquement chez la souris, soit avec des outils moléculaires ciblés en culture — protège les mitochondries, améliore l’élimination des déchets et permet de conserver davantage de cellules vivantes. Bien que ces travaux soient encore au stade des études en laboratoire et sur modèles animaux, ils mettent en lumière ATF4 et les voies de stress associées comme des cibles médicamenteuses prometteuses susceptibles, un jour, de ralentir ou prévenir la progression de la dystrophie de Fuchs et de réduire le besoin de greffes de cornée.
Citation: Qureshi, S., Kim, S.Y., Lee, S. et al. ATF4 regulates mitochondrial dysfunction and mitophagy, contributing to corneal endothelial apoptosis. Sci Rep 16, 5960 (2026). https://doi.org/10.1038/s41598-026-36453-x
Mots-clés: Dystrophie endothéliale de Fuchs, endothélium cornéen, stress mitochondrial, mitophagie, ATF4