Clear Sky Science · fr
Une approche intégrative pour identifier de nouveaux réseaux d’interactions miRNA-mRNA dans la cardiomyopathie liée à LMNA
Pourquoi ces petits régulateurs cardiaques sont importants
La cardiomyopathie dilatée est une affection grave dans laquelle le cœur s’élargit et s’affaiblit, conduisant souvent à une insuffisance cardiaque, à des rythmes cardiaques dangereux et parfois à une mort subite. Pour de nombreuses familles, cette maladie est héréditaire, et des altérations d’un gène appelé LMNA sont fréquemment en cause. Cette étude pose une question apparemment simple mais aux conséquences considérables : dans les cœurs endommagés par des mutations de LMNA, quels gènes sont activés ou réprimés, et quels petits ARN tirent ces interrupteurs ? En cartographiant ces dialogues moléculaires en détail, le travail ouvre des pistes pour mieux prédire, surveiller et peut‑être un jour traiter cette forme agressive de maladie cardiaque.
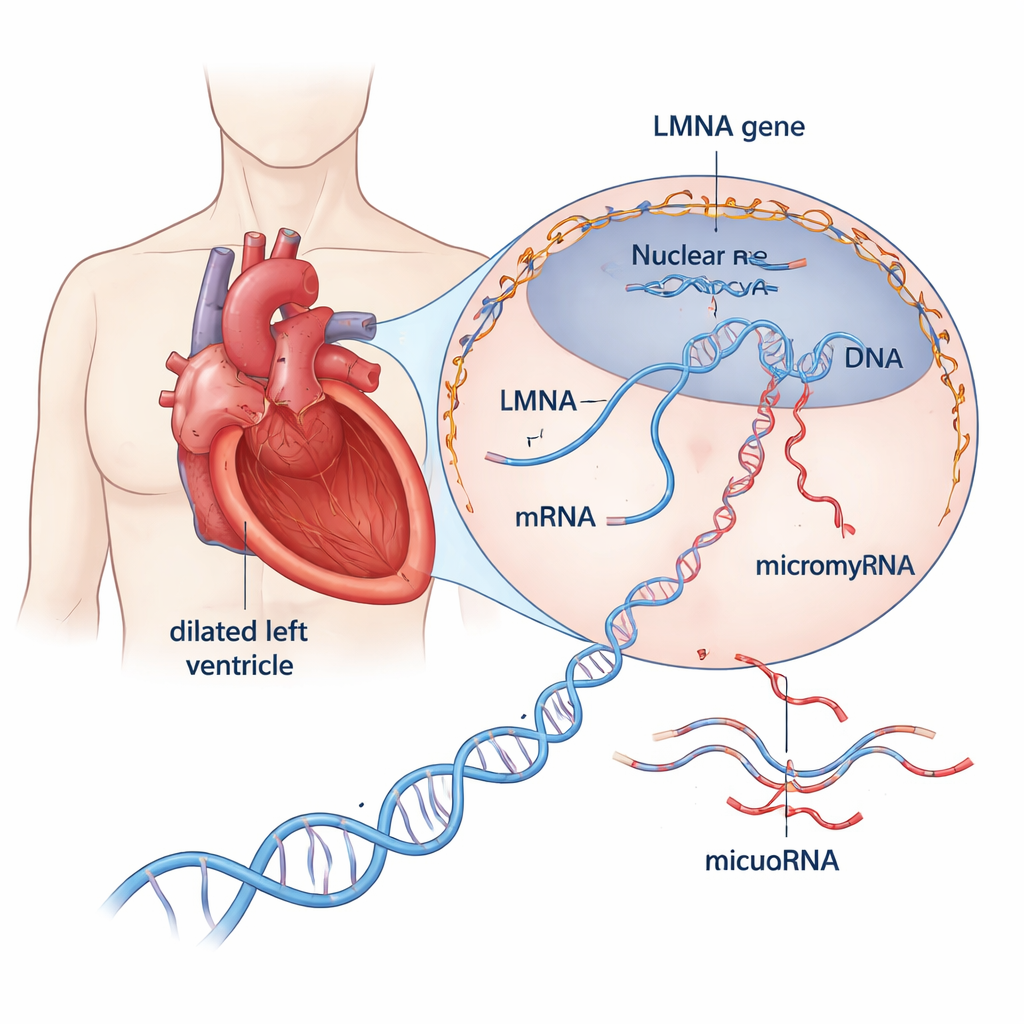
Un examen approfondi d’une maladie cardiaque dangereuse
La cardiomyopathie dilatée étire et amincit la principale chambre de pompage du cœur, affaiblissant sa capacité à propulser le sang dans le corps. Environ un tiers à la moitié des cas autrefois qualifiés d’« idiopathiques » s’avèrent désormais d’origine génétique. Parmi les plus de 30 gènes impliqués, LMNA se distingue : des variantes délétères de ce gène représentent environ 10 % des cas héréditaires et sont associées à une progression rapide de la maladie, à des troubles du rythme précoce et à un risque élevé de mort cardiaque subite. LMNA code pour des protéines structurelles qui forment un échafaudage autour de l’ADN de la cellule, aidant à maintenir la forme du noyau et influençant l’activité des gènes. Pourtant, la façon dont des protéines LMNA défectueuses poussent le cœur vers l’insuffisance reste mal comprise.
Suivre les messages à l’intérieur des cœurs de souris
Pour explorer cela, les chercheurs ont utilisé un modèle murin portant une mutation LMNA bien caractérisée (R249W) qui développe une forme de cardiomyopathie dilatée similaire à la maladie humaine. À 50 semaines d’âge — moment où les souris présentent des ventricules dilatés, une fonction de pompage réduite et des foyers de fibrose — l’équipe a extrait le tissu cardiaque et examiné deux types d’ARN : l’ARN messager (ARNm), qui porte les instructions pour fabriquer des protéines, et les microARN (miARN), de courts brins non codants qui ajustent finement l’activité des gènes en bloquant ou en dégradant des ARNm spécifiques. Grâce au séquençage à haut débit et à des filtres statistiques rigoureux, ils ont identifié 2 148 gènes dont l’activité changeait dans les cœurs mutants et 53 miARNs augmentés ou diminués par rapport aux souris saines.
Ce qui change à l’intérieur des cellules cardiaques malades
Lorsque les chercheurs ont regroupé les gènes altérés en voies biologiques, plusieurs thèmes sont apparus. Beaucoup des gènes modifiés étaient liés à la contraction des cellules musculaires cardiaques, à leur adhérence entre elles et à la matrice de soutien environnante, à la conduction des signaux électriques dans le cœur, et au métabolisme des lipides pour produire de l’énergie. Ces résultats concordent avec le tableau clinique de la maladie liée à LMNA : tissu raide et fibreux ; conduction électrique perturbée favorisant les arythmies ; et déséquilibre énergétique. Des analyses de voies en s’appuyant sur des bases de données établies ont confirmé un enrichissement dans le remodelage de la matrice extracellulaire, les canaux ioniques voltages‑dépendants, la communication de type synaptique dans le cœur et le métabolisme des acides gras — suggérant que la mutation LMNA perturbe plusieurs systèmes interconnectés plutôt qu’une seule étape défaillante.
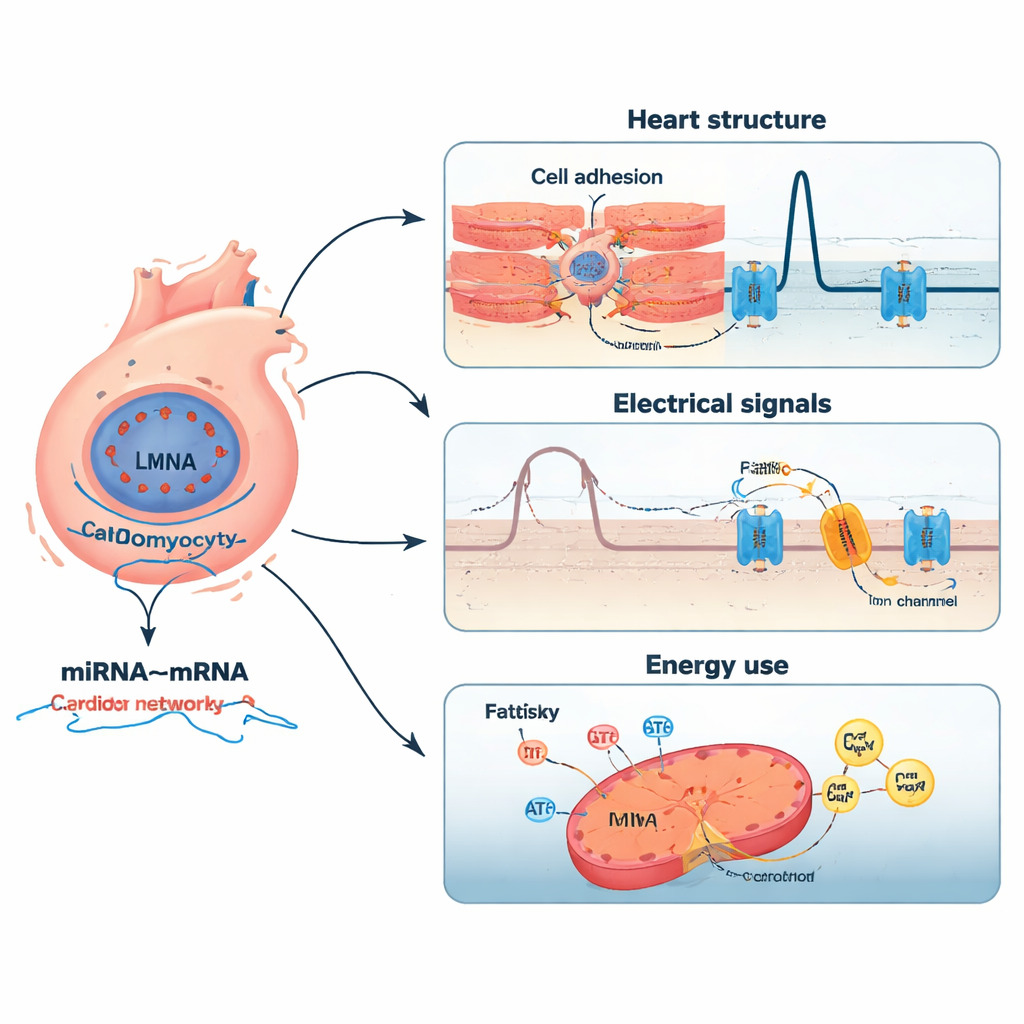
Réseaux de petits interrupteurs et leurs cibles
L’étude est allée plus loin en associant les miARNs à leurs cibles ARNm probables. Grâce à des analyses de corrélation et à une vérification croisée avec de larges bases de données d’interactions validées expérimentalement, les auteurs ont assemblé un réseau de haute confiance de 2 197 paires miARN–ARNm impliquant 12 miARNs clés. Certains miARNs étaient plus actifs et semblaient réduire l’expression de gènes essentiels au développement cardiaque, à la gestion du calcium et aux réponses au stress oxydatif. D’autres étaient moins actifs, pouvant lever des freins sur des gènes impliqués dans l’adhésion cellulaire, l’inflammation et le remodelage de l’échafaudage structurel du cœur. Par exemple, un miARN (miR‑183‑5p) a été relié à un récepteur de la voie Wnt, qui influence la communication cellule‑à‑cellule, tandis qu’un autre (miR‑3473a) se connectait à un canal de libération du calcium central pour le rythme cardiaque. Ensemble, ces réseaux montrent comment des variations subtiles de ces petits régulateurs ARN peuvent amplifier l’impact d’une mutation LMNA.
Des cartes moléculaires aux thérapies futures
Pour les non‑spécialistes, la conclusion est que cette étude propose une carte détaillée de la manière dont une mutation LMNA reconfigure le câblage interne du cœur au niveau du contrôle génique. Plutôt qu’un « mauvais gène » isolé, la maladie reflète une cascade de messages altérés — beaucoup orchestrés par des miARNs — qui affectent la structure cardiaque, la stabilité électrique et l’utilisation de l’énergie. Bien que le travail ait été réalisé chez la souris et repose largement sur des analyses computationnelles, il met en lumière des paires miARN–gène spécifiques comme candidats prometteurs pour de futurs biomarqueurs sanguins ou des thérapies ciblées. À long terme, moduler ces petits interrupteurs ARN pourrait aider les médecins à mieux prédire qui est le plus à risque, à surveiller la progression de la maladie avec plus de précision et à concevoir des traitements plus personnalisés pour les familles touchées par la cardiomyopathie liée à LMNA.
Citation: Córdoba-Caballero, J., Martínez, F.B., Campuzano, O. et al. An integrative approach to identify novel miRNA-mRNA interaction networks in LMNA-cardiomyopathy. Sci Rep 16, 6110 (2026). https://doi.org/10.1038/s41598-026-36439-9
Mots-clés: cardiomyopathie dilatée, gène LMNA, microARN, régulation génique, insuffisance cardiaque