Clear Sky Science · fr
La réalité virtuelle médiée par une interface cerveau-ordinateur améliore la neuromodulation sensori-motrice chez des personnes indemnes et après une lésion médullaire
Remarcher, du moins dans l’esprit
Pour les personnes vivant avec une paralysie après une lésion de la moelle épinière, l’idée de remarcher ou de reprendre le vélo peut sembler hors de portée. Cette étude explore une forme différente de récupération : réentraîner directement le cerveau à l’aide de la réalité virtuelle et d’une interface cerveau-ordinateur. En demandant à des volontaires et à des personnes atteintes de lésions médullaires d’imaginer le mouvement de leurs jambes pendant qu’ils traversent une forêt virtuelle luxuriante, les chercheurs montrent que le cerveau peut apprendre à émettre des signaux de mouvement plus nets — même lorsque le corps ne peut pas bouger.
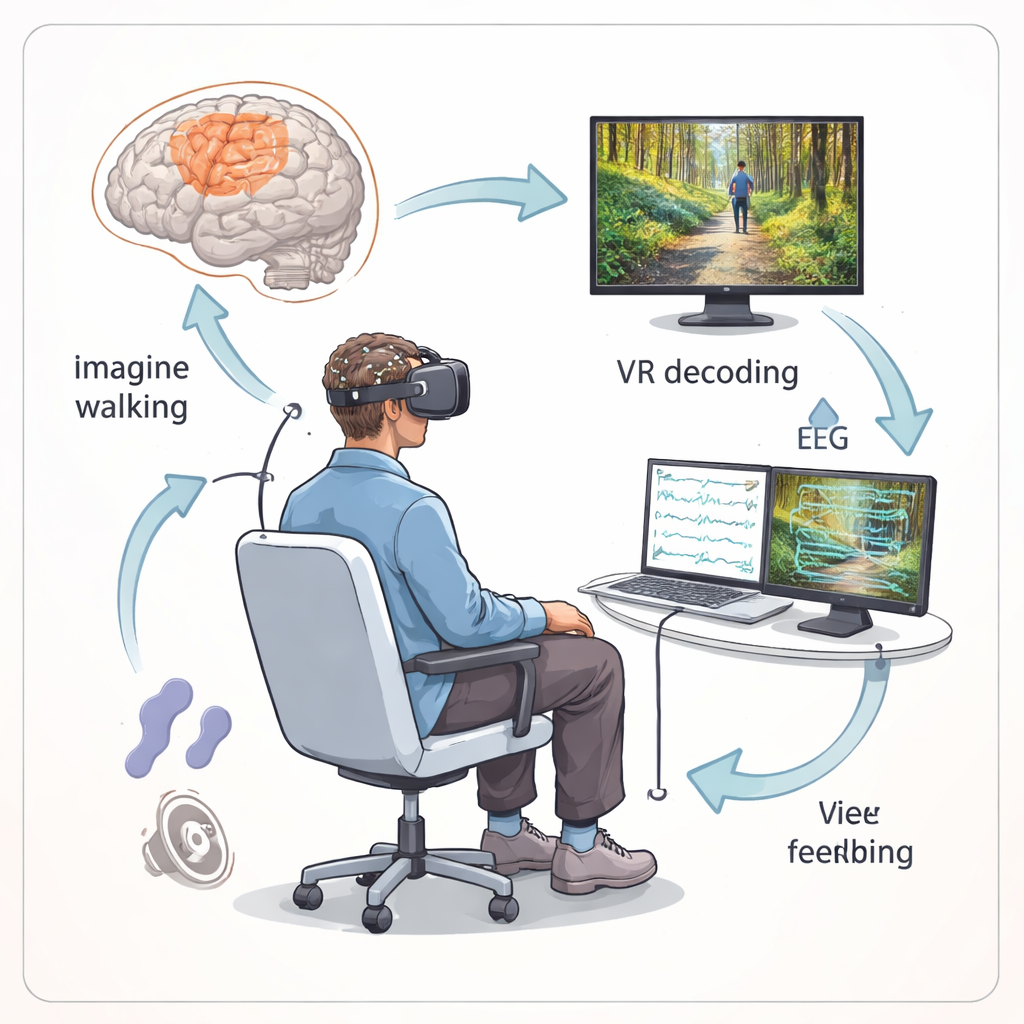
Un pont numérique entre le cerveau et le monde virtuel
L’équipe de recherche a construit un système qui relie l’activité cérébrale à un monde virtuel. Les participants portaient une casquette munie de capteurs EEG à sec qui captaient de faibles signaux électriques à la surface du cuir chevelu, ainsi qu’un casque de réalité virtuelle affichant un sentier forestier. Les volontaires indemnes voyaient un avatar marchant en vue à la première personne, comme s’ils regardaient à travers leurs propres yeux, tandis que les personnes présentant une lésion médullaire complète se voyaient pédaler le long du même sentier. Lorsque les participants se détendaient, l’avatar restait immobile. Lorsqu’ils imaginaient de manière vivide marcher ou pédaler, un ordinateur décodait leurs signaux cérébraux et faisait avancer l’avatar en temps réel, déclenchant également des sons et, pour le groupe de personnes blessées, une stimulation musculaire douce délivrée par des impulsions électriques aux jambes.
Entraîner le cerveau comme un muscle
Apprendre à contrôler cette interface cerveau-ordinateur n’a pas été instantané ; cela a demandé de la pratique, un peu comme apprendre un sport ou un instrument de musique. Les volontaires indemnes ont réalisé 15 séances d’entraînement réparties sur différents jours, chacune durant environ une heure. Chaque séance commençait par une période d’étalonnage pendant laquelle le système « écoutait » le cerveau alors que la personne alternait entre détente et imagination de la marche. L’ordinateur construisait ensuite un modèle neuf capable de distinguer ces deux états. Après l’étalonnage, les participants enchaînaient des runs plus longs où ils suivaient des indices audio pour se détendre ou imaginer marcher continuellement pendant une minute complète, l’avancement de l’avatar reflétant l’activité cérébrale décodée. Dans une phase distincte de contrôle libre, ils essayaient de faire prendre à l’avatar autant de pas auto-initiés que possible en cinq minutes, sans indices externes.
Des signaux cérébraux plus clairs et un meilleur contrôle
Avec le temps, le cerveau des participants a produit des motifs plus fiables lorsqu’ils imaginaient bouger par rapport à l’état de repos. Les chercheurs ont mesuré la distinctivité et la stabilité de ces motifs au moyen d’outils mathématiques indépendants de tout algorithme de décodage particulier. Au fil des séances, ces mesures se sont améliorées, montrant que les participants apprenaient réellement à modeler leur activité cérébrale. Cet apprentissage s’est traduit par un meilleur contrôle : chez les individus indemnes, la précision de l’ordinateur pour distinguer « marcher » de « se détendre » est passée d’environ 60 % lors des premières séances à environ 80 % lors des dernières. Pendant les essais en contrôle libre, le nombre de pas correctement décodés a plus que doublé. Les personnes présentant des lésions médullaires anciennes, complètes sur le plan moteur et sensoriel — qui ne peuvent ni bouger ni sentir leurs jambes — ont également montré des gains significatifs. Leur précision de classification est passée d’environ la tranche haute des 50 % à plus de 70 % à mesure qu’ils apprenaient à produire des signaux cérébraux « pédaler versus détente » plus clairs tout en recevant à la fois un retour VR et une stimulation musculaire des jambes.
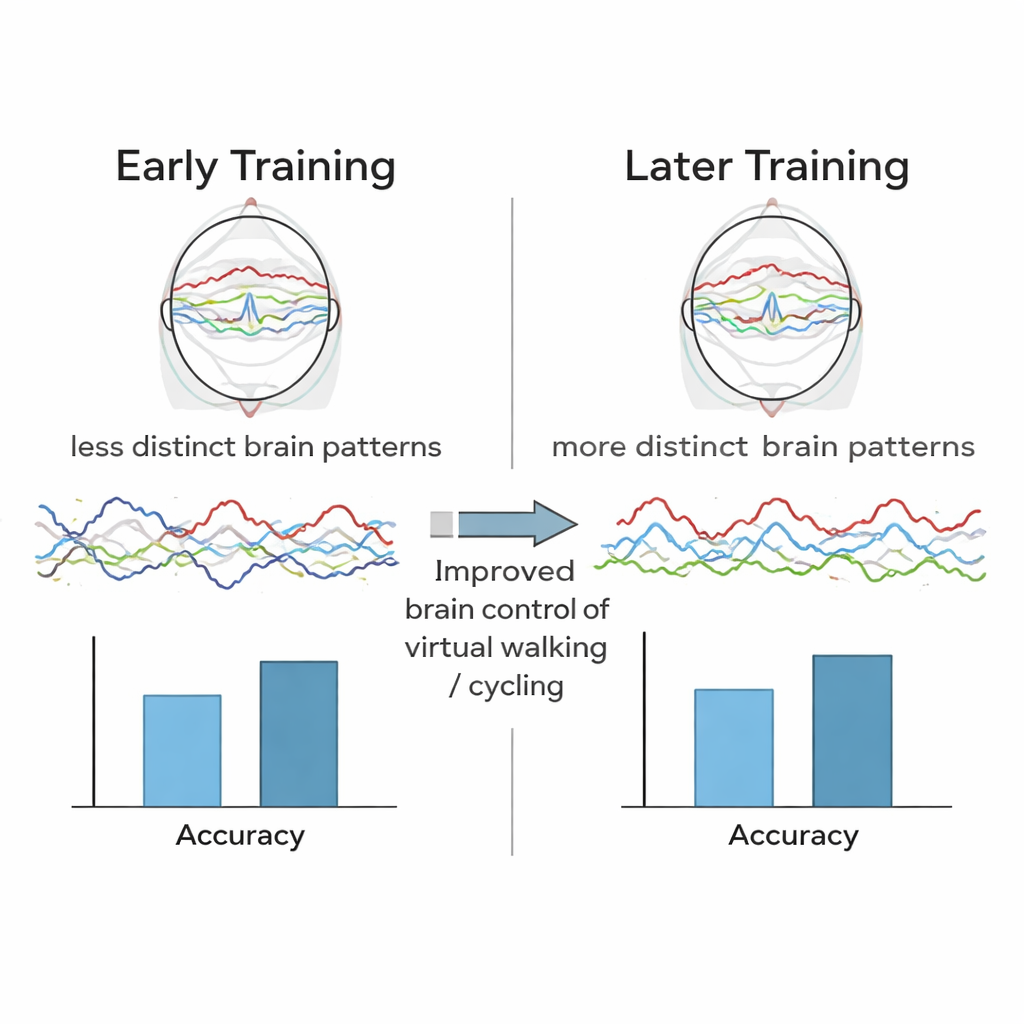
Pourquoi la réalité virtuelle compte
Le cadre immersif de la VR semble jouer un rôle important. Le simple fait d’observer un corps réaliste se mouvoir en synchronie avec ses actions imaginées peut activer les réseaux cérébraux impliqués dans le mouvement et la conscience corporelle. L’environnement forestier, la vue à la première personne et les sons subtils rendent l’expérience plus engageante que de fixer de simples symboles à l’écran. Pour les participants atteints de lésions médullaires, l’ajout d’une stimulation électrique qui déplaçait réellement leurs jambes, liée à leurs commandes cérébrales, a probablement renforcé le lien entre intention et rétroaction. Bien que l’étude n’ait pas inclus de groupe témoin sans VR, les résultats suggèrent que la combinaison d’un retour sensoriel riche, d’un cadre ludique et d’un entraînement répété aide le cerveau à affiner son « plan » interne du mouvement.
Pas vers une rééducation future
Pour un non-spécialiste, le message principal est que le cerveau reste adaptable, même des années après une blessure dévastatrice. En pratiquant la marche ou le pédalage imaginés dans un monde virtuel qui répond instantanément à leurs pensées, les personnes indemnes comme celles avec une lésion médullaire complète ont appris à émettre des signaux de mouvement plus précis qu’un ordinateur pouvait interpréter. Ce travail ne restaure pas à lui seul la marche dans le monde réel. Mais il renforce les circuits cérébraux sous-jacents au mouvement et montre que des casques à électrodes sèches peu coûteux et la VR grand public peuvent soutenir un entraînement à long terme. À l’avenir, des systèmes similaires pourraient être couplés à des exosquelettes robotiques ou à des stimulations électriques avancées pour aider à traduire ces signaux cérébraux améliorés en mouvements fonctionnels réels en dehors de la réalité virtuelle.
Citation: Mannan, M.M.N., Palipana, D.B., Mulholland, K. et al. Virtual reality mediated brain-computer interface training improves sensorimotor neuromodulation in unimpaired and post spinal cord injury individuals. Sci Rep 16, 6215 (2026). https://doi.org/10.1038/s41598-026-36431-3
Mots-clés: rééducation en réalité virtuelle, interface cerveau-ordinateur, entraînement par imagerie motrice, lésion de la moelle épinière, neuroplasticité