Clear Sky Science · fr
Activité antitumorale de QAL333 et modélisation prédictive : analyse intégrée transcriptomique-bioinformatique révélant une cytotoxicité sélective et des déterminants de sensibilité
Pourquoi ce nouveau candidat-médicament est important
Les médicaments contre le cancer sont souvent efficaces chez certains patients mais inefficaces chez d’autres, principalement parce que les tumeurs diffèrent dans leur architecture interne. Cette étude présente un composé nouvellement conçu, QAL333, qui semble frapper certaines formes de cancer colorectal beaucoup plus fortement que d’autres tout en épargnant de nombreuses cellules normales. Autre point important, les chercheurs montrent comment des profils d’activité génique des cellules tumorales pourraient aider à prédire qui bénéficiera le plus, ouvrant la voie à des stratégies de traitement plus précises et personnalisées.
Une frappe ciblée sur des types tumoraux spécifiques
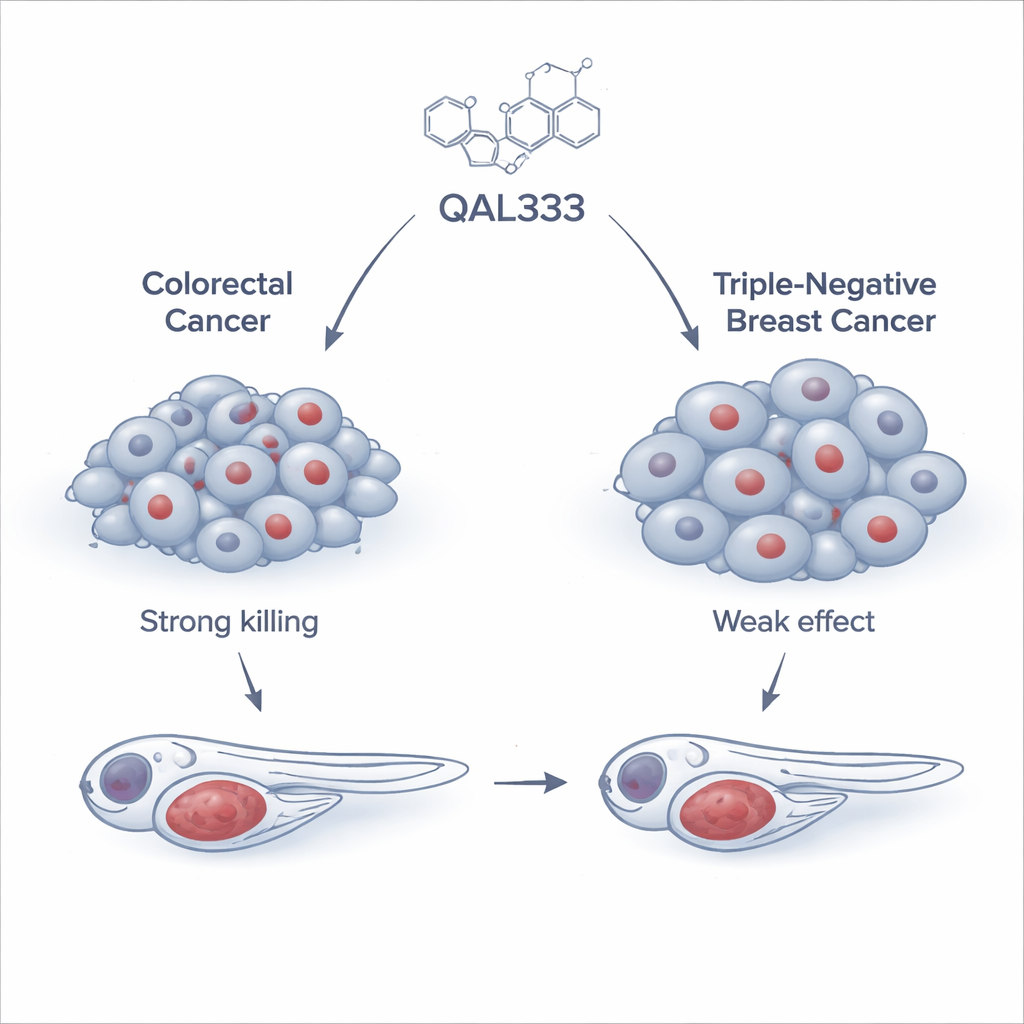
L’équipe a commencé par tester QAL333, une molécule synthétique apparentée à une famille de composés déjà connue pour endommager les cellules cancéreuses, sur un large panel de 15 lignées cellulaires humaines cancéreuses et trois lignées non cancéreuses. Ils ont observé que les cellules du cancer colorectal, en particulier une lignée appelée SW620, étaient très sensibles, le médicament les tuant à des doses relativement faibles. En revanche, les cellules de cancer du sein triple négatif étaient bien plus résistantes et nécessitaient des doses plus de dix fois supérieures, difficiles à atteindre en toute sécurité. Fait intéressant, toutes les cellules non cancéreuses ne réagissaient pas de la même façon : certaines étaient sensibles, tandis que d’autres, comme une lignée rénale couramment utilisée, étaient étonnamment résistantes. Ce schéma montre que les effets de QAL333 dépendent davantage de la biologie interne d’une cellule que de son étiquette « cancer » ou « normale ».
Tester le médicament in vivo
Pour vérifier si les résultats prometteurs en culture cellulaire se maintenaient dans un organisme vivant, les chercheurs se sont tournés vers le poisson-zèbre, un petit poisson transparent couramment utilisé comme modèle de maladie humaine. Ils ont implanté des cellules cancéreuses humaines marquées par fluorescence dans des embryons de poisson-zèbre et les ont traités avec QAL333. Chez les poissons portant des cellules de cancer colorectal, le médicament a clairement ralenti la croissance tumorale, approchant l’effet d’une combinaison chimio-standard utilisée en clinique. En revanche, les tumeurs formées par les cellules de cancer du sein triple négatif ont à peine répondu, bien qu’un médicament courant contre le cancer du sein, le paclitaxel, ait bien fonctionné dans le même modèle. Ces essais in vivo confirment que la force de QAL333 réside dans un sous-ensemble de tumeurs plutôt que dans l’ensemble des cancers.
Examiner l’intérieur des cellules pour comprendre le mode d’action de QAL333
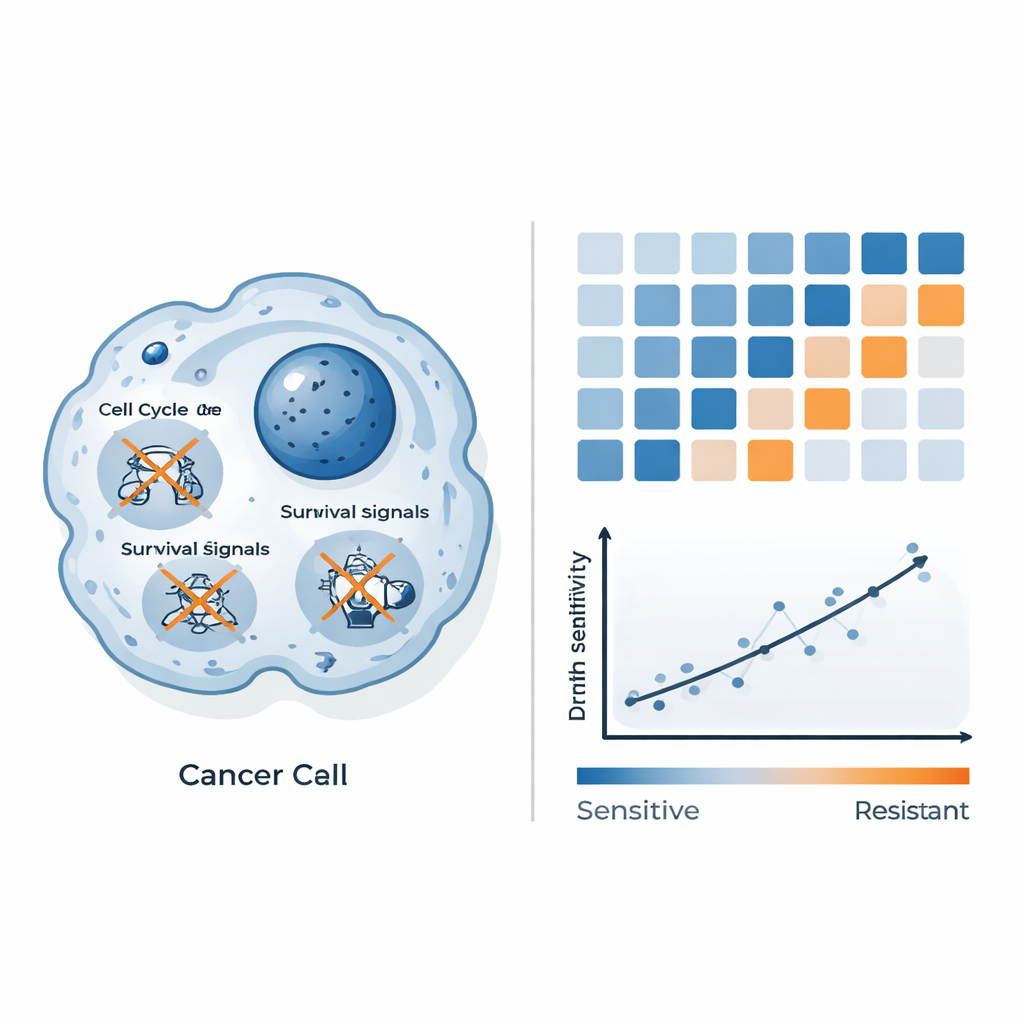
Pour comprendre pourquoi certaines cellules meurent et d’autres résistent, les scientifiques ont mesuré comment des milliers de gènes modifiaient leur niveau d’activité après un traitement par QAL333. Dans les cellules de cancer colorectal sensibles, des gènes clés qui pilotent le cycle de division et la croissance cellulaire étaient réprimés, et les principales voies de survie étaient atténuées. Des signaux liés au stress oxydatif et à une forme de mort cellulaire distincte de l’apoptose classique ont également été modifiés, suggérant que QAL333 surcharge des systèmes déjà fragiles chargés de gérer les dommages dans ces cellules. Les cellules de cancer du sein résistantes, en revanche, ont activé des programmes de stress et d’inflammation contrôlés par des facteurs comme NF-κB, connus pour aider les cellules à faire face à des conditions nocives. Cette comparaison côte à côte dessine le portrait d’un QAL333 qui submerge des défenses faibles dans certaines cellules tandis que d’autres montent une contre-réponse efficace.
Utiliser des profils géniques pour prédire la réponse
Au-delà du simple inventaire des changements d’expression, les chercheurs se sont demandé si ces profils pouvaient être transformés en un outil prédictif pratique. Ils ont combiné les données d’expression génique de base du panel de lignées cellulaires avec leur sensibilité mesurée au médicament et utilisé l’apprentissage automatique pour rechercher les signaux les plus informatifs. Plutôt que de s’appuyer sur des gènes isolés, ils ont regroupé les gènes en voies biologiques et créé un « score de voie » composite construit à partir de trois systèmes : le métabolisme et le traitement énergétique, l’organisation de l’environnement cellulaire (protéoglycanes et structures apparentées dans le cancer) et l’agencement du cytosquelette. Ce score composite corrélait fortement avec la quantité de QAL333 nécessaire pour tuer chaque lignée : des scores plus faibles s’alignaient sur une sensibilité élevée, et des scores plus élevés sur la résistance. Autrement dit, la configuration de ces réseaux à l’intérieur d’une tumeur peut prédire l’efficacité de QAL333.
Indices inattendus d’effets biologiques plus larges
Alors que l’objectif principal était le cancer, QAL333 a aussi montré la capacité de perturber la « quorum sensing », un système de communication que les bactéries utilisent pour coordonner des comportements comme la formation de biofilms. À des doses infimes, le composé a réduit la formation de biofilm par une bactérie responsable de maladies des gencives et a atténué certains signaux inflammatoires dans des cellules immunitaires. Les auteurs considèrent ces résultats comme exploratoires et préliminaires, mais ils suggèrent que QAL333 ou des molécules apparentées pourraient un jour avoir des usages au-delà de la thérapie anticancéreuse, par exemple dans des infections où les communautés bactériennes sont difficiles à éradiquer.
Ce que cela pourrait signifier pour les patients futurs
Globalement, l’étude présente QAL333 comme un candidat-médicament sélectif qui frappe les tumeurs colorectales vulnérables tout en épargnant de nombreux autres types cellulaires, et l’associe à une feuille de route pour prédire quelles tumeurs sont les plus susceptibles de répondre. Si cela se confirme dans des modèles animaux plus avancés puis chez l’humain, un test simple d’expression génique pourrait aider les médecins à décider quand QAL333 est approprié, s’inscrivant dans l’objectif plus large d’adapter le traitement du cancer à l’architecture moléculaire de chaque tumeur. Dans le même temps, le travail souligne que même les médicaments prometteurs ont des limites : les cancers du sein et d’autres tumeurs résistantes pourront nécessiter des combinaisons astucieuses ou des stratégies entièrement différentes.
Citation: Kim, H.H., Im, S., Kim, J. et al. QAL333’s antitumor activity and predictive modeling: integrated transcriptomic-bioinformatic analysis reveals selective cytotoxicity and sensitivity determinants. Sci Rep 16, 5648 (2026). https://doi.org/10.1038/s41598-026-36430-4
Mots-clés: cancer colorectal, thérapie ciblée, expression génique, modélisation de la sensibilité aux médicaments, xénogreffe sur poisson-zèbre