Clear Sky Science · fr
De la modélisation QSAR in silico au test MTT in vitro : validation expérimentale de nouvelles pistes uPAR pour le cancer du sein triple négatif (TNBC) et le cancer de la peau
Pourquoi cette recherche importe
Des cancers tels que le cancer du sein triple‑négatif et certains cancers cutanés sont notoirement difficiles à traiter parce qu’ils se propagent rapidement et résistent souvent aux thérapies standard. Cette étude explore une nouvelle cible prometteuse à la surface des cellules cancéreuses — appelée uPAR — et montre comment la combinaison de la conception de médicaments assistée par ordinateur et d’expérimentations en laboratoire peut révéler de nouveaux candidats-médicaments susceptibles de ralentir ou d’empêcher la propagation de ces tumeurs agressives.
Une porte qui aide la propagation du cancer
Pour qu’une tumeur devienne mortelle, ses cellules doivent se détacher de leur site d’origine, dégrader les tissus environnants, pénétrer dans la circulation sanguine et coloniser des organes distants. uPAR est un acteur clé de ce processus. Il est présent à la surface des cellules cancéreuses et coopère avec des protéines partenaires pour activer des enzymes qui dissolvent la matrice de soutien environnante, facilitant ainsi la migration et l’invasion des cellules. uPAR est particulièrement surexprimé dans les cellules de cancer du sein triple‑négatif et dans certains cancers de la peau, et son abondance est corrélée à une croissance plus rapide, une invasivité accrue et des résultats cliniques plus défavorables. Pour ces raisons, uPAR constitue une cible attrayante — mais jusqu’à présent sous‑exploitable — pour des médicaments anticancéreux.
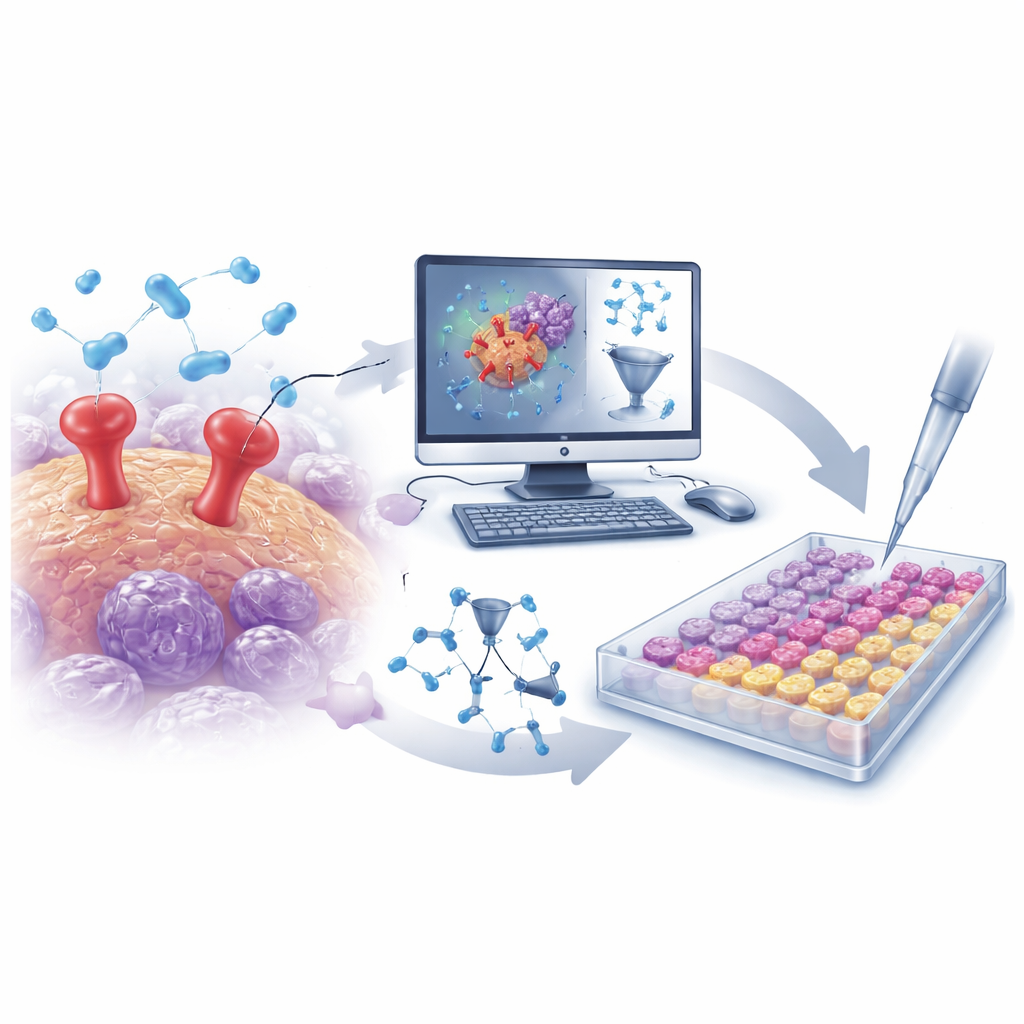
Exploiter de grandes données chimiques avec des algorithmes intelligents
Les chercheurs ont commencé par rassembler une grande collection de plus de 500 molécules connues pour bloquer uPAR à partir d’une base de données publique. La structure de chaque molécule a été traduite en milliers de descripteurs numériques capturant des caractéristiques telles que la taille, la forme, la répartition des charges et la flexibilité. À partir de ces données, l’équipe a construit un modèle QSAR (relation quantitative structure‑activité) — un outil mathématique qui apprend quelles caractéristiques structurales tendent à rendre une molécule un inhibiteur de uPAR plus efficace. Après une validation rigoureuse pour éviter le surapprentissage, le modèle a montré une forte capacité prédictive sur des composés non vus précédemment, mettant en évidence plusieurs caractéristiques clés qui renforcent ou affaiblissent le blocage de uPAR. Ces connaissances ont guidé la recherche de nouvelles molécules mieux conçues.
Des cribles virtuels aux éprouvettes réelles
Équipée du modèle QSAR entraîné, l’équipe a procédé à un criblage virtuel d’une bibliothèque ciblée d’environ 30 000 molécules dirigées contre des protéases. Le modèle a rapidement réduit cet ensemble vaste à un petit groupe de candidats probables inhibiteurs de uPAR. En parallèle, des simulations d’amarrage (docking) ont évalué l’aptitude de chaque candidat à s’insérer dans le site de liaison de uPAR, et des simulations de dynamique moléculaire ont testé si ces complexes amarrés resteraient stables au fil du temps. De cette campagne in silico combinée sont ressorties deux molécules remarquables : D685‑0061, identifiée par le modèle QSAR comme très puissante, et C878‑1660, mise en avant par les simulations d’amarrage et de dynamique pour former des interactions particulièrement stables avec uPAR.
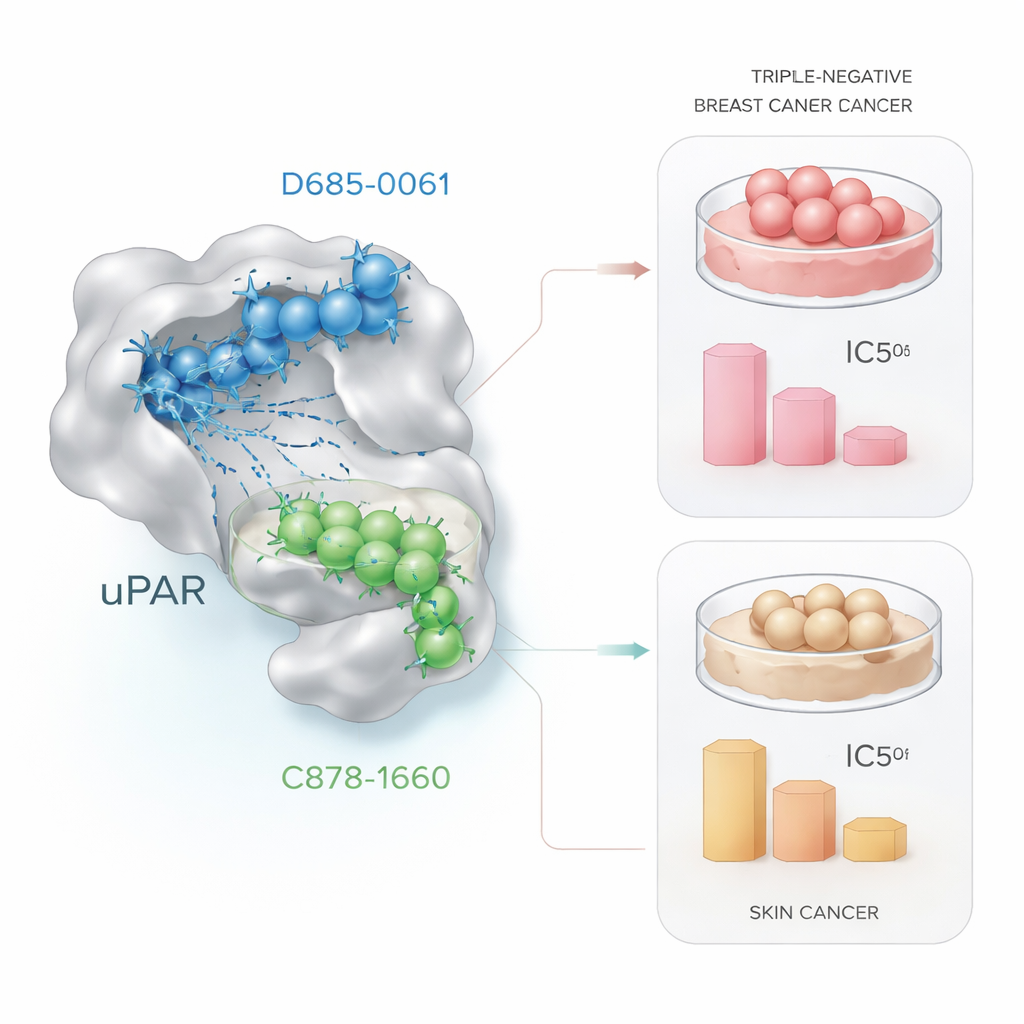
Mettre les candidats à l’épreuve dans des cellules cancéreuses
La promesse informatique n’est pertinente que si elle se traduit en effets biologiques réels. Pour tester cela, les chercheurs ont exposé des cellules cancéreuses vivantes à des doses croissantes des deux molécules candidates et ont mesuré la survie cellulaire à l’aide d’une méthode standard de laboratoire appelée test MTT. Dans les cellules de cancer du sein triple‑négatif (MDA‑MB‑231), D685‑0061 a éliminé les cellules plus efficacement, réduisant la viabilité de moitié à environ 21 micromoles, tandis que C878‑1660 nécessitait environ quatre fois cette concentration. Au microscope, les cellules traitées par D685‑0061 présentaient des signes nets d’apoptose, tels que le arrondissement, le détachement de la surface et la fragmentation. En revanche, dans les cellules de cancer de la peau (A431), C878‑1660 était le tueur le plus efficace, atteignant 50 % de mortalité cellulaire à environ 19 micromoles contre ≈28 micromoles pour D685‑0061, avec des dommages dépendant de la dose visibles au microscope.
Ce que cela signifie pour les traitements futurs du cancer
Ce travail ne livre pas immédiatement un nouveau médicament, mais il fournit deux points de départ prometteurs et, tout aussi important, une feuille de route puissante pour en trouver d’autres. En combinant modélisation sur de grandes bases de données, simulations 3D et expérimentations cellulaires rigoureuses, l’étude montre que uPAR peut être ciblé de manière sélective par de petites molécules qui endommagent des cellules agressives de cancers du sein et de la peau. D685‑0061 et C878‑1660 servent désormais de composés leaders que les chimistes peuvent optimiser pour augmenter la puissance, améliorer la sécurité et affiner leur distribution dans l’organisme. À plus long terme, des médicaments développés selon cette approche pourraient aider à bloquer la dissémination des cancers pilotés par uPAR, transformant certains des tumeurs les plus dangereuses d’aujourd’hui en maladies plus gérables.
Citation: Badukle, H., Jawarkar, R.D., Shah, U. et al. From in-silico QSAR modeling to in-vitro MTT assay: experimental validation of novel uPAR leads for triple-negative breast cancer (TNBC) and skin cancer. Sci Rep 16, 5786 (2026). https://doi.org/10.1038/s41598-026-36406-4
Mots-clés: inhibiteurs de uPAR, cancer du sein triple négatif, cancer de la peau, conception de médicaments assistée par ordinateur, test de viabilité cellulaire MTT