Clear Sky Science · fr
Étude en théorie de la fonctionnelle de la densité de l’adsorption du cyclophosphamide et du purinethol sur un cadre triazine covalent (CTF-2) pour des applications d’administration de médicaments
Pourquoi une chimiothérapie plus intelligente compte
Les médicaments de chimiothérapie sauvent des vies, mais ils agissent souvent comme un projecteur plutôt que comme un faisceau ciblé — attaquant les cellules saines en même temps que les cellules cancéreuses. Cela peut entraîner des effets secondaires graves, allant de la fatigue et des infections à des lésions d’organes. L’étude présentée ici explore un matériau ultrafin et très poreux appelé cadre triazine covalent (CTF-2) comme une « éponge intelligente » capable de transporter deux médicaments anticancéreux d’usage ancien — le cyclophosphamide et le purinethol — de façon plus sûre et plus efficace vers leur cible, puis de les relâcher dans des conditions proches de celles d’une tumeur.
Un nouveau type d’éponge moléculaire
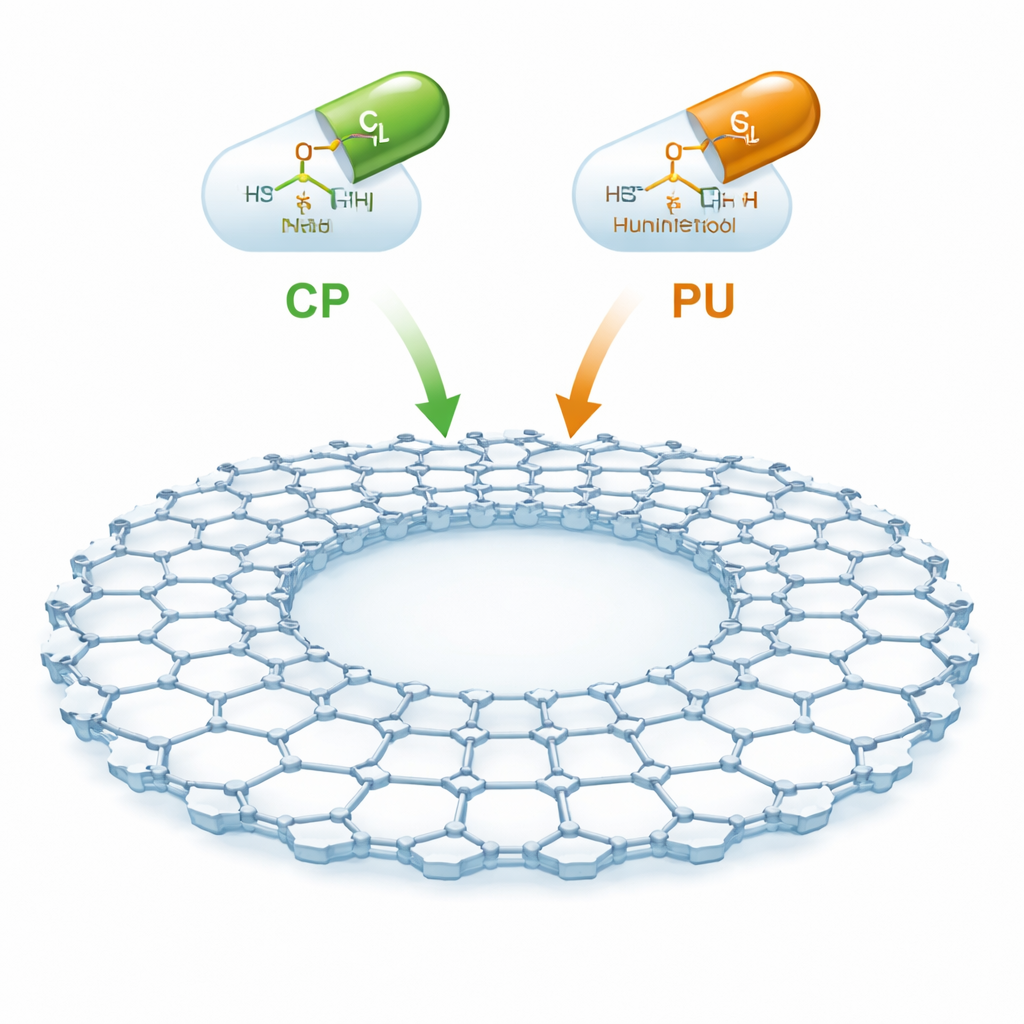
Le CTF-2 est un matériau synthétique construit à partir d’anneaux de carbone et d’azote reliés en un réseau plat en forme de feuille avec une grande cavité centrale et beaucoup d’espace ouvert. Parce qu’il est fin, stable et poreux, il offre une très grande surface interne pour piéger des molécules médicamenteuses. Les auteurs se sont concentrés sur deux médicaments anticancéreux importants : le cyclophosphamide, largement utilisé pour les hémopathies et les tumeurs solides, et le purinethol (aussi appelé mercaptopurine), employé contre certaines leucémies et certaines maladies inflammatoires de l’intestin. L’idée est d’arrimer ces médicaments en douceur à la surface du CTF-2 pour qu’ils puissent être transportés dans la circulation sanguine et libérés de façon plus sélective, réduisant ainsi les dommages aux tissus sains.
Explorer l’invisible par des expériences informatiques
Plutôt que de travailler en laboratoire humide, l’équipe a utilisé des calculs informatiques de niveau quantique avancés (théorie de la fonctionnelle de la densité et méthodes apparentées) pour évaluer la force avec laquelle chaque médicament adhérerait au CTF-2 et ce qui maintient les complexes ensemble. Ils ont optimisé les géométries du CTF-2 avec chaque médicament, mesuré les distances entre atomes au point de contact, et calculé l’énergie gagnée lorsque le médicament s’adsorbe sur le cadre. Pour le cyclophosphamide, l’énergie d’adsorption calculée était d’environ −1,04 électron-volt, un peu plus forte que les −0,82 électron-volt trouvés pour le purinethol. Ces valeurs, qui restent clairement favorables même après correction d’artéfacts techniques et simulation de l’eau comme solvant, indiquent que les deux médicaments se lient suffisamment fermement pour être chargés mais pas au point d’empêcher une libération ultérieure.
Des forces douces qui accomplissent un travail important
L’étude montre que la « colle » entre les médicaments et le CTF-2 n’est pas une liaison chimique dure mais un réseau de forces douces, non covalentes. Grâce à des analyses spécialisées de la densité électronique — essentiellement des cartes indiquant où résident les électrons partagés — les chercheurs ont observé que les attractions de van der Waals (les mêmes forces faibles qui permettent aux geckos de grimper aux murs) et des interactions électrostatiques modérées dominent. Ces interactions se produisent à des distances courtes mais non liantes entre les atomes d’hydrogène, d’azote, d’oxygène, de soufre et de carbone des médicaments et du cadre. Des calculs supplémentaires décomposant l’attraction totale en différents composants ont confirmé que les forces électrostatiques et de dispersion (van der Waals) fournissent la majeure partie de l’attraction stabilisante, tandis que des forces répulsives empêchent le médicament de s’enfoncer trop profondément ou de se lier de manière irréversible.
Signes d’un chargement stable et d’une libération modulable
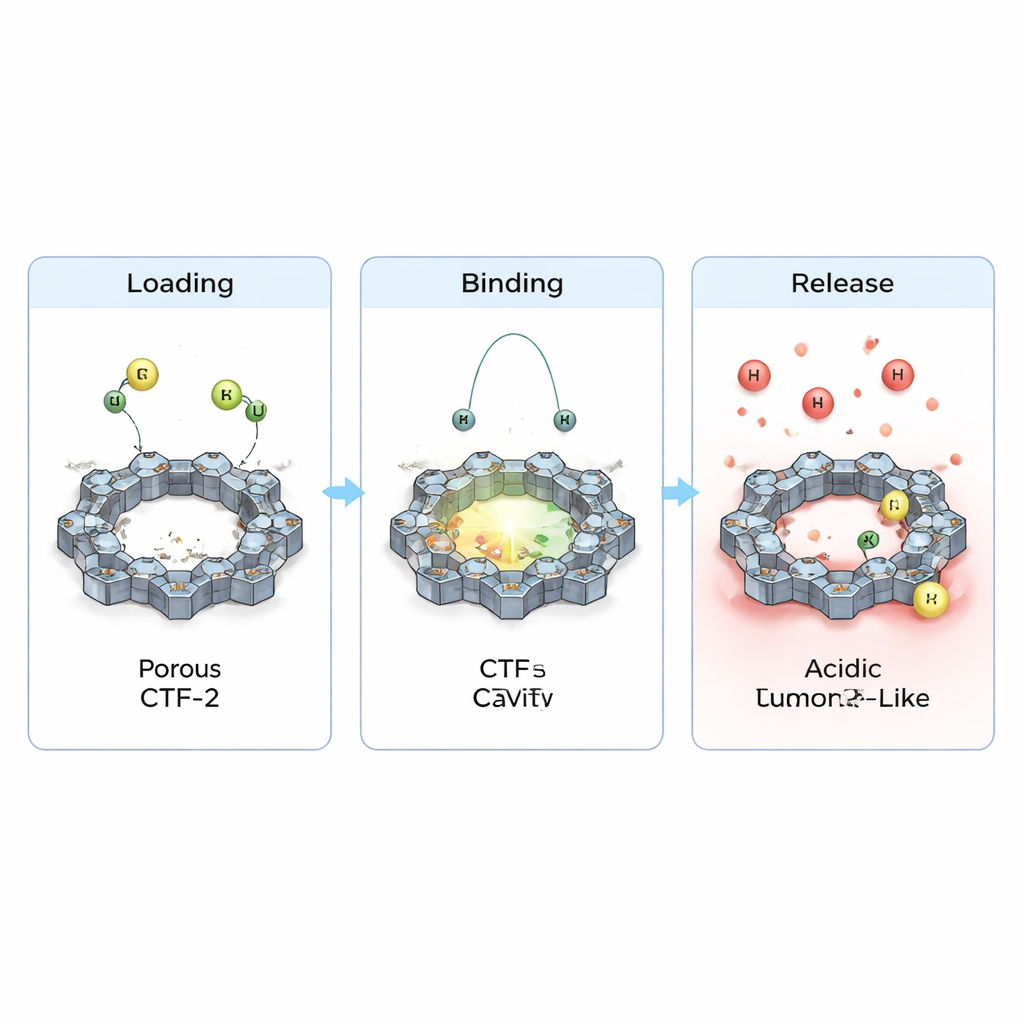
L’équipe a également examiné comment les électrons se redistribuent lorsque les médicaments reposent sur le CTF-2, et comment cela modifie les propriétés électriques de base. Ils ont observé de faibles mais nettes transferts de charge entre chaque médicament et le cadre et un léger rétrécissement du gap d’énergie qui sépare les états électroniques remplis des états vides. Cela implique que la réactivité et la conductivité du matériau sont subtilement modifiées lors du chargement, une caractéristique utile pour d’éventuelles applications de détection ou théranostiques. De façon cruciale, lorsqu’ils ont simulé l’environnement plus acide trouvé près des tumeurs en ajoutant des protons supplémentaires, la liaison calculée s’est affaiblie et les distances de contact ont augmenté. En termes simples, les simulations suggèrent que le CTF-2 peut retenir les médicaments dans des conditions sanguines normales, mais les libérer plus facilement dans des milieux tumoraux acides — exactement le comportement souhaité pour une délivrance ciblée.
Ce que cela signifie pour les traitements anticancéreux futurs
Pris dans leur ensemble, ces calculs dépeignent le CTF-2 comme un transporteur prometteur pour le cyclophosphamide et le purinethol : il peut les empiler sur sa surface poreuse de façon stable, les protéger durant la circulation, puis les relâcher quand la chimie locale change autour d’une tumeur. Bien que ce travail soit théorique et nécessite une confirmation expérimentale, il suggère que des cadres riches en azote finement conçus comme le CTF-2 pourraient aider à transformer des médicaments de chimiothérapie anciens mais efficaces en traitements plus intelligents — délivrant des doses puissantes là où elles sont le plus nécessaires tout en réduisant les dommages collatéraux aux cellules saines.
Citation: Tariq, T., Yar, M., Bayach, I. et al. A density functional theory study of cyclophosphamide and purinethol adsorption on a covalent triazine framework (CTF-2) for drug delivery applications. Sci Rep 16, 6125 (2026). https://doi.org/10.1038/s41598-026-36405-5
Mots-clés: nanotransporteur, administration de médicaments, chimiothérapie du cancer, cadre triazine covalent, modélisation computationnelle