Clear Sky Science · fr
Un cadre interactif en cascade d’apprentissage profond avec affinage par un expert pour une segmentation précise des sous-régions striatales
Pourquoi cartographier de minuscules régions cérébrales importe
Le striatum, une petite structure enfouie au cœur du cerveau, joue un rôle central dans le mouvement et la motivation et est fortement affecté dans des troubles comme la maladie de Parkinson. Les médecins utilisent souvent des scintigraphies PET et des IRM pour mesurer les changements chimiques dans cette zone, mais le striatum est divisé en nombreuses sous-régions minuscules qui sont difficiles à visualiser et à délimiter avec précision. Cet article présente une nouvelle méthode assistée par ordinateur, appelée StriaSeg‑iARM, qui aide les spécialistes à tracer ces limites de façon plus précise et plus efficace, même chez des personnes dont le cerveau est altéré par le vieillissement ou la maladie.
Le problème clinique sous les yeux
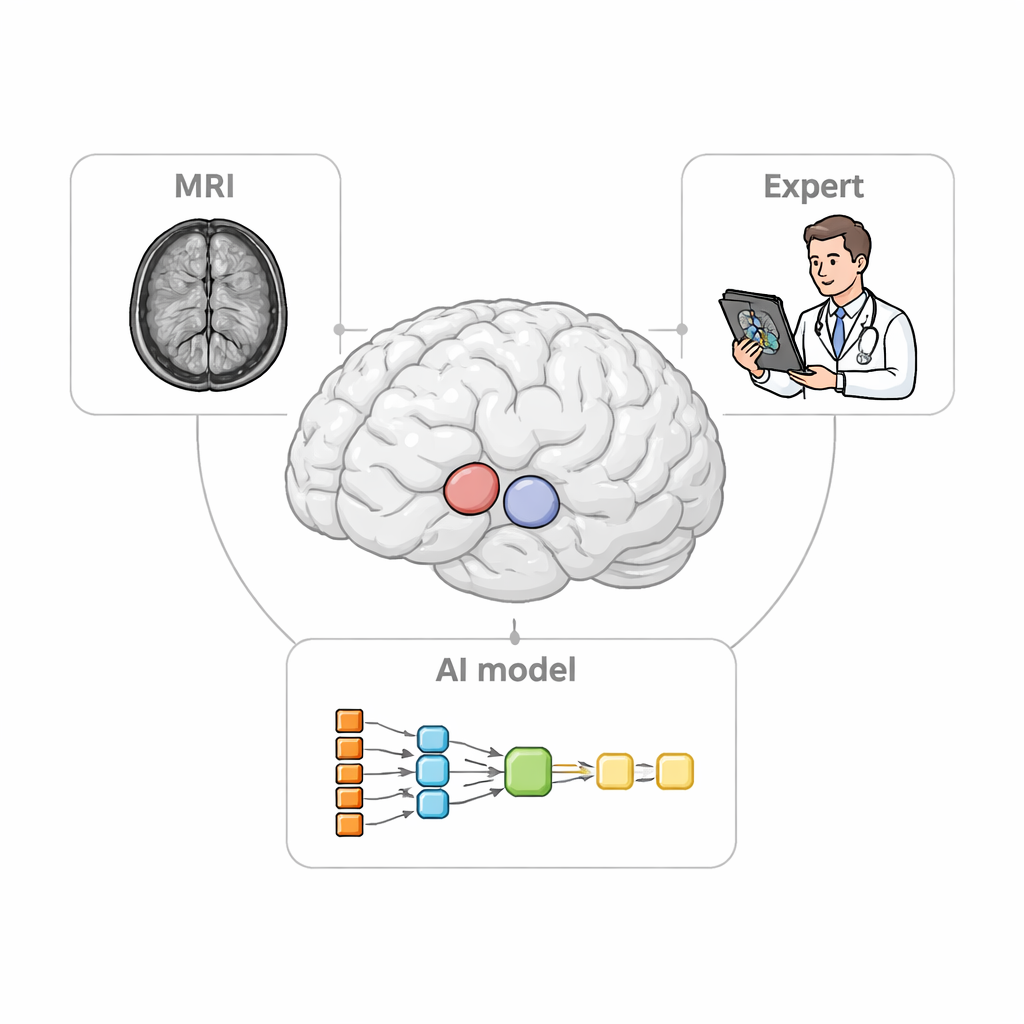
Lorsque les neurologues évaluent des affections comme la maladie de Parkinson, ils s’appuient sur des scans PET pour suivre comment les signaux liés à la dopamine varient selon les différentes parties du striatum. Pour faire cela correctement, ils doivent d’abord définir de petites « régions d’intérêt » tridimensionnelles sur l’IRM, qui servent de récipients de mesure pour les données PET. Le tracé manuel de ces régions est un travail lent et fastidieux et peut varier d’un expert à l’autre. Les logiciels existants ne localisent automatiquement que les structures les plus larges et peinent souvent chez des patients dont le cerveau est rétréci ou déformé, situation fréquente dans les maladies neurodégénératives avancées. Ces limites peuvent estomper le véritable schéma des lésions et affaiblir la valeur diagnostique de l’imagerie.
Un assistant plus intelligent en deux étapes
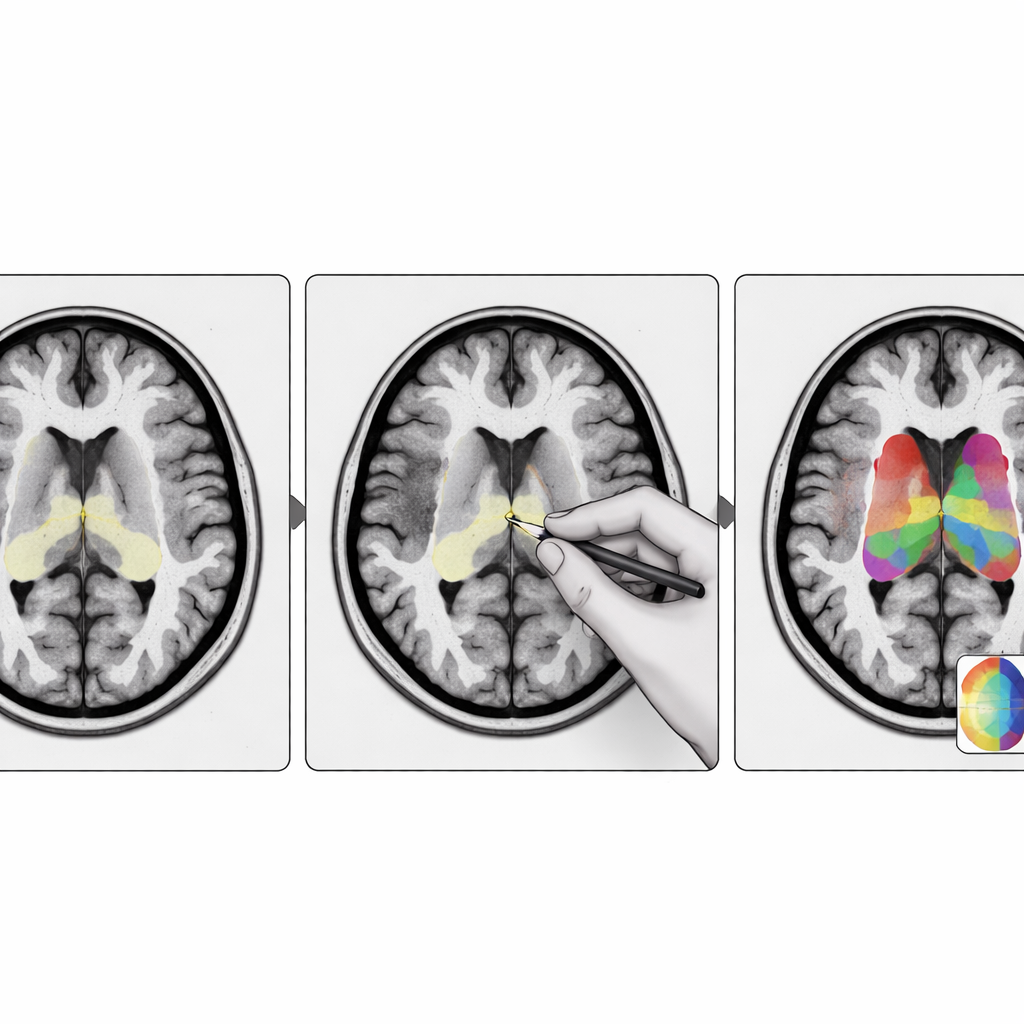
Les chercheurs ont conçu StriaSeg‑iARM comme un système d’apprentissage profond en deux étapes qui travaille directement dans l’espace cérébral propre à chaque personne plutôt que d’imposer l’alignement sur un modèle standard. Dans la première étape, le programme repère le striatum global sur une IRM tridimensionnelle. Dans la seconde, il divise cette structure en 12 sous-régions anatomiquement définies de chaque côté du cerveau. Entre ces deux étapes se trouve l’innovation clé : une étape interactive où un expert peut rapidement vérifier et, si nécessaire, corriger le contour grossier produit par la première étape avant de lancer la subdivision plus fine. Cette approche marie la rapidité de l’automatisation au jugement d’un observateur humain formé.
Entraînement et test sur des cerveaux du monde réel
Pour apprendre au système ce qu’il doit reconnaître, l’équipe a rassemblé des centaines d’IRM issues de plusieurs hôpitaux et types de scanners, et a créé des tracés manuels soignés des 12 sous‑régions striatales. Ils ont ensuite testé le modèle sur deux jeux de données externes incluant à la fois IRM et PET liés à la dopamine : l’un provenant de patients de Parkinson relativement précoces et de volontaires sains, et l’autre d’un groupe clinique plus âgé et plus gravement atteint, avec une atrophie cérébrale marquée et des diagnostics mixtes. Dans ces cas difficiles, StriaSeg‑iARM a systématiquement mieux reproduit les tracés manuels des experts que les méthodes traditionnelles basées sur des atlas et qu’un modèle d’apprentissage profond à étape unique, avec un recouvrement plus élevé, des contours plus précis et des mesures de volume stables.
Des mesures plus nettes pour les scans de chimie cérébrale
Parce que l’objectif final est de quantifier les signaux PET, les auteurs ont aussi examiné comment différentes méthodes de segmentation influençaient les mesures PET. En utilisant une métrique standard de fixation du traceur dans chaque sous‑région, ils ont comparé les résultats automatiques à ceux basés sur des tracés manuels. La méthode par atlas avait tendance à sous-estimer la fixation, surtout chez les patients présentant des altérations plus sévères, tandis que le modèle d’apprentissage profond de base montrait encore un biais notable dans certaines régions. À l’inverse, les modèles en cascade — en particulier lorsque l’étape de correction interactive était utilisée — produisaient des valeurs PET qui suivaient de près la référence experte, avec un biais et une dispersion minimaux. L’équipe a en outre montré qu’un simple score d’incertitude issu de la première étape peut repérer environ un quart des cas les plus difficiles nécessitant un affinage expert, laissant le reste entièrement automatique.
Ce que cela signifie pour les patients et les cliniciens
Pour les non‑spécialistes, la conclusion est que de meilleures cartes numériques des petites régions cérébrales peuvent rendre les scans chimiques du cerveau plus fiables. StriaSeg‑iARM offre un cadre flexible dans lequel un modèle d’apprentissage profond réalise la majeure partie du travail, tout en permettant aux spécialistes d’intervenir pour corriger les cas difficiles sans réentraîner le système. Cette combinaison d’automatisation et de supervision experte améliore la précision des mesures utilisées pour diagnostiquer et suivre des troubles comme la maladie de Parkinson, et pourrait être adaptée à d’autres organes et maladies où de petites structures difficiles à voir détiennent des indices vitaux.
Citation: Kim, J., Kim, D., Kim, S. et al. An interactive cascaded deep learning framework with expert refinement for accurate striatal subregion segmentation. Sci Rep 16, 6550 (2026). https://doi.org/10.1038/s41598-026-36399-0
Mots-clés: Imagerie de la maladie de Parkinson, segmentation striatale, apprentissage profond en radiologie, PET IRM cérébral, biomarqueurs neurodégénératifs