Clear Sky Science · fr
Un souche de Staphylococcus capitis produisant deux bactériocines, la capidermicine et la micrococcine P1, montre une activité antimicrobienne à large spectre
Pourquoi de petites bactéries cutanées comptent face aux menaces de super‑bactéries
Les infections résistantes aux antibiotiques augmentent dans le monde et les médecins manquent de médicaments fiables. Une idée prometteuse consiste à mobiliser nos propres microbes « bénéfiques » pour combattre les microbes nuisibles. Cette étude se concentre sur une bactérie cutanée commune, Staphylococcus capitis, et montre qu’une souche particulière, appelée HBC3, produit naturellement deux molécules puissantes qui tuent les germes. Ensemble, ces molécules peuvent réduire des agents pathogènes dangereux rencontrés en milieu hospitalier, y compris Staphylococcus aureus résistant à la méthicilline (SARM), ce qui suggère que des bactéries cutanées amies pourraient devenir des outils futurs pour lutter contre les infections.
Un résident de la peau avec une puissance cachée
S. capitis vit normalement discrètement sur notre peau, en particulier sur le cuir chevelu, et est généralement inoffensif. Les chercheurs ont dépisté 18 souches de S. capitis prélevées dans le nez de volontaires pour voir si l’une d’elles pouvait inhiber le SARM, une cause majeure d’infections difficiles à traiter. Une souche, HBC3, s’est distinguée. Dans des tests en laboratoire, elle a fortement supprimé une grande variété de bactéries à Gram positif, y compris le SARM, des entérocoques résistants à la vancomycine (ERV), Streptococcus pyogenes, Listeria monocytogenes, ainsi que des espèces de Bacillus et Clostridium responsables de maladies graves. Notamment, elle n’a montré aucun effet sur plusieurs bactéries à Gram négatif courantes telles qu’Escherichia coli et Klebsiella pneumoniae, suggérant une action ciblée mais puissante plutôt qu’un pouvoir de destruction indifférencié. 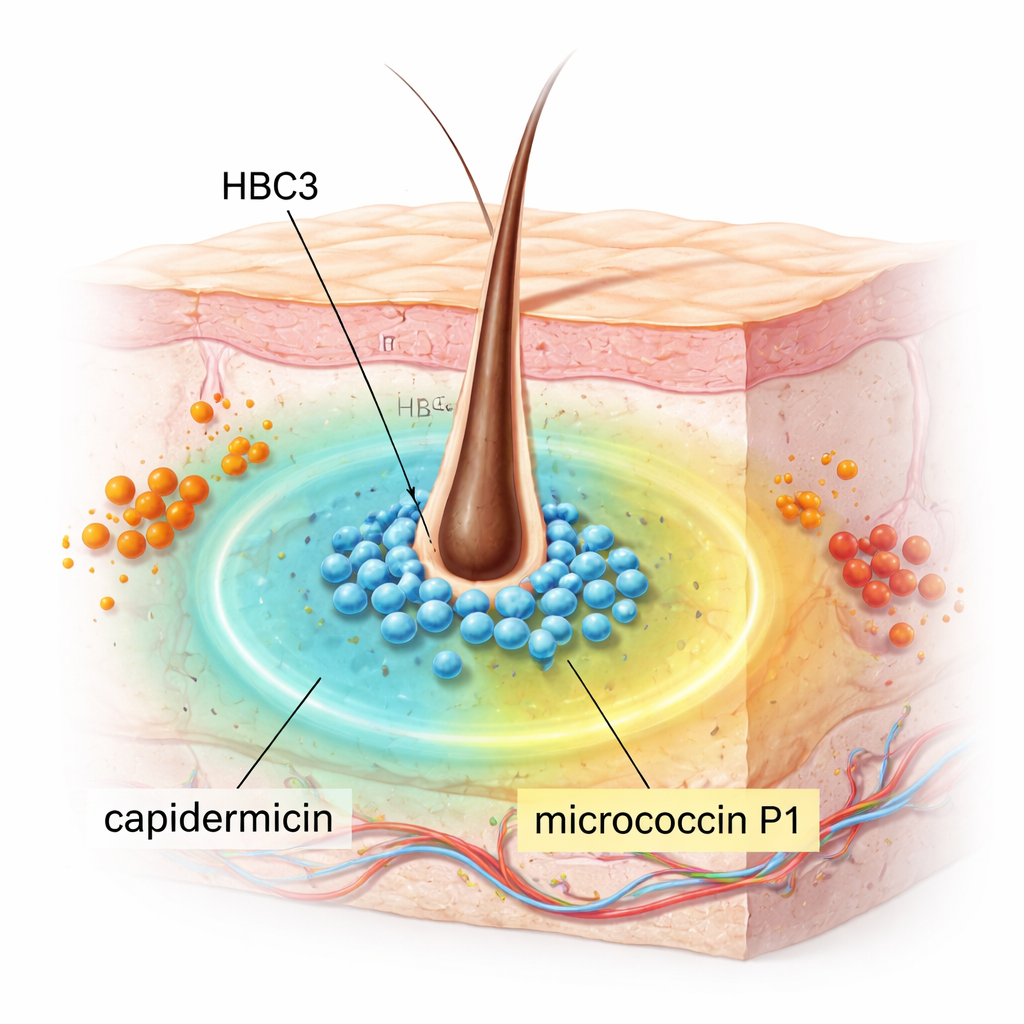
Deux antibiotiques naturels sur un seul « mini‑chromosome » génétique
Pour découvrir comment HBC3 exerce cette puissante activité antimicrobienne, l’équipe a séquencé son génome complet. Ils ont identifié un petit élément d’ADN circulaire, un plasmide nommé pHBC3_1, qui porte les instructions complètes pour produire deux bactériocines différentes — des peptides naturels de type antibiotique produits par des bactéries. L’un est la capidermicine, un petit peptide chargé positivement déjà observé dans d’autres souches de S. capitis. L’autre est la micrococcine P1 (MP1), une thiopeptide qui bloque la synthèse protéique chez les bactéries cibles et qui n’avait pas été rapportée auparavant chez S. capitis. Lorsqu’on a éliminé ce plasmide de HBC3, la souche a complètement perdu son activité antibactérienne, confirmant que ces gènes sont essentiels à ses capacités défensives.
Des cibles différentes, un objectif commun
En purifiant chaque bactériocine séparément, les scientifiques ont testé leur pouvoir d’inhibition sur divers microbes. La MP1 a montré une activité large et forte contre de nombreux cocci à Gram positif, y compris le SARM et les entérocoques, à faibles concentrations. La capidermicine, en revanche, était la plus efficace contre des bacilles à Gram positif comme Bacillus coagulans et Listeria, mais avait peu ou pas d’effet sur les staphylocoques dans les conditions utilisées ici. Lorsque l’équipe a combiné les deux peptides contre B. coagulans, ils ont observé un effet additif : des doses plus faibles utilisées ensemble produisaient une inhibition de croissance plus grande que chacune séparément. Ce ciblage complémentaire permet à HBC3 de supprimer une gamme plus large de concurrents en déployant deux armes moléculaires différentes adaptées à diverses formes bactériennes et surfaces cellulaires. 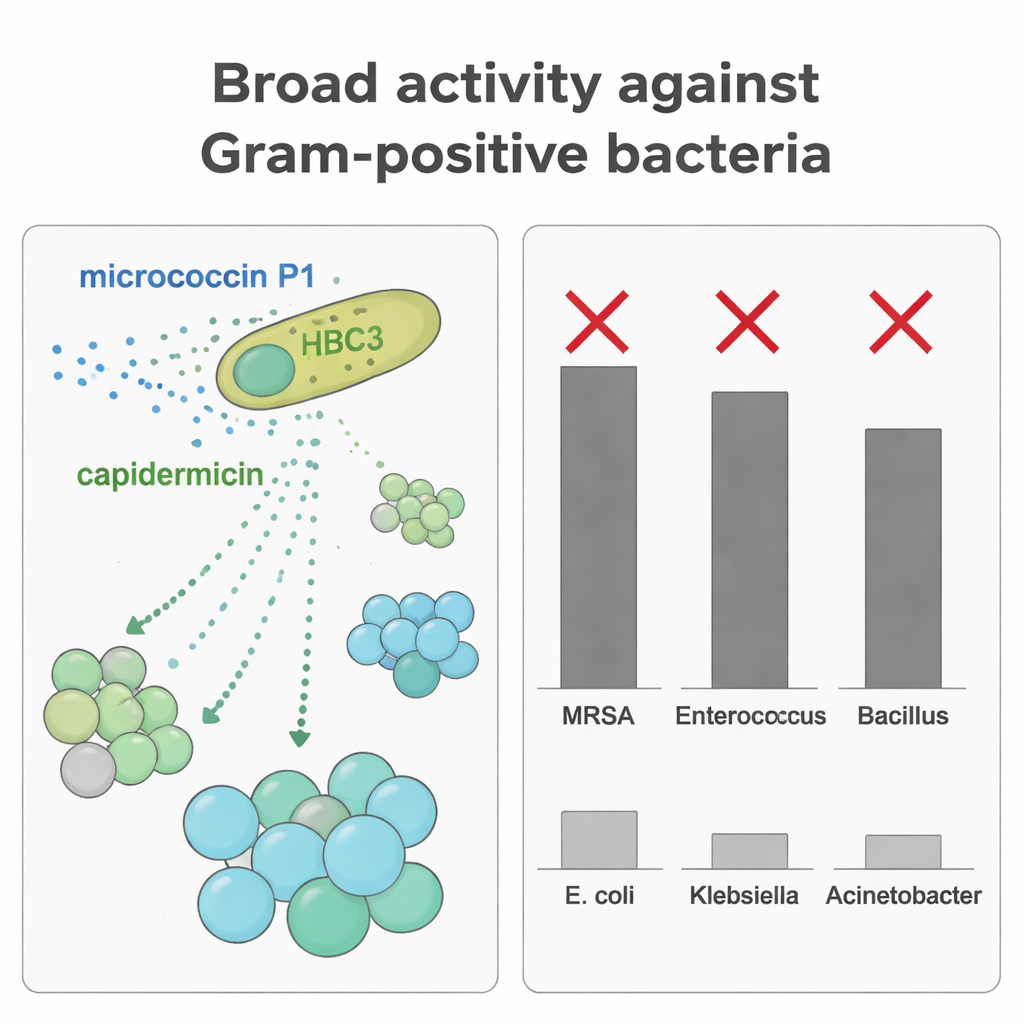
Gagner de l’espace dans des voisinages microbiens encombrés
Pour imiter la compétition en conditions réelles, les chercheurs ont cocultivé HBC3 avec SARM, ERV et B. coagulans sur les mêmes plaques. La souche HBC3 normale a presque complètement éliminé ces agents pathogènes des communautés mixtes, tandis qu’une version dépourvue du plasmide leur a permis de prospérer. Les comparaisons génétiques suggèrent que le plasmide à double bactériocine provient probablement d’anciennes fusions et réarrangements de plasmides séparés, facilités par des éléments d’ADN mobiles capables de déplacer des clusters de gènes entre bactéries. Ce plasmide composite confère à HBC3 un net avantage dans des environnements encombrés comme la peau ou les muqueuses, où de nombreux microbes se disputent nutriments et espace.
D’un allié cutané à un futur probiotique ?
L’étude conclut que S. capitis HBC3 possède une combinaison rare de deux bactériocines distinctes sur un même plasmide, ce qui lui permet d’inhiber fortement plusieurs pathogènes cliniquement importants à Gram positif, y compris des souches résistantes aux antibiotiques. Comme HBC3 ne fait pas partie d’une lignée connue à haut risque et ne porte pas de gènes de résistance détectables, elle pourrait être candidate au développement d’un probiotique ciblé ou d’un agent de décolonisation — conçu, par exemple, pour réduire sélectivement S. aureus sur la peau ou dans le nez tout en épargnant des voisins plus bénins. Avant que de telles applications deviennent réalité, la sécurité, l’efficacité chez l’animal et l’humain, et les impacts à long terme sur le microbiote normal devront être soigneusement évalués, mais ce travail met en lumière la manière dont nos propres microbes pourraient aider à contrer la crise persistante des super‑bactéries.
Citation: Ohdan, K., Suzuki, Y., Kawada-Matsuo, M. et al. Staphylococcus capitis strain producing dual bacteriocins, capidermicin and micrococcin P1, shows broad-spectrum antimicrobial activity. Sci Rep 16, 6835 (2026). https://doi.org/10.1038/s41598-026-36393-6
Mots-clés: bactériocines, Staphylococcus capitis, micrococcine P1, capidermicine, résistance aux antibiotiques