Clear Sky Science · fr
Déploiement de l’approche de criblage virtuel à haut débit (HTVS) pour l’identification de nouveaux inhibiteurs de la lactate déshydrogénase (LDH) présentant des propriétés anticancéreuses
Pourquoi cette recherche compte pour le traitement du cancer
Les cellules cancéreuses réorganisent souvent leur production d’énergie, et ce basculement peut être exploité pour concevoir des médicaments plus intelligents et plus sélectifs. Cette étude explore une enzyme métabolique clé, la lactate déshydrogénase (LDH), qui aide les tumeurs à prospérer dans des conditions difficiles et à résister aux traitements. Grâce à des criblages informatiques avancés et à des tests en laboratoire, les chercheurs ont identifié deux petites molécules nouvelles qui bloquent la LDH et montrent des effets anticancéreux prometteurs sur des lignées de cancer de la prostate.
Le métabolisme étrange des cellules cancéreuses
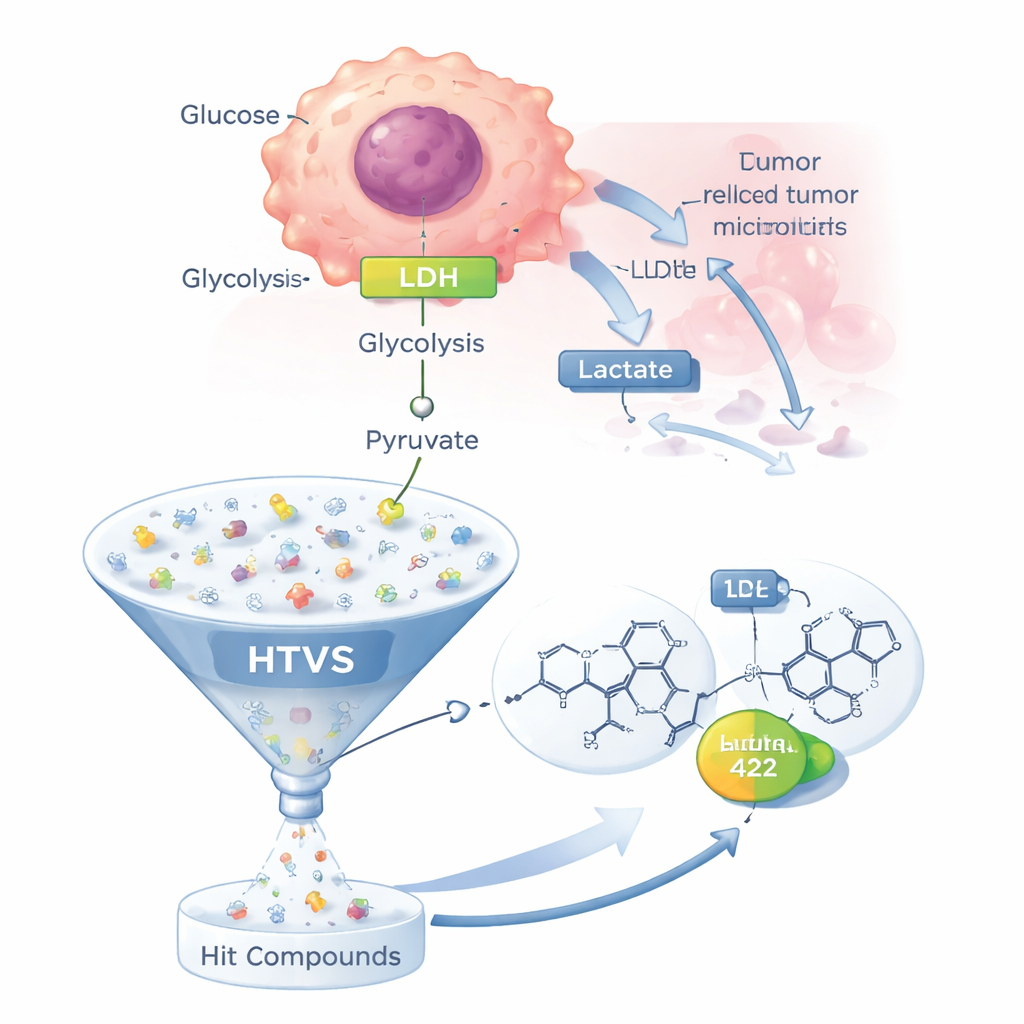
La plupart des cellules saines utilisent efficacement l’oxygène dans leurs mitochondries pour produire de l’énergie. Beaucoup de cellules cancéreuses, en revanche, comptent fortement sur une voie moins efficace appelée glycolyse, même lorsque l’oxygène est abondant — un phénomène connu sous le nom d’effet Warburg. Dans cette voie de raccourci, le glucose est dégradé en pyruvate, qui est ensuite converti en lactate par la LDH au lieu d’être acheminé vers les mitochondries. Le lactate est expulsé hors de la cellule, acidifiant l’environnement tumoral, aidant les cellules cancéreuses à échapper à la mort cellulaire, à affaiblir l’attaque immunitaire et même à atténuer l’effet de nombreux médicaments chimiothérapeutiques. Comme la LDH se trouve au cœur de ce métabolisme altéré et qu’aucun médicament ciblant la LDH n’a encore été approuvé, elle est devenue une cible prioritaire pour de nouvelles thérapies anticancéreuses.
Utiliser les ordinateurs pour trier un demi-million de molécules
Plutôt que de tester les candidats un par un en laboratoire, l’équipe a utilisé une stratégie de criblage virtuel à haut débit (HTVS). Ils ont commencé avec 28 molécules rapportées dans la littérature comme bloquant la LDH et en ont extrait un « pharmacophore » — un schéma 3D abstrait de caractéristiques que tout bon inhibiteur de la LDH est susceptible de partager. Ils ont ensuite appliqué ce modèle à une bibliothèque commerciale d’environ 500 000 molécules de type médicament, cherchant lesquelles correspondaient aux caractéristiques essentielles. Environ 110 000 molécules ont franchi ce premier filtre, et une sélection supplémentaire basée sur des règles standard de « drug-likeness » a réduit la liste à 2 337 candidats plus réalistes pour le dockage sur l’enzyme LDH.
Se concentrer sur les meilleurs ligands
L’étape suivante consistait à estimer avec quelle affinité ces candidats pourraient s’insérer dans le site actif de la LDH. En utilisant plusieurs niveaux de docking computationnel, les chercheurs ont calculé comment chaque molécule pourrait interagir avec des acides aminés spécifiques à l’intérieur de la cavité enzymatique. Ce processus en plusieurs étapes a progressivement réduit le nombre de candidats de milliers à seulement 59 molécules prometteuses, puis à cinq « hits » clairs présentant une affinité prédite particulièrement forte. Deux d’entre elles, désignées composés 15 et 422, se sont distinguées car des simulations de dynamique moléculaire suggéraient qu’elles forment des complexes exceptionnellement stables avec la LDH au fil du temps, maintenant des contacts clés avec des résidus critiques du site actif tout en préservant une structure protéique globale raisonnable.
Du criblage aux cellules cancéreuses réelles
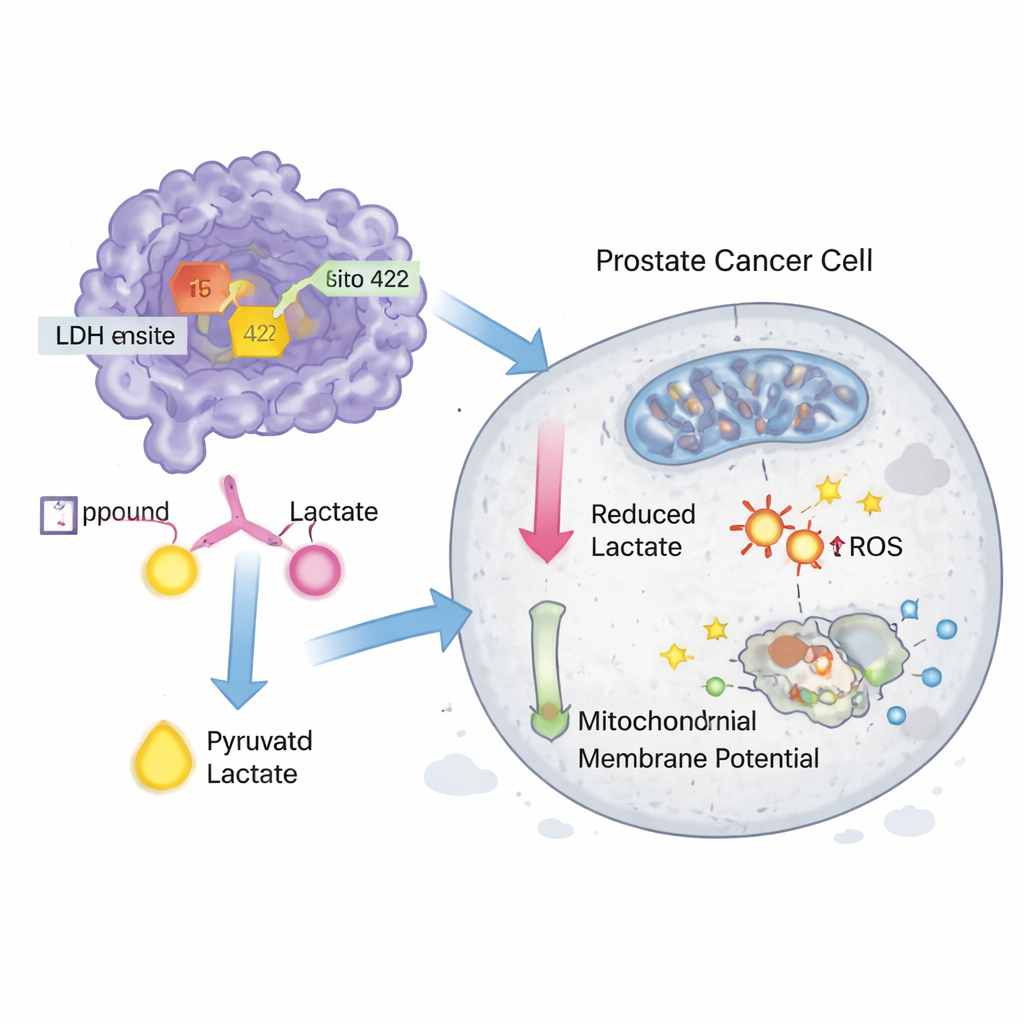
Pour vérifier si ces hits avaient un impact dans des systèmes vivants, les scientifiques ont acheté les composés 15 et 422 et les ont testés sur des lignées de cancer de la prostate DU-145 et PC-3. Les deux molécules ont inhibé l’activité de la LDH dans les cellules à des concentrations nanomolaires et ont également ralenti directement l’activité d’une enzyme LDH purifiée, bien qu’elles fussent quelque peu moins puissantes qu’un inhibiteur expérimental connu, GNE‑140. Dans des essais de croissance, les composés ont diminué la survie des cellules cancéreuses à de faibles doses micromolaires, se rapprochant à nouveau des performances de GNE‑140. Des expériences supplémentaires ont montré que les traitements augmentaient légèrement le stress oxydatif, perturbaient le potentiel de membrane mitochondrial — signe d’usure des « centrales énergétiques » — et déclenchaient la mort cellulaire programmée (apoptose) dans les cellules DU‑145, le composé 15 étant le plus actif des deux.
Ce que cela pourrait signifier pour les futurs médicaments contre le cancer
Bien que ces molécules ne soient pas des médicaments prêts à l’emploi, elles constituent des points de départ précieux pour la conception de médicaments. Les composés 15 et 422 présentent des propriétés chimiques suggérant une meilleure solubilité, perméabilité et « drug-likeness » globale que certains inhibiteurs de LDH existants, ce qui en fait des candidats attractifs pour une optimisation ultérieure. L’étude démontre comment un criblage informatique à grande échelle, guidé par des caractéristiques structurelles connues, peut mettre au jour de nouveaux inhibiteurs de LDH affaiblissant les cellules cancéreuses en privant leur approvisionnement énergétique altéré. Avec des travaux futurs visant à affiner leurs structures, tester plus rigoureusement la liaison directe et étudier leur comportement chez l’animal, ces composés pourraient contribuer à une nouvelle classe d’agents anticancéreux attaquant les tumeurs via leurs vulnérabilités métaboliques uniques.
Citation: Huang, Y., Benni, S., Yadav, U.P. et al. Deploying the high-throughput virtual screening (HTVS) approach for the identification of new lactate dehydrogenase (LDH) inhibitors with anticancer assets. Sci Rep 16, 5921 (2026). https://doi.org/10.1038/s41598-026-36385-6
Mots-clés: inhibiteurs de la lactate déshydrogénase, métabolisme du cancer, criblage virtuel, cancer de la prostate, découverte de médicaments anticancéreux