Clear Sky Science · fr
Démêler la pathogenèse de la BPCO : une approche multi-omique pour identifier des métabolites et des liens génétiques
Pourquoi la maladie pulmonaire et la chimie du corps sont liées
La broncho-pneumopathie chronique obstructive (BPCO) est surtout connue comme une maladie du fumeur, mais cette étude montre que ce qui se passe dans la chimie sanguine peut être tout aussi important que ce que nous inhalons. En combinant de vastes jeux de données génétiques, des mesures détaillées de petites molécules dans le sang et des expériences en laboratoire sur des cellules des voies aériennes humaines, les chercheurs révèlent comment une altération du traitement des lipides dans l’organisme pourrait contribuer à la BPCO — et comment un médicament inhalé bien connu, le salbutamol, pourrait aider d’une manière nouvelle et surprenante.
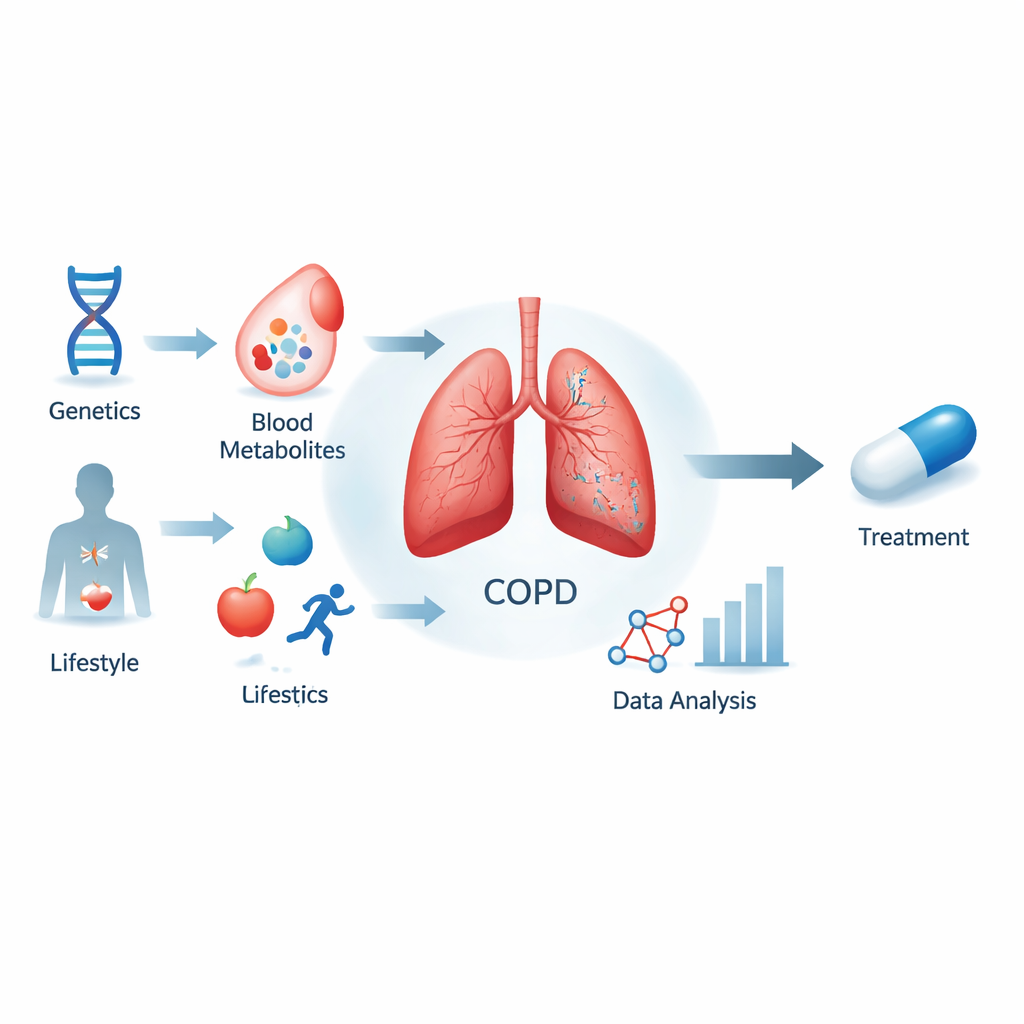
Regarder la BPCO au-delà du tabagisme
La BPCO touche des centaines de millions de personnes dans le monde et devrait devenir la troisième cause de mortalité. Si le tabagisme et la pollution de l’air sont des facteurs majeurs, ils n’expliquent pas entièrement qui développera la maladie ni sa vitesse de progression. L’équipe a cherché à savoir si des molécules sanguines spécifiques, appelées métabolites, sont non seulement des marqueurs de dommages mais aussi des acteurs actifs de la maladie. Ils se sont concentrés sur plus de 1 400 métabolites mesurés dans de larges études européennes et ont relié ceux-ci au risque de BPCO en utilisant les différences génétiques des individus comme une sorte d’expérience naturelle.
Utiliser les gènes pour tester la cause et l’effet
Pour dépasser la simple corrélation, les chercheurs ont employé une technique appelée randomisation mendélienne. En termes simples, ils ont suivi si des personnes nées avec des variantes génétiques qui augmentent ou diminuent certains métabolites ont aussi des risques plus élevés ou plus faibles de développer la BPCO. Cette approche aide à distinguer les causes véritables des habitudes de vie qui peuvent brouiller le tableau, comme la consommation de café ou le tabagisme. Sur 1 400 métabolites, six semblaient initialement liés au risque de BPCO. Cependant, un second test génétique plus strict a montré que seuls deux — la carnitine C14 et la 3-hydroxyoléoylcarnitine — partagent le même signal génétique sous-jacent que la BPCO elle‑même. Les deux sont liés à la façon dont l’organisme traite les acides gras à longue chaîne, ce qui suggère que le métabolisme des lipides, et pas seulement l’inflammation et le flux d’air, est au cœur de la BPCO.
Des molécules aux interrupteurs de contrôle clés
Une fois les deux métabolites robustes identifiés, les chercheurs les ont rattachés aux « routes » métaboliques qu’ils empruntent. Ces routes convergent vers le métabolisme des acides gras et ont mis en évidence un ensemble d’enzymes qui fonctionnent comme des feux de signalisation, contrôlant la synthèse et la dégradation des lipides — en particulier les enzymes ACACA et ACACB. En explorant des bases de données existantes sur les médicaments et les interactions protéiques, l’équipe a découvert que ces enzymes se trouvent dans le même réseau que ADRB2, la cible protéique du salbutamol, un inhalateur de secours courant pour la BPCO. Des analyses de tissus pulmonaires de patients ont montré que ACACA et ACACB étaient augmentés, tandis qu’ADRB2 était diminué, cohérent avec un état de surcharge en acides gras dans les poumons malades.
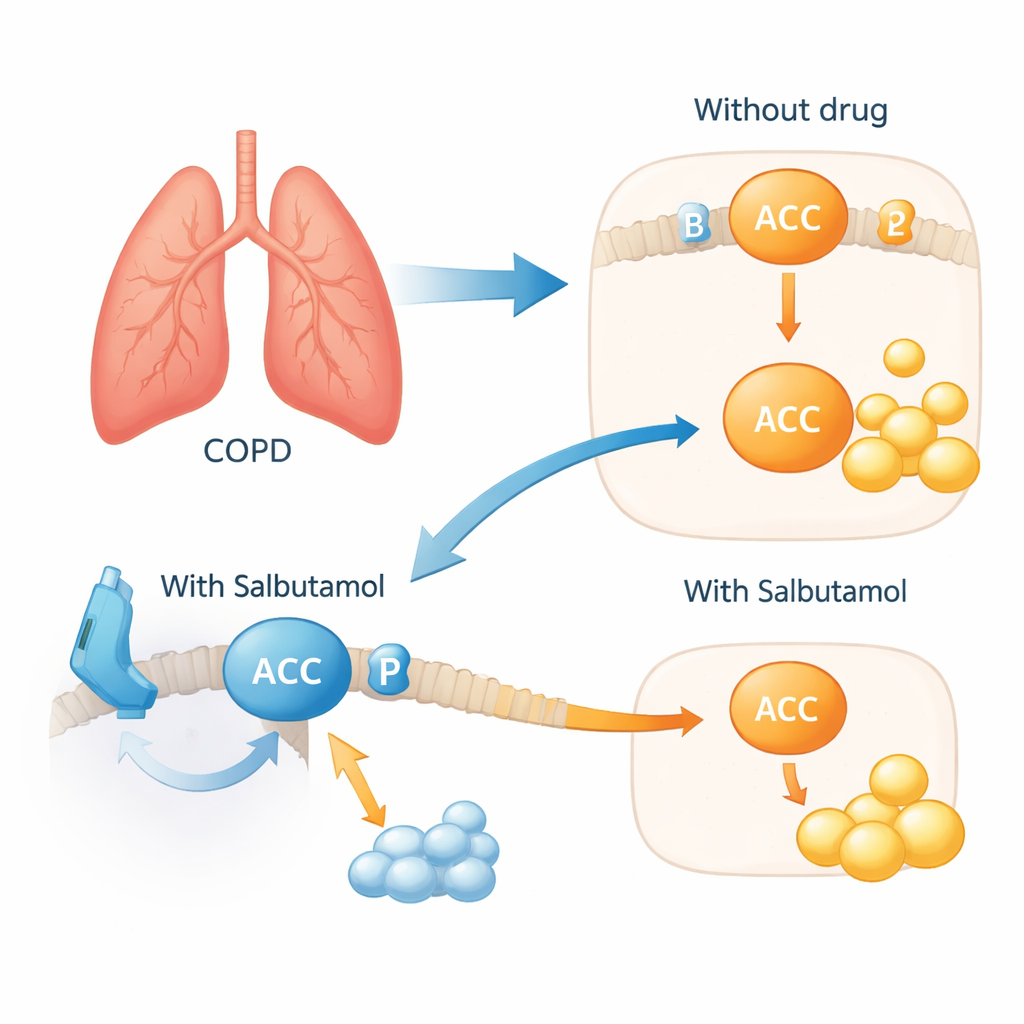
Un inhalateur qui calme aussi l’emballement des lipides
Pour tester si ce réseau est pertinent dans des cellules vivantes, les scientifiques ont exposé des cellules bronchiques humaines à un extrait de fumée de cigarette pour imiter le stress de type BPCO. Les cellules ont réagi en augmentant ACACA et ACACB et en réduisant une marque chimique protectrice sur ACACA qui, normalement, limite la production de lipides. L’ajout de salbutamol a inversé ce schéma néfaste : la marque protectrice sur ACACA a été restaurée et les signes d’une synthèse lipidique excessive ont diminué. En termes simples, le médicament semble avoir freiné la machinerie de construction des lipides au sein des cellules des voies aériennes, en agissant via l’interrupteur ADRB2 à la surface cellulaire. Des analyses génétiques liées au mode de vie ont en outre soutenu l’idée que les deux métabolites clés sont liés à la biologie sous-jacente plutôt qu’à des habitudes comme la consommation de café, qui avait expliqué plusieurs autres molécules candidates.
Ce que cela signifie pour les patients et les traitements futurs
Pour les non-spécialistes, le message est que la BPCO pourrait être provoquée en partie par un embouteillage métabolique dans la manière dont les cellules pulmonaires traitent les lipides, et qu’un bronchodilatateur largement utilisé pourrait aussi aider discrètement à dégager cet embouteillage. La carnitine C14 et la 3-hydroxyoléoylcarnitine apparaissent comme de solides marqueurs sanguins susceptibles, un jour, d’aider à signaler les personnes à risque élevé ou à suivre la progression de la maladie. Les enzymes ACACA et ACACB, placées à des carrefours clés du métabolisme des lipides et liées à la cible du salbutamol ADRB2, offrent de nouvelles cibles pour les développeurs de médicaments. Bien que des travaux supplémentaires dans des populations diversifiées et des études métaboliques approfondies soient nécessaires, cette approche multi-omique ouvre une voie vers des traitements de la BPCO qui font plus qu’élargir les voies respiratoires — ils pourraient aussi restaurer une utilisation plus saine des carburants à l’intérieur des poumons.
Citation: Zeng, M., Liu, J., Cao, X. et al. Unraveling COPD pathogenesis: a multi-omics approach to identify metabolites and genetic links. Sci Rep 16, 6013 (2026). https://doi.org/10.1038/s41598-026-36368-7
Mots-clés: BPCO, métabolisme des acides gras, Salbutamol, biomarqueurs carnitine, multi-omique