Clear Sky Science · fr
Rôle des modifications d’histones médiées par MNX1 et de la famille de gènes PBX dans la leukémogenèse induite par MNX1
Pourquoi une petite erreur génétique compte pour des enfants malades
La plupart des leucémies infantiles sont aujourd’hui traitables, mais une forme rare appelée leucémie myéloïde aiguë (LMA) infantile reste particulièrement meurtrière. Beaucoup de ces nourrissons partagent le même accident génétique : deux chromosomes s’échangent des segments, transformant un gène de développement normalement discret, MNX1, en un moteur trop actif. Cette étude pose une question simple mais cruciale : une fois MNX1 activé, que fait-il concrètement dans les jeunes cellules sanguines pour les pousser vers le cancer — et peut‑on interrompre ce processus ?
Des cellules sanguines normales du bébé à une croissance incontrôlée
La leucémie apparaît lorsque des cellules sanguines immatures cessent de mûrir et se mettent à se multiplier de façon incontrôlée. Chez les nourrissons porteurs de la translocation t(7;12), MNX1 devient anormalement actif dans les cellules très précoces de la lignée hématopoïétique présentes dans le foie fœtal et la moelle osseuse. Les chercheurs ont construit un modèle murin qui reproduit cette situation : ils ont activé MNX1 humain dans des cellules souches fœtales hématopoïétiques, les ont transplantées chez des souris, et ont suivi la progression des animaux d’un état pré‑leucémique vers une leucémie manifeste. En comparant les cellules à ces différents stades avec des témoins sains, ils ont pu retracer comment MNX1 reprogramme progressivement les systèmes de contrôle internes de la cellule.
Comment MNX1 réécrit le mode d’emploi de la cellule
MNX1 est un facteur de transcription, une protéine qui se lie à l’ADN et régule l’activation ou la répression de gènes. L’équipe a combiné plusieurs méthodes puissantes — spectrométrie de masse, séquençage de l’ARN et profilage de la chromatine — pour identifier les partenaires de MNX1 et les gènes qu’il modifie. Ils ont constaté que MNX1 s’associe à des enzymes qui ajoutent des marques chimiques aux protéines histones, ces « bobines » autour desquelles l’ADN s’enroule. En particulier, MNX1 augmente une marque d’activation appelée H3K4me3 et diminue une marque de répression appelée H3K27me3 à certains sites du génome. Ces modifications relâchent la structure locale de l’ADN et facilitent l’activation de gènes clés liés à la croissance.
Un coup de pouce bref sur un gène de contrôle critique
Parmi les nombreux gènes affectés, un a retenu l’attention : Pbx1, membre de la famille PBX de protéines de liaison à l’ADN, longtemps associée à la leucémie. L’étude montre que MNX1 se lie directement à la région régulatrice du gène Pbx1, augmente la marque d’activation et élimine la marque de répression à cet endroit. Cela déclenche l’expression de Pbx1 très tôt, lorsque les cellules sont encore pré‑leucémiques. De façon surprenante, plus tard — une fois la leucémie installée — MNX1 n’est plus fortement associé à ce site, et pourtant le gène Pbx1 reste activé et ses marques d’histones restent dans une configuration favorable à la croissance. Cela suggère un mécanisme de « coup-de-pouce et départ » : MNX1 visite brièvement des régions clés de la chromatine, laisse derrière lui des marques épigénétiques durables, puis peut partir tandis que l’état altéré continue d’alimenter la maladie.
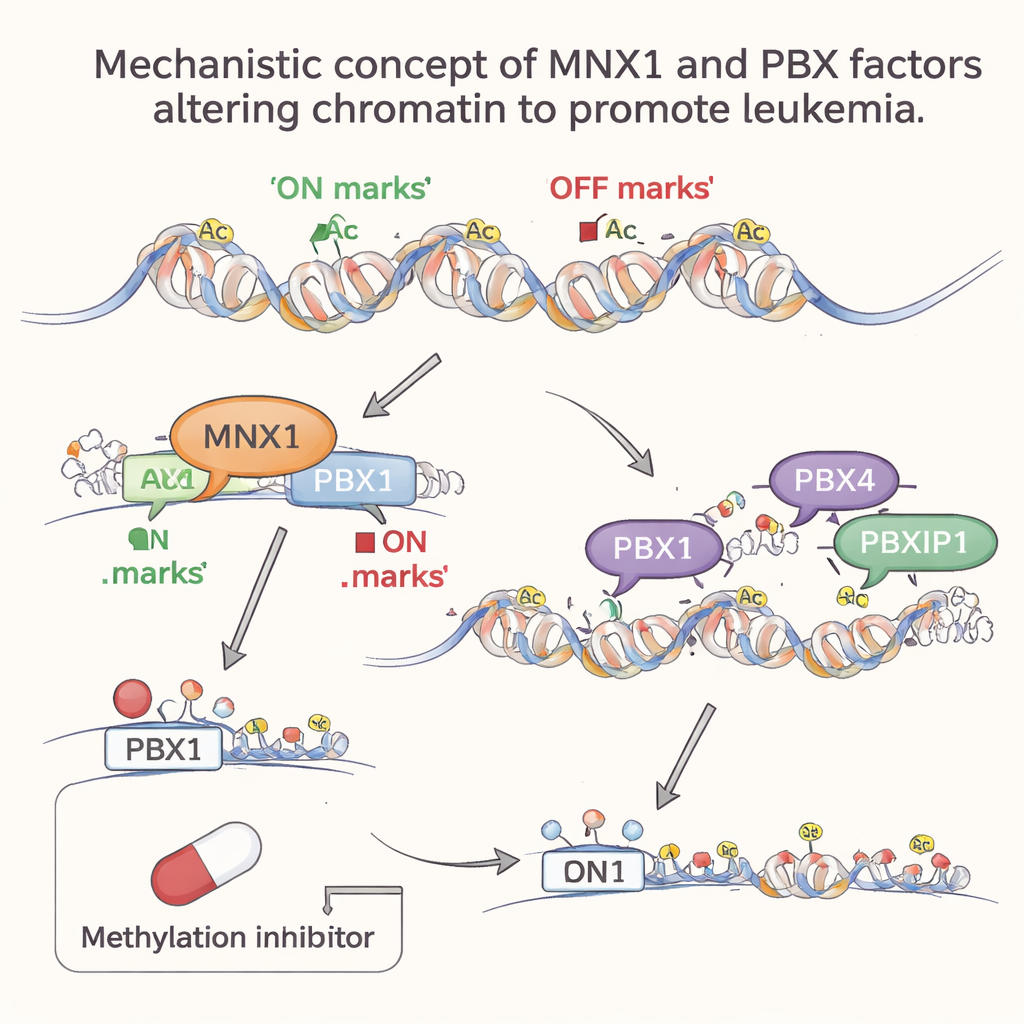
D’autres facteurs interviennent ensuite pour verrouiller l’état cancéreux
À mesure que la leucémie progresse, d’autres membres de la famille PBX, PBX4 et PBXIP1, deviennent plus actifs, mais seulement à ce stade avancé. Des analyses à l’échelle du génome ont montré que leurs motifs ADN préférés sont fortement enrichis dans des régions de chromatine ouvertes et actives qui ont été remodelées suite à l’activité de MNX1. Autrement dit, MNX1 remodèle d’abord le paysage de la chromatine et active Pbx1 ; ensuite PBX4 et PBXIP1 investissent ces régions nouvellement accessibles pour renforcer des programmes géniques anormaux qui favorisent la division cellulaire, bloquent la maturation hématopoïétique normale et altèrent la réparation de l’ADN. Cette implication progressive suggère une division du travail : PBX1 agit comme un interrupteur précoce dépendant de MNX1, tandis que PBX4 et PBXIP1 contribuent à maintenir le programme leucémique.
Bloquer les marques chimiques qui alimentent la leucémie
Parce que MNX1 agit via des enzymes qui ajoutent des groupes méthyle aux histones, l’équipe a testé si un inhibiteur large des méthyltransférases, la Sinefungine, pouvait perturber cette chaîne d’événements. Dans des cellules sanguines fœtales pré‑leucémiques exprimant MNX1, la Sinefungine a fortement réduit les niveaux de Pbx1, ce qui concorde avec un blocage de la méthylation spécifique du promoteur sur laquelle MNX1 s’appuie. En revanche, les niveaux de PBX4 et PBXIP1 ont peu changé, en accord avec leur activation plus tardive et indirecte au cours de la progression. Pris ensemble, ces résultats soutiennent l’idée que la LMA infantile avec t(7;12) n’est pas seulement causée par un gène cassé, mais par une cascade de changements épigénétiques durables initiés par MNX1.
Ce que cela implique pour les traitements futurs
Pour les non‑spécialistes, le message clé est que cette étude cartographie une réaction en chaîne : un gène MNX1 hyperactif reprogramme les marques chimiques sur les protéines qui emballent l’ADN, active précocement PBX1, et ouvre la voie à PBX4 et PBXIP1 pour verrouiller les cellules dans un état leucémique. Parce que ces étapes dépendent de motifs précis de méthylation des histones, elles offrent des cibles claires et testables pour des médicaments qui perturbent ces marques. À plus long terme, des thérapies visant l’axe MNX1–PBX ou les enzymes qui déposent ces étiquettes épigénétiques pourraient contribuer à éteindre les instructions défaillantes qui pilotent cette leucémie agressive chez les nourrissons, améliorant les chances d’un remède durable.
Citation: Malmhäll-Bah, E., Östlund, A., Nilsson, T. et al. Role of MNX1-mediated histone modifications and PBX gene family in MNX1-induced leukemogenesis. Sci Rep 16, 2593 (2026). https://doi.org/10.1038/s41598-026-36367-8
Mots-clés: leucémie myéloïde aiguë infantile, MNX1, PBX1 PBX4 PBXIP1, méthylation épigénétique des histones, translocation chromosomique t(7;12)