Clear Sky Science · fr
Compromis entre sites de recombinaison canoniques et inhabituels favorisant la diversité et la stabilité des ensembles de cassettes géniques des intégrons mobiles
Comment les bactéries mélangent leurs défenses
Les bactéries en milieu hospitalier font face à un flux constant d’antibiotiques, et pourtant beaucoup survivent et se propagent. Une raison majeure est un dispositif génétique appelé intégron, qui permet aux bactéries de collecter et de réarranger rapidement des gènes de résistance. Cet article explore un mode de fonctionnement inhabituel de ces dispositifs, montrant comment les bactéries équilibrent deux besoins à la fois : conserver suffisamment stable leurs gènes de résistance pour s’y fier, tout en restant assez flexibles pour s’adapter à de nouveaux médicaments.
Une boîte à outils génétique en attente
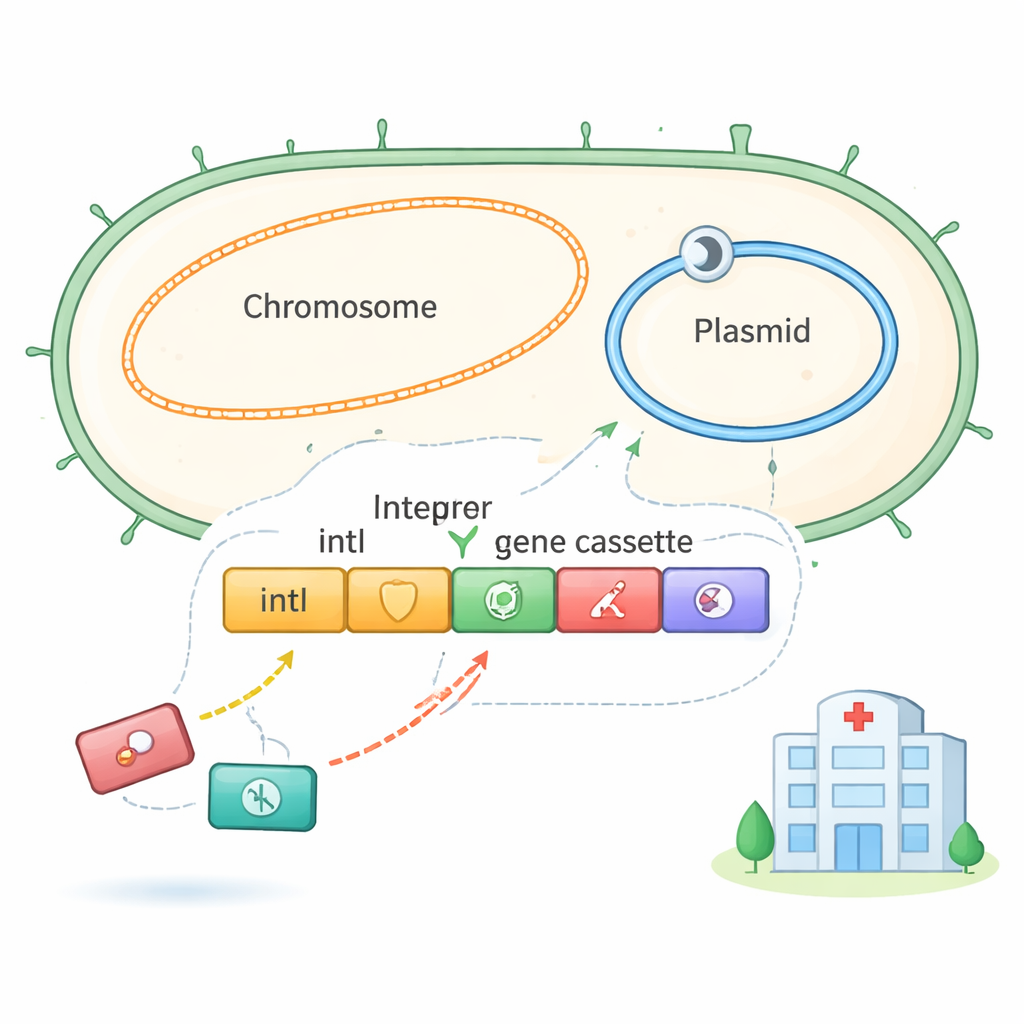
De nombreuses bactéries à Gram négatif portent des intégrons, de petites plateformes génétiques qui servent de stations d’amarrage pour des « cassettes géniques ». Chaque cassette contient typiquement un seul gène, souvent de résistance aux antibiotiques, accompagné d’un court signal d’ADN qui indique à l’enzyme de l’intégron, IntI, où couper et coller. Deux types principaux de signaux sont connus : attI, généralement au début de l’intégron, et attC, qui marque les cassettes standard. Quand les conditions changent, par exemple sous pression antibiotique, IntI peut remanier ces cassettes — ajouter de nouvelles, en retirer, ou modifier leur ordre — permettant à la bactérie d’ajuster rapidement ses défenses.
Des signaux étranges mais importants
Au-delà des signaux bien étudiés attI et attC, les auteurs se sont focalisés sur des versions étranges, partiellement délétées d’attI, appelées sites ΔattI. Celles-ci apparaissent dans des cassettes « inhabituelles » où le signal attC habituel a été remplacé par un fragment d’attI. En analysant plus de 1 700 intégrons complets issus de bases de données publiques, l’équipe a trouvé huit types distincts de ΔattI dans les intégrons de classes 1 et 2, principalement chez des bactéries liées aux milieux hospitaliers. Ils ont identifié 26 cassettes inhabituelles de type ΔattI, dont beaucoup codent la résistance à plusieurs familles d’antibiotiques. L’une d’elles, portant le gène de résistance blaOXA-10, était particulièrement fréquente, soulignant que même ces cassettes à l’apparence étrange sont répandues et cliniquement pertinentes.
Mettre les cassettes inhabituelles à l’épreuve
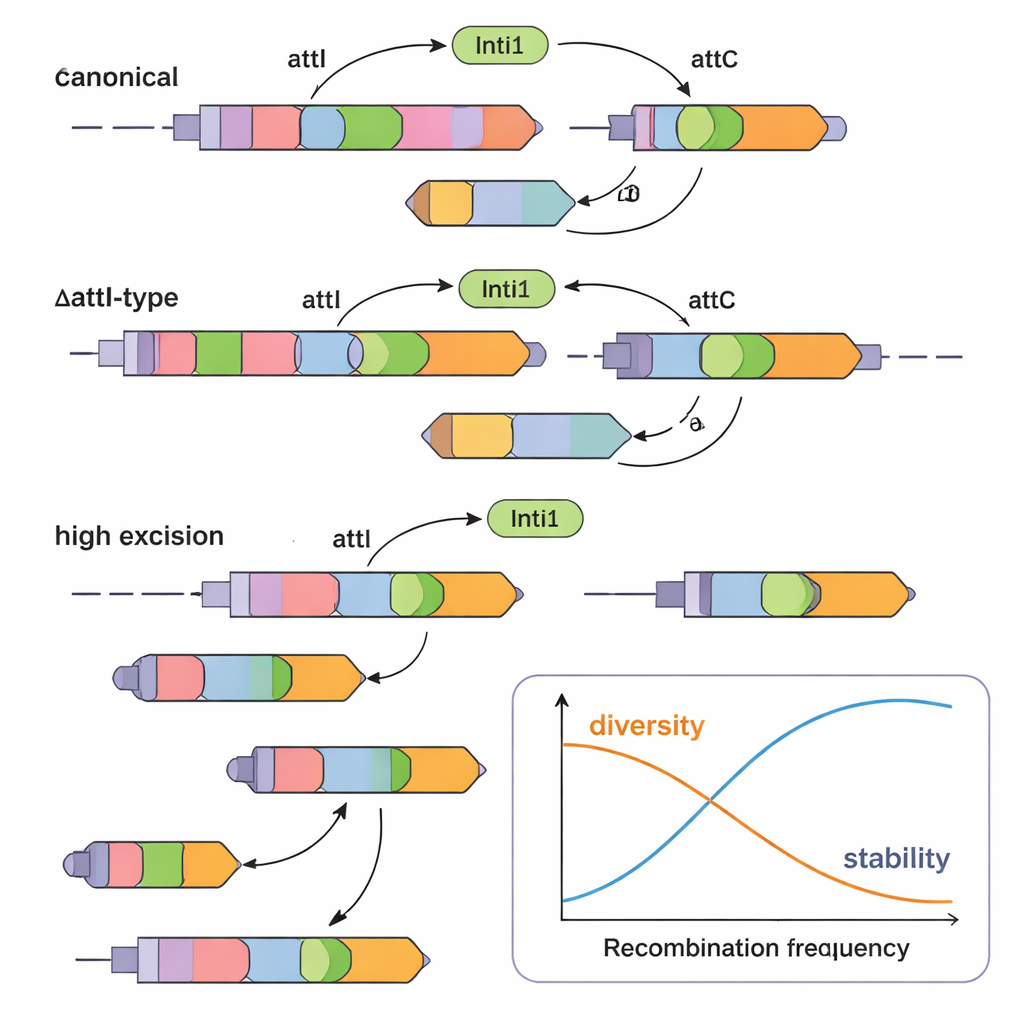
Pour vérifier si ces cassettes de type ΔattI fonctionnent réellement, les chercheurs en ont recréé plusieurs exemples en laboratoire. Ils les ont placées sur des plasmides dans E. coli avec l’enzyme IntI1 et ont mesuré la fréquence à laquelle les cassettes étaient excisées (retraites) ou insérées dans un site attI. Ils ont comparé des architectures canoniques (avec un attC normal à une extrémité) à des formes inhabituelles où l’attC en aval était remplacé par un fragment ΔattI court ou long. Résultat surprenant : de nombreuses cassettes de type ΔattI étaient pleinement actives. Certaines étaient excisées moins efficacement que les cassettes classiques mais insérées tout aussi bien, tandis que d’autres, en particulier celles portant un certain fragment ΔattI2, étaient excisées à des taux similaires aux cassettes standard. Cela montre que des signaux de recombinaison partiellement délétés peuvent encore servir de substrats robustes pour la machinerie des intégrons.
Pourquoi les gènes dupliqués disparaissent rarement
Les auteurs abordent aussi une autre énigme : pourquoi il est rare d’observer la même cassette de résistance dupliquée en tandem dans les intégrons, bien que cela pourrait augmenter la résistance en augmentant le dosage génique. Ils ont conçu des cassettes artificielles encadrées par des sites de recombinaison identiques de chaque côté — soit deux sites attI1, soit deux attC identiques autour du même gène. Dans ces architectures, IntI1 les a excisées avec une efficacité frappante, souvent supérieure à 97 % et jusqu’à 100 %. Autrement dit, dès qu’une cassette en tandem parfaite se forme, elle est presque instantanément supprimée. Cette instabilité intrinsèque aide à expliquer pourquoi les duplications de cassettes sont peu courantes dans la nature, sauf si une forte pression antibiotique favorise activement leur conservation.
Un équilibre intégré entre changement et contrôle
Pris ensemble, les résultats révèlent un équilibre subtil. Les intégrons utilisent un mélange de sites attI, attC et ΔattI pour ajuster la facilité avec laquelle différentes cassettes se déplacent. Les arrangements canoniques favorisent le remaniement efficace, tandis que les cassettes de type ΔattI et la perte rapide de duplications parfaites empêchent l’ensemble de se remplir de copies du même gène. Ce compromis permet aux bactéries de maintenir un assortiment diversifié d’options de résistance tout en évitant des configurations trop instables ou redondantes. Pour un lecteur non spécialiste, le message clé est que les bactéries ne se contentent pas de collecter passivement des gènes de résistance ; elles utilisent un système d’ADN sophistiqué qui gère activement quels gènes sont conservés, copiés ou éliminés, ce qui les aide à prospérer dans l’environnement riche en antibiotiques des hôpitaux modernes.
Citation: Gonzales Machuca, A., Molina, M.C., Álvarez, V.E. et al. Trade-off between canonical and unusual recombination sites promotes diversity and stability of gene cassette arrays of mobile integrons. Sci Rep 16, 6133 (2026). https://doi.org/10.1038/s41598-026-36353-0
Mots-clés: résistance aux antibiotiques, intégrons, cassettes géniques, évolution bactérienne, infections hospitalières