Clear Sky Science · fr
La baisse de CDC25C supprime la croissance du CHC via l’autophagie et l’apoptose induites par le stress mitochondrial
Pourquoi cette étude sur le cancer du foie est importante
Le cancer du foie est l’un des cancers les plus meurtriers au monde, et de nombreux patients sont diagnostiqués trop tard pour que la chirurgie ou les traitements standards soient très efficaces. Cette étude explore un « interrupteur » cellulaire unique, une protéine appelée CDC25C, qui semble favoriser la croissance du cancer du foie tout en étant moins cruciale pour les cellules hépatiques saines. En réduisant l’activité de cet interrupteur, les chercheurs ont constaté qu’ils pouvaient affaiblir et finalement tuer les cellules cancéreuses via les systèmes de nettoyage et d’autodestruction de la cellule, ce qui ouvre la voie à une stratégie thérapeutique prometteuse et plus sélective.
Un interrupteur de croissance à l’intérieur des tumeurs hépatiques
Toute cellule doit décider quand se diviser et quand s’arrêter. CDC25C est l’une des protéines clés qui poussent les cellules à travers le cycle de division. Dans le cancer du foie, cet interrupteur est souvent bloqué en position « marche », aidant les tumeurs à croître et à se disséminer. L’équipe a utilisé des cellules de cancer du foie de souris et des cellules hépatiques normales de souris, ainsi que des souris porteuses de tumeurs, pour réduire artificiellement les niveaux de CDC25C. Ils ont confirmé, par des tests génétiques et protéiques standard, que CDC25C était fortement réduit dans leur groupe expérimental par rapport aux témoins, établissant un modèle solide pour étudier ce qui se passe lorsque cet interrupteur de croissance est atténué.
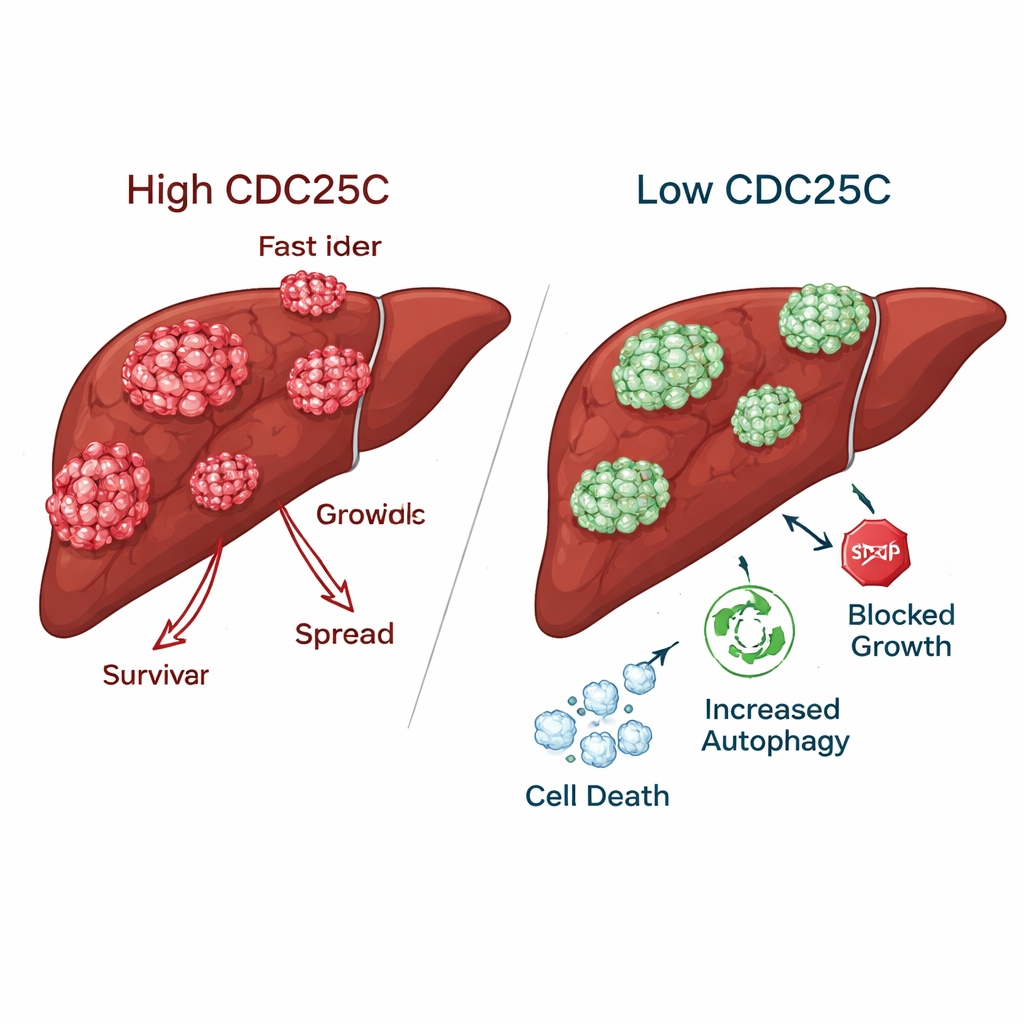
Ralentir le cancer tout en épargnant les cellules hépatiques saines
Lorsque CDC25C a été réduit dans les cellules cancéreuses hépatiques, les tumeurs ont perdu de nombreuses caractéristiques agressives. Les cellules cancéreuses formaient beaucoup moins de colonies, migraient plus lentement lors de tests de « cicatrisation » artificielle et étaient moins capables de traverser et d’envahir des barrières lors d’essais en laboratoire. En revanche, les cellules hépatiques normales ont montré une meilleure croissance et mobilité lorsque CDC25C était diminué, ce qui suggère que le tissu sain peut tolérer, voire bénéficier, d’une inhibition de CDC25C. Chez la souris, les tumeurs conçues pour réduire CDC25C présentaient des niveaux plus faibles de cette protéine tant aux niveaux génétique que protéique, confirmant que le même effet se produisait chez l’animal vivant.
Stress des centrales énergétiques et l’équipe de nettoyage de la cellule
En observant l’intérieur des cellules au microscope électronique, les chercheurs ont vu que les cellules cancéreuses avec un faible CDC25C contenaient des mitochondries gonflées et endommagées — les petites centrales énergétiques de la cellule — ainsi que des structures en forme de bulles appelées autophagosomes, qui signalent l’activation du système de recyclage interne de la cellule, l’autophagie. Ils ont ensuite mesuré des signes clés du stress mitochondrial : les niveaux de calcium et d’espèces réactives de l’oxygène (ROS), tous deux élevés dans les cellules cancéreuses après réduction de CDC25C. Des marqueurs de la réponse au stress mitochondrial, y compris des protéines d’assistance comme HSP60 et deux enzymes de « contrôle qualité » mitochondriales, ont également augmenté, tout comme CHOP, un facteur lié au stress qui relie les problèmes mitochondriaux à des réponses cellulaires plus larges. De façon frappante, ces signaux de stress évoluaient en sens inverse dans les cellules hépatiques normales, renforçant l’idée que les cellules cancéreuses et saines réagissent très différemment à la perte de CDC25C.
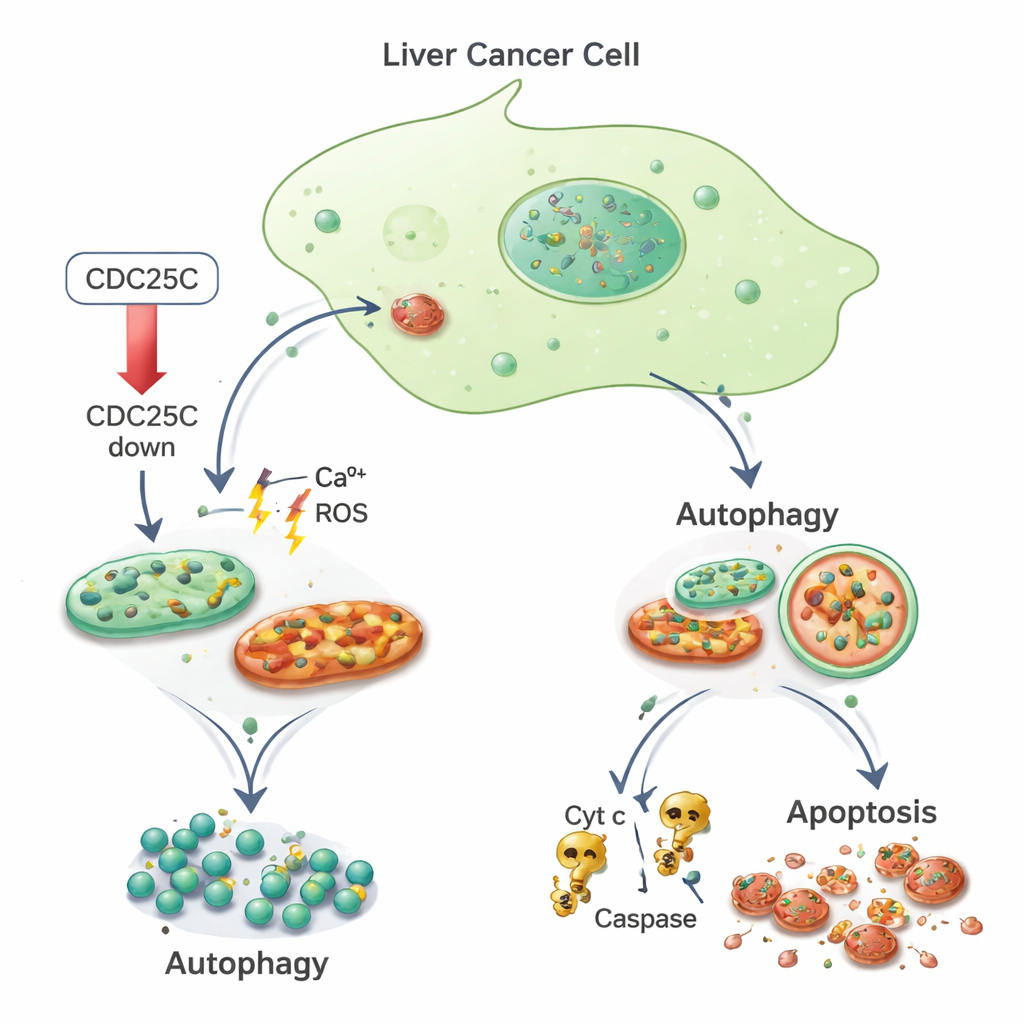
Du stress à l’autodigestion et à la mort cellulaire
L’équipe a ensuite cherché à savoir comment ces cellules cancéreuses stressées faisaient face à la situation. Ils ont constaté que les marqueurs de l’autophagie étaient augmentés chez les cellules cancéreuses et normales lorsque CDC25C était réduit. Des protéines telles que LC3 et p62, qui reflètent la formation et l’activité des autophagosomes, augmentaient, indiquant que les cellules renforçaient leur machinerie de nettoyage. Parallèlement, uniquement dans les cellules cancéreuses, les dommages mitochondriaux semblent pousser les cellules au-delà de la réparation et les conduire à la mort programmée. À l’aide de colorations fluorescentes et de cytométrie en flux, les chercheurs ont observé davantage de cellules cancéreuses présentant des noyaux fragmentés et fortement colorés — un signe distinctif de l’apoptose — et une diminution du potentiel de membrane mitochondrial. Ils ont également trouvé des niveaux accrus de cytochrome c et des enzymes Caspase-3 et Caspase-9, composants classiques de la voie de mort dirigée par les mitochondries. Les cellules hépatiques normales, par contraste, présentaient moins d’apoptose dans les mêmes conditions de réduction de CDC25C.
Ce que cela pourrait signifier pour les traitements futurs
Pour un lecteur non spécialiste, le message principal est que diminuer CDC25C semble atteindre les cellules du cancer du foie là où elles sont vulnérables : surcharge de leurs centrales énergétiques, mise en surchauffe de leurs systèmes de recyclage et déclenchement finalement d’une autodestruction propre — tout en épargnant majoritairement les cellules hépatiques normales. Les auteurs concluent que CDC25C est plus qu’un simple interrupteur de croissance ; il influence aussi la façon dont les cellules gèrent le stress, le nettoyage et la mort. Parce que les cellules cancéreuses dépendent fortement de CDC25C et répondent à sa perte par un stress mitochondrial et une apoptose fatals, des médicaments ciblant cette protéine, ou ses voies de stress en aval, pourraient un jour offrir une façon plus sélective de traiter le cancer du foie avec moins de dommages pour le tissu hépatique sain.
Citation: Miao, X., Zheng, F., Mo, X. et al. CDC25C downregulation suppresses HCC growth via mitochondrial stress-induced autophagy and apoptosis. Sci Rep 16, 5631 (2026). https://doi.org/10.1038/s41598-026-36351-2
Mots-clés: carcinome hépatocellulaire, CDC25C, stress mitochondrial, autophagie, apoptose