Clear Sky Science · fr
TET1 supprime la progression du carcinome hépatocellulaire en modulant les voies de signalisation PI3K/Akt
Pourquoi une enzyme hépatique compte pour le cancer
Le cancer primaire du foie, en particulier une forme appelée carcinome hépatocellulaire, est l’un des cancers les plus meurtriers au monde. De nombreux patients sont diagnostiqués trop tard pour une chirurgie curative, et les médicaments disponibles ne bénéficient qu’à une fraction d’entre eux. Cette étude explore une molécule nommée TET1, une enzyme qui modifie des marques chimiques sur l’ADN, pour poser une question simple mais essentielle : TET1 favorise‑t‑il la croissance des tumeurs hépatiques, et pourrait‑il devenir une nouvelle cible thérapeutique ?
Un éditeur caché dans notre ADN
Nos gènes sont régulés non seulement par le code ADN lui‑même, mais aussi par des marques chimiques qui activent ou répriment les gènes. Une marque courante est la méthylation de l’ADN, qui agit comme un variateur de l’activité génique. TET1 appartient à une famille d’enzymes qui effacent ou transforment ces marques, aidant les cellules à répondre à leur environnement et à maintenir une fonction normale. Quand ce système dysfonctionne, les cellules peuvent basculer vers des états pathologiques, y compris le cancer. Des travaux antérieurs ont montré que TET1 peut soit ralentir soit accélérer la croissance tumorale selon le tissu, mais son rôle exact dans le cancer hépatique humain restait incertain et largement débattu.
Les niveaux de TET1 augmentent dans les tumeurs hépatiques
Pour savoir ce que fait TET1 dans le cancer du foie, les chercheurs se sont d’abord tournés vers de larges bases de données publiques de gènes puis vers des échantillons de patients. Dans de nombreux types de cancer, les niveaux de TET1 étaient anormalement élevés dans plusieurs tumeurs, y compris le cancer du foie. En se concentrant sur les tumeurs hépatiques, ils ont comparé le tissu tumoral au foie non cancéreux adjacent chez les mêmes patients. Dans huit paires appariées, la protéine TET1 était systématiquement plus élevée dans la tumeur. Les jeux de données publics issus de centaines de patients ont raconté la même histoire au niveau de l’ARN : les cancers du foie présentaient plus de TET1 que les foies sains ou que les foies seulement cicatrisés. Les patients dont les tumeurs montraient des niveaux élevés de TET1 avaient tendance à présenter une maladie plus avancée et une survie globale et sans maladie plus courte, suggérant que TET1 est associé à l’agressivité tumorale et à un pronostic défavorable.
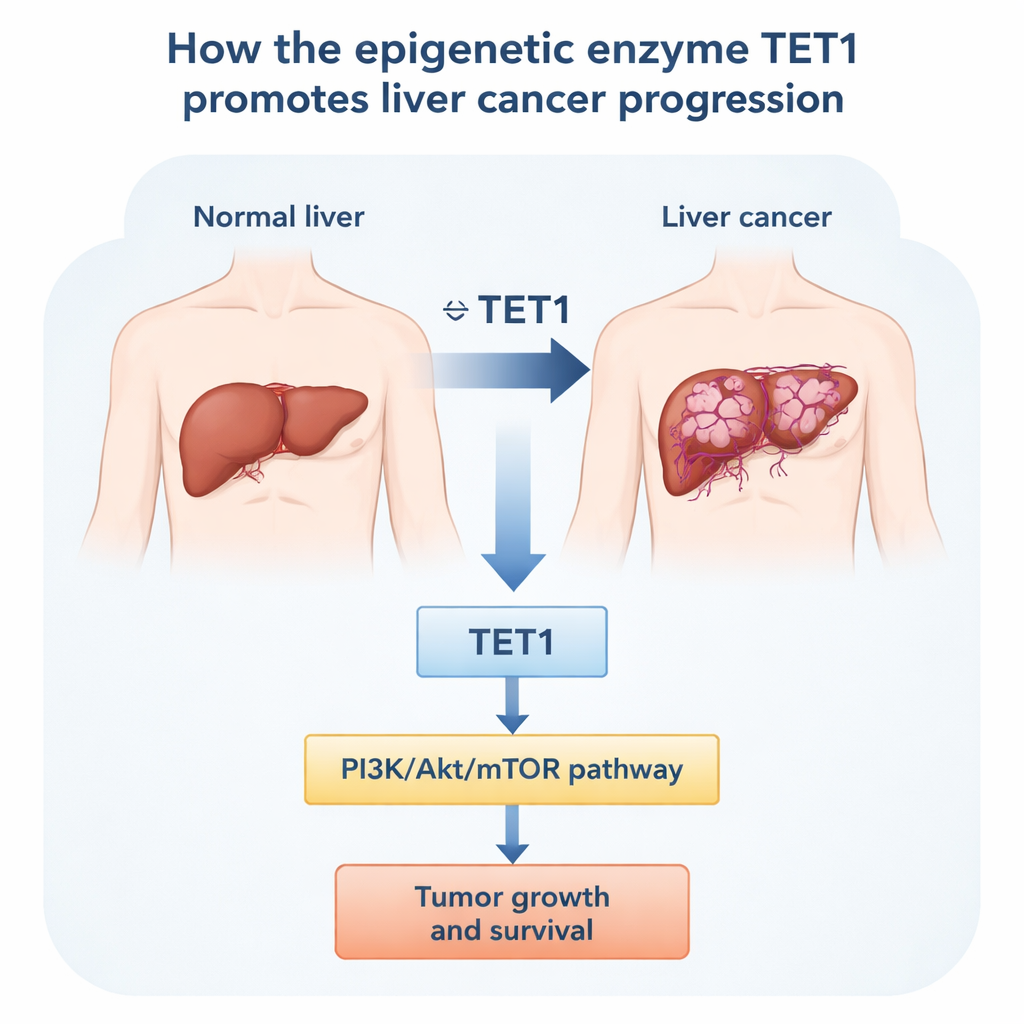
Réduire TET1 ralentit les cellules tumorales
Ensuite, l’équipe a cherché à savoir ce qui se passe lorsque TET1 est diminué dans des cellules de cancer du foie cultivées en laboratoire. En utilisant de petits ARN pour silencier le gène TET1, ils ont fortement réduit les niveaux de TET1 dans plusieurs lignées cellulaires humaines de carcinome hépatocellulaire, y compris des lignées porteuses de modifications liées au virus de l’hépatite B. Une fois TET1 supprimé, les cellules se divisaient plus lentement, formaient moins de colonies et montraient des signes clairs de stress. Des expériences de cytométrie en flux ont révélé qu’un plus grand nombre de cellules étaient bloquées en phase précoce « G1 » du cycle cellulaire, plutôt que d’avancer vers la division. Parallèlement, la proportion de cellules subissant la mort cellulaire programmée, l’apoptose, a fortement augmenté. Ces effets sont apparus tant dans des cellules hépatiques cancéreuses classiques que dans une lignée HBV‑positive, indiquant que TET1 contribue au maintien de la survie et de la croissance continue dans différents contextes du cancer du foie.
Une voie de croissance sous le contrôle de TET1
Pour comprendre comment TET1 exerce cette influence, les chercheurs ont profilé les gènes qui variaient entre les cellules hépatiques normales et les cellules tumorales. Des milliers de gènes étaient différents, et beaucoup d’entre eux se regroupaient dans des circuits bien connus de croissance et de survie. Une voie a particulièrement émergé : PI3K/Akt/mTOR, une chaîne de signalisation centrale que de nombreux cancers utilisent pour renforcer le métabolisme, résister à la mort cellulaire et se prémunir contre les thérapies. Les analyses de bases de données ont montré que les niveaux de TET1 augmentaient en parallèle avec des composants clés de cette voie, et diminuaient en opposition à PTEN, un frein naturel à l’activité PI3K/Akt. Lorsque TET1 était silencé dans des cellules de cancer du foie, les formes activées, « phosphorylées », de PI3K, Akt et surtout mTOR ont diminué. Le traitement des cellules par un inhibiteur chimique bloquant l’activité des enzymes de la famille TET réduisait également la phosphorylation d’Akt et de mTOR. Ces résultats suggèrent que l’activité enzymatique de TET1 — sa capacité à remodeler les marques de l’ADN — alimente la cascade PI3K/Akt/mTOR, faisant pencher la balance en faveur de la croissance et de la survie plutôt que du freinage.
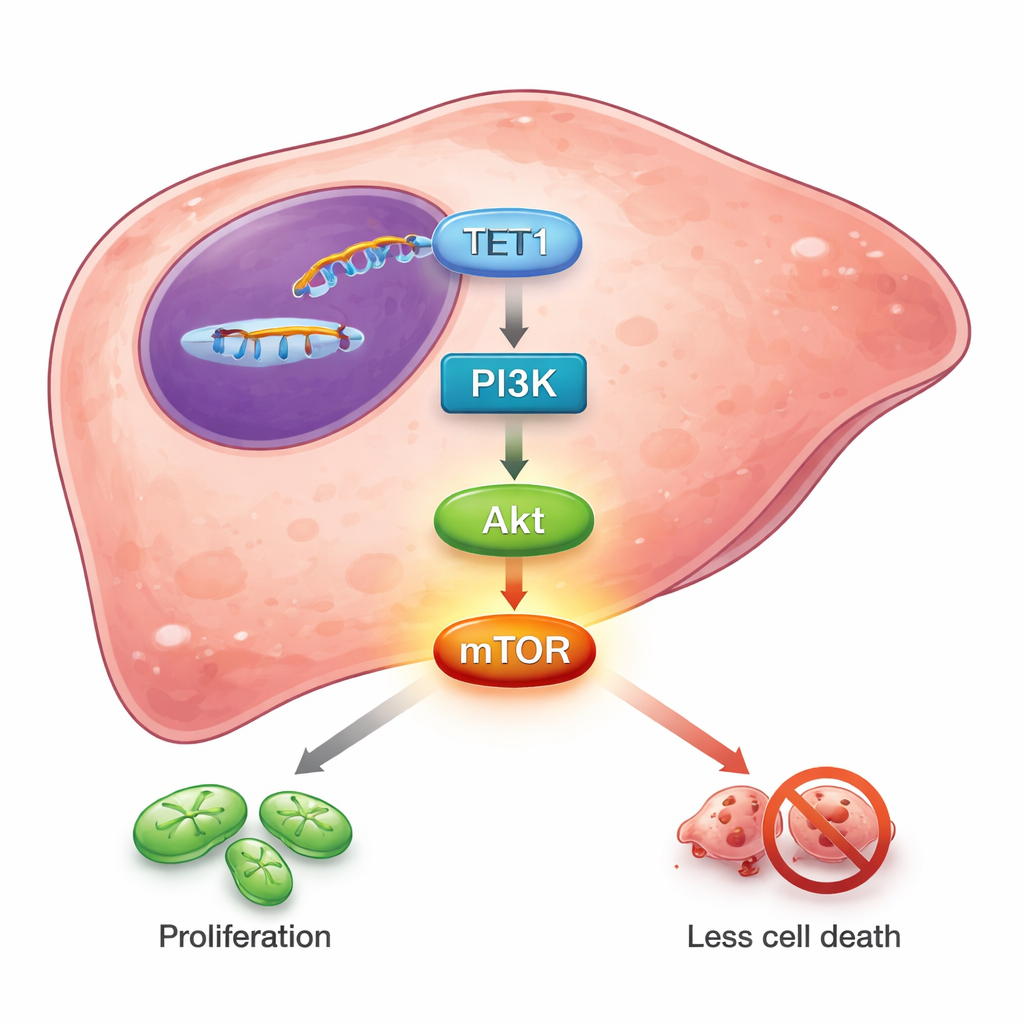
Du renseignement moléculaire à des traitements possibles
Dans l’ensemble, ce travail présente TET1 comme un allié important des tumeurs hépatiques plutôt que comme un gardien contre elles. Un TET1 élevé aide les cellules du cancer du foie à proliférer et à éviter la mort, en partie en maintenant la voie PI3K/Akt/mTOR activée. Chez les patients, une plus grande expression de TET1 dans les tumeurs s’associe à une maladie plus avancée et à de moins bons résultats. Pour un lecteur non spécialiste, le message est le suivant : une enzyme qui modifie discrètement des marques chimiques sur l’ADN peut fortement influencer la survie des cellules cancéreuses hépatiques. En concevant des médicaments qui inhibent TET1, ou en associant de tels médicaments aux traitements ciblant déjà PI3K/Akt, les thérapies futures pourraient couper une ligne de soutien cruciale aux tumeurs hépatiques et améliorer la survie des personnes atteintes de cette maladie difficile.
Citation: Qi, S., Chen, M., Ding, Z. et al. TET1 suppresses hepatocellular carcinoma progression by modulating the PI3K/Akt signaling pathways. Sci Rep 16, 5791 (2026). https://doi.org/10.1038/s41598-026-36334-3
Mots-clés: cancer du foie, TET1, épigénétique, PI3K Akt mTOR, carcinome hépatocellulaire