Clear Sky Science · fr
Le microbiome fécal prédit la réponse au traitement après l’initiation de la prise de sémaglutide ou d’empagliflozine
Pourquoi vos bactéries intestinales peuvent influencer le traitement du diabète
Les personnes atteintes de diabète de type 2 reçoivent de plus en plus de nouveaux médicaments comme le sémaglutide (souvent connu grâce aux publicités pour la perte de poids) et l’empagliflozine, qui aident à faire baisser la glycémie et le poids corporel. Pourtant, tout le monde ne répond pas de la même façon. Cette étude pose une question simple mais puissante : les billions de bactéries vivant dans notre intestin peuvent‑ils expliquer qui profite le plus de ces médicaments, et pourraient‑ils un jour orienter une prise en charge du diabète plus personnalisée ?
Ce que l’étude a mesuré
Les chercheurs ont suivi 20 adultes atteints de diabète de type 2 qui prenaient déjà le traitement standard metformine et souffraient d’obésité. Leurs médecins ont ajouté soit le sémaglutide soit l’empagliflozine selon les besoins cliniques. Pendant une année complète, les participants ont fourni quatre échantillons de selles et trois prélèvements sanguins et urinaires. Les échantillons de selles ont servi à profiler le microbiote intestinal, tandis que les analyses sanguines et urinaires ont suivi des marqueurs de santé clés tels que la glycémie à long terme (HbA1c), le poids corporel, la fonction rénale et des signes d’inflammation. Ce protocole a permis à l’équipe d’évaluer à la fois l’effet des médicaments sur la santé et la capacité du microbiome initial à prévoir ces changements. 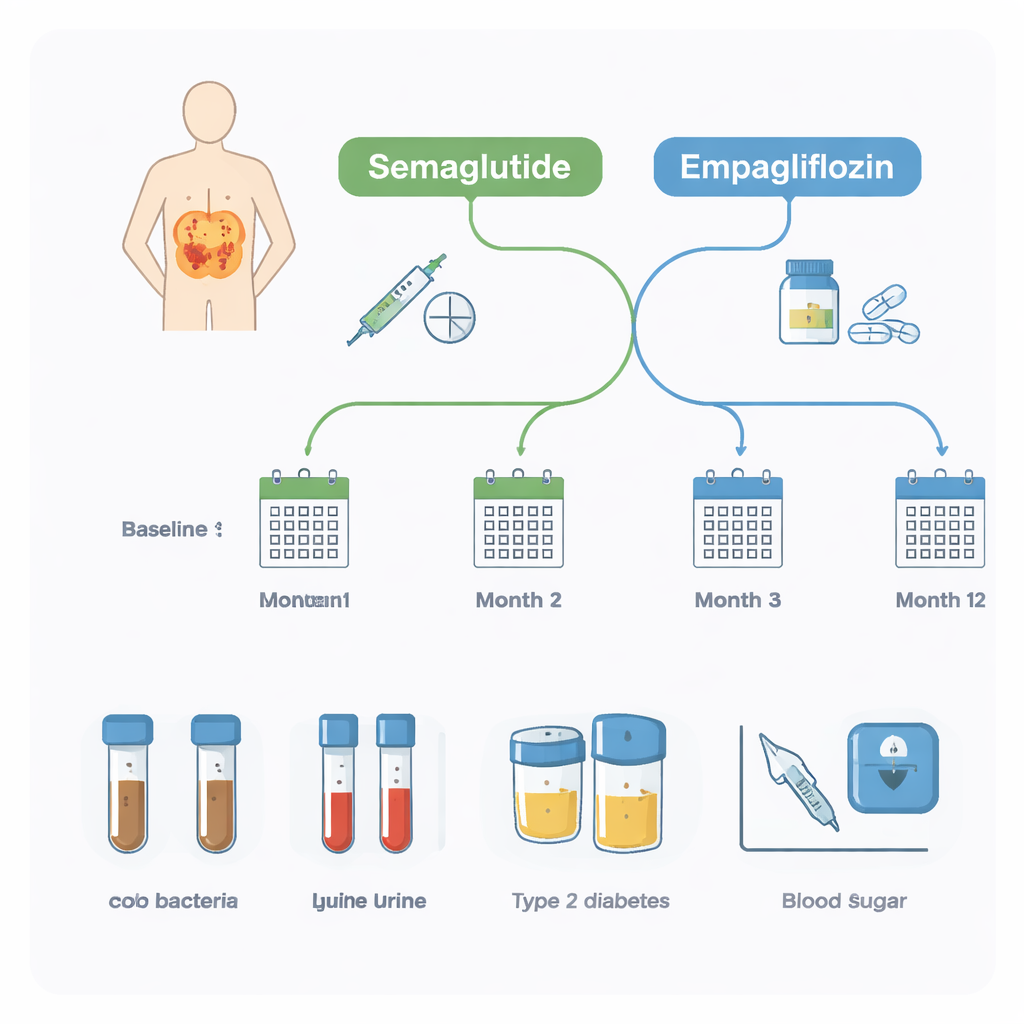
Effets des médicaments sur la santé et les communautés microbiennes
Sur le plan clinique, les deux médicaments ont amélioré le contrôle glycémique dès le troisième mois de traitement, et le sémaglutide a en particulier entraîné une perte de poids marquée et soutenue sur 12 mois. Lorsqu’ils ont examiné la diversité bactérienne intestinale – le nombre d’espèces différentes présentes et leur répartition – ils n’ont constaté aucun changement net évident après le début de l’un ou l’autre traitement. De même, en regardant les schémas généraux des groupes bactériens présents, la plupart des changements apparents n’ont pas tenu statistiquement une fois appliquées des corrections strictes pour tests multiples. Certains groupes bactériens et voies métaboliques prédites semblaient varier entre les mois 3 et 12, mais ces tendances étaient modestes et reflétaient probablement des effets indirects d’un meilleur métabolisme ou d’un changement de mode de vie plutôt qu’un impact direct des médicaments eux‑mêmes.
Le microbiote comme prédicteur potentiel de succès
Les résultats les plus intrigants proviennent de l’analyse du microbiome avant le traitement et de la question de savoir s’il pouvait prédire qui s’améliorerait le plus. Pour les personnes sous sémaglutide, des centaines de caractéristiques microbiennes de base montraient des liens nominaux avec des changements ultérieurs des marqueurs cliniques, en particulier le nombre de globules blancs et une mesure de l’inflammation connue sous le nom de rapport neutrophiles/lymphocytes. Après un filtrage statistique strict, un groupe bactérien appelé Alistipes est resté significativement associé : les individus ayant une plus grande abondance de cette bactérie au départ avaient tendance à montrer une plus forte baisse des cellules inflammatoires. Plusieurs genres bactériens et voies microbiennes à l’inclusion étaient également corrélés à la diminution de l’HbA1c au troisième mois, suggérant que la communauté intestinale initiale pourrait influencer l’ampleur de la réduction de la glycémie induite par le sémaglutide. Dans le groupe empagliflozine, de nombreuses bactéries et voies étaient aussi liées aux variations d’HbA1c et aux mesures de la fonction rénale, mais aucune n’a tenu aux tests statistiques les plus conservateurs, en partie parce que l’étude était de petite taille.
Ce que les résultats signifient – et ce qu’ils ne signifient pas
Il est important de noter que ce travail ne prétend pas que le sémaglutide ou l’empagliflozine remodelent radicalement le microbiome intestinal à eux seuls, ni qu’une bactérie spécifique garantisse le succès ou l’échec d’un traitement. Il suggère plutôt que des caractéristiques subtiles du microbiote existant d’une personne peuvent être liées à la façon dont son organisme réagit – non seulement en termes de glycémie, mais aussi d’inflammation et d’autres marqueurs de santé. Parce que tous les participants prenaient déjà de la metformine, qui influence elle‑même le microbiote, l’effet additionnel des nouveaux médicaments a pu être plus difficile à détecter. La taille d’échantillon modeste et certains prélèvements manquants limitent par ailleurs la confiance avec laquelle on peut identifier des groupes bactériens individuels comme de véritables moteurs de la réponse au traitement.
Perspectives pour une prise en charge du diabète sur mesure
Pour le grand public, la conclusion est que vos bactéries intestinales pourraient un jour aider les médecins à choisir le médicament antidiabétique le plus adapté. Dans cette étude exploratoire, la composition microbienne des échantillons de selles prélevés avant le traitement était liée à l’intensité des améliorations de la glycémie et de l’inflammation sous sémaglutide et empagliflozine, tandis que les médicaments eux‑mêmes n’ont provoqué que des modifications subtiles et lentes des communautés intestinales. Des études plus larges et plus longues seront nécessaires pour confirmer quelles bactéries importent réellement et si les modifier peut renforcer l’efficacité des traitements. Si ces efforts réussissent, un simple test de selles pourrait devenir partie intégrante d’une médecine personnalisée du diabète, aidant à associer le bon médicament au bon microbiome. 
Citation: Klemets, A., Reppo, I., Krigul, K.L. et al. Fecal microbiome predicts treatment response after the initiation of semaglutide or empagliflozin uptake. Sci Rep 16, 6126 (2026). https://doi.org/10.1038/s41598-026-36318-3
Mots-clés: microbiome intestinal, diabète de type 2, sémaglutide, empagliflozine, médecine personnalisée