Clear Sky Science · fr
Surmonter la résistance médicamenteuse du biofilm de Candida albicans grâce à la synergie azole–sophorolipide
Pourquoi les infections fongiques tenaces comptent
Toute personne ayant eu une candidose persistante, un cathéter central à l’hôpital ou un implant médical est potentiellement exposée à Candida albicans, un champignon courant qui peut devenir dangereux lorsqu’il forme des communautés difficiles à traiter appelées biofilms. Ces couches visqueuses protègent les microbes contre nombre de nos meilleurs antifongiques, permettant aux infections de persister et parfois de devenir menaçantes pour la vie. L’étude décrite ici cherche une nouvelle façon de percer ces défenses en associant des médicaments existants à une molécule naturelle à propriétés savonneuses produite par des levures.
Un bouclier caché sur les surfaces médicales
Candida albicans peut adhérer aux tissus et aux dispositifs médicaux puis se développer en biofilms structurés — des couches denses de cellules maintenues par une matrice auto-produite de sucres, de protéines et d’ADN. À l’intérieur de cette forteresse, le champignon ralentit son métabolisme et expulse les médicaments, si bien que les traitements qui tuent facilement les cellules libres ont peu d’effet sur celles qui vivent dans le biofilm. Les azolés comme le fluconazole et l’itraconazole sont des piliers de la thérapie antifongique, mais face à des biofilms mûrs ils nécessitent souvent des doses beaucoup plus élevées, ce qui peut provoquer des effets indésirables et échouer à éliminer complètement l’infection. Les cliniciens sont de plus en plus confrontés à des infections à la fois liées aux biofilms et résistantes, ce qui souligne le besoin de molécules d’appoint capables d’affaiblir le biofilm lui‑même.
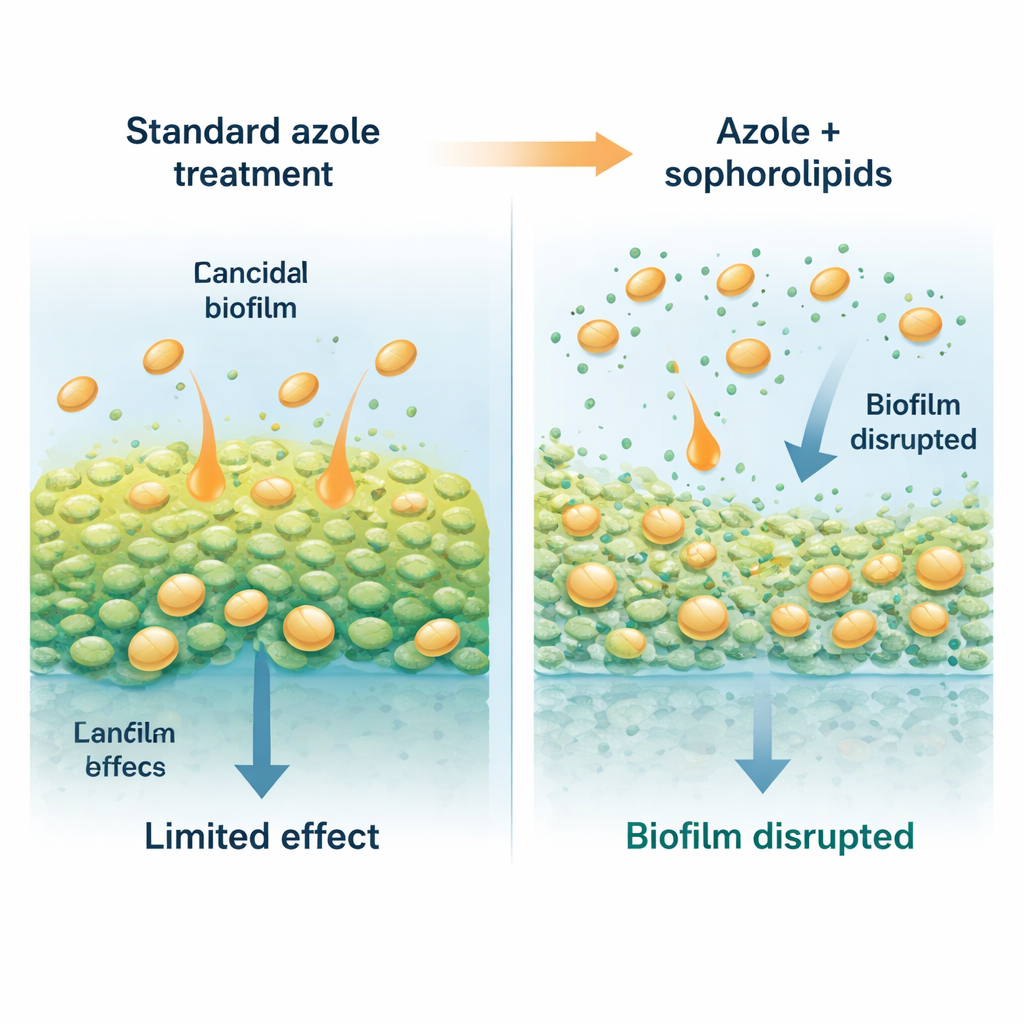
Aides savonneuses provenant d’une levure inoffensive
Les chercheurs se sont intéressés aux sophorolipides, des tensioactifs naturels biodégradables — des molécules qui se comportent un peu comme des détergents très doux — produites par certaines levures non pathogènes. Ces molécules ont une tête sucrée hydrophile et une queue huileuse, leur permettant de se positionner aux surfaces et aux interfaces. Dans cette étude, une levure nommée Starmerella riodocensis a été utilisée pour produire un mélange de sophorolipides, qui a ensuite été purifié et analysé. Pris isolément, ces sophorolipides ne tuaient pas les cellules de Candida en suspension, même à fortes concentrations, mais ils interféraient fortement avec la capacité du champignon à former et maintenir des biofilms. Les biofilms jeunes, en formation, étaient particulièrement sensibles, et même les biofilms établis depuis 24 heures pouvaient être éclaircis et affaiblis après exposition à des sophorolipides purifiés.
Associer les antifongiques existants
La question centrale était de savoir si les sophorolipides pouvaient améliorer l’efficacité des azolés classiques. L’équipe a testé des combinaisons de sophorolipides avec trois azolés largement utilisés : le fluconazole, l’itraconazole et le kétoconazole. Lorsqu’ils ont exposé des biofilms à ces mélanges, ils ont constaté que certains appariements faisaient plus que simplement additionner leurs effets — ils agissaient en synergie, c’est‑à‑dire que le couple était plus puissant que ce que l’on attendrait de chaque composant pris séparément. Le partenariat le plus remarquable était l’itraconazole associé aux sophorolipides. Contre des biofilms tenaces préformés, la quantité d’itraconazole nécessaire pour réduire le biofilm de moitié a chuté jusqu’à seize fois, tandis que la dose requise de sophorolipides diminuait elle aussi de plusieurs fois par rapport à l’utilisation des sophorolipides seuls. Les combinaisons avec le fluconazole et le kétoconazole ont montré des gains plus modestes, suggérant que la nature chimique de chaque médicament influence la façon dont il bénéficie de l’« aide » du tensioactif.
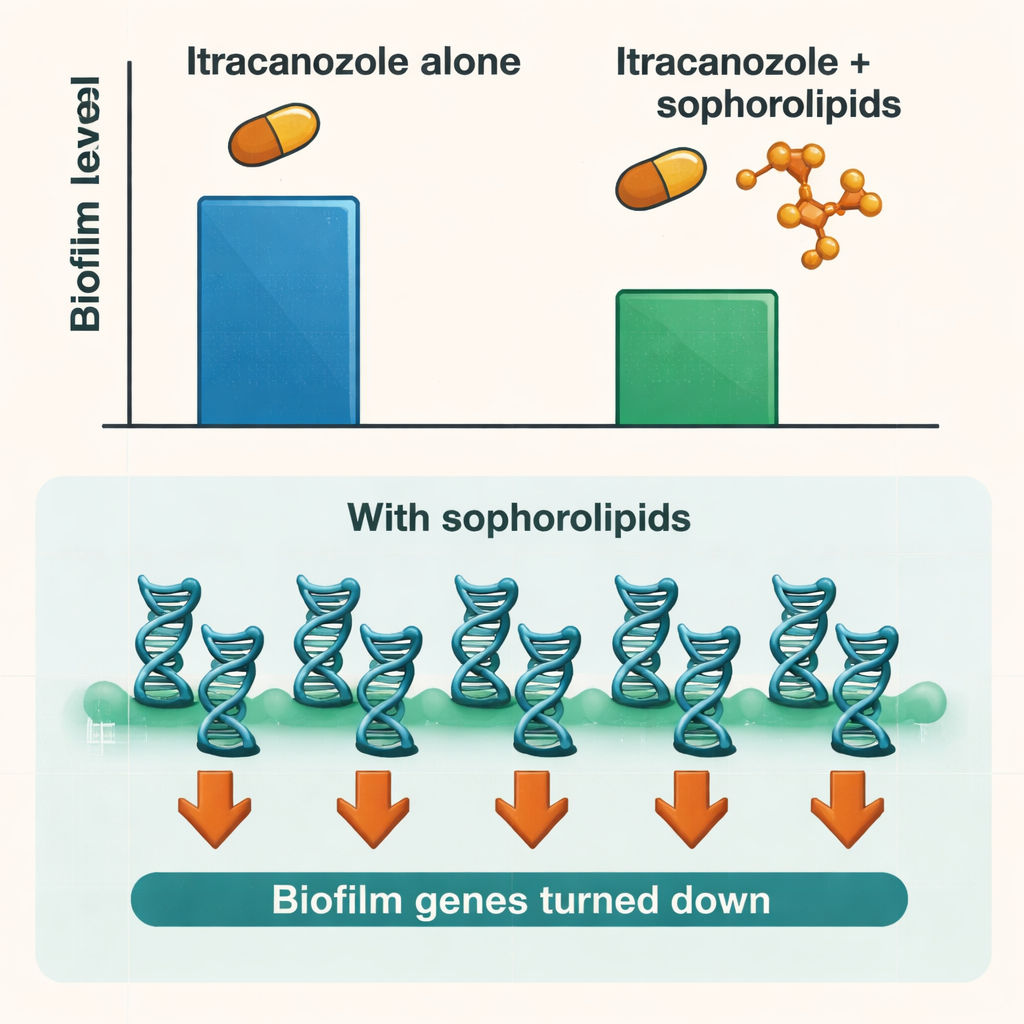
Éteindre le programme du biofilm chez le champignon
Pour comprendre ce qui se passait à l’intérieur des cellules fongiques, les chercheurs ont examiné l’activité de gènes clés de Candida impliqués dans l’adhérence aux surfaces, la croissance sous forme filamenteuse et la construction de la matrice du biofilm. Le traitement par les sophorolipides seuls a réduit l’expression de nombreux de ces gènes, en particulier ceux qui contrôlent les premières étapes de l’adhésion et le passage de formes ressemblant à des levures à des formes filamenteuses. Lorsque les cellules étaient synchronisées à un stade spécifique du cycle cellulaire qui favorise la formation de biofilm, les effets d’inhibition génique étaient encore plus forts. Cela suggère que les sophorolipides ne se contentent pas de déloger le biofilm ; ils perturbent aussi le programme biologique du champignon pour construire et maintenir sa communauté protectrice.
Promesse de traitements plus doux et plus efficaces
L’étude conclut que les sophorolipides issus de Starmerella riodocensis peuvent agir comme partenaires sûrs ciblant les biofilms pour les azolés, la combinaison itraconazole–sophorolipide étant particulièrement puissante. Parce que les sophorolipides présentent une faible toxicité sur les cellules de mammifères et affaiblissent principalement la structure du biofilm et les réseaux géniques plutôt que de tuer directement le champignon, ils pourraient permettre aux médecins d’utiliser des doses plus faibles de médicaments conventionnels tout en éliminant les infections tenaces sur dispositifs et tissus. Pour les patients, ce type de thérapie combinée intelligente pourrait un jour se traduire par des traitements à la fois plus efficaces contre les biofilms résistants de Candida et plus respectueux du reste de l’organisme.
Citation: Jayasekara, L.C.B., Watchaputi, K., Butkinaree, C. et al. Overcoming Candida albicans biofilm drug resistance via azole-sophorolipid synergy. Sci Rep 16, 5963 (2026). https://doi.org/10.1038/s41598-026-36278-8
Mots-clés: biofilm de Candida, antifongiques azolés, sophorolipides, synergie médicamenteuse, résistance antimicrobienne