Clear Sky Science · fr
Repositionnement du dapagliflozine via des nanogels polymériques pour le traitement du cancer colorectal
Pourquoi un médicament contre le diabète pourrait aider à combattre le cancer du côlon
Le cancer colorectal est l’une des principales causes de décès liés au cancer dans le monde, et de nombreux patients rechutent malgré la chirurgie et la chimiothérapie. Cette étude explore un allié inattendu contre cette maladie : le dapagliflozine, un comprimé courant pour le diabète de type 2. En emballant ce médicament dans de minuscules particules molles qui se transforment en un gel doux dans l’estomac, les chercheurs visent à délivrer une plus grande quantité au gros intestin — où se développent les tumeurs colorectales — tout en conservant une dose orale comparable à celle des comprimés existants.
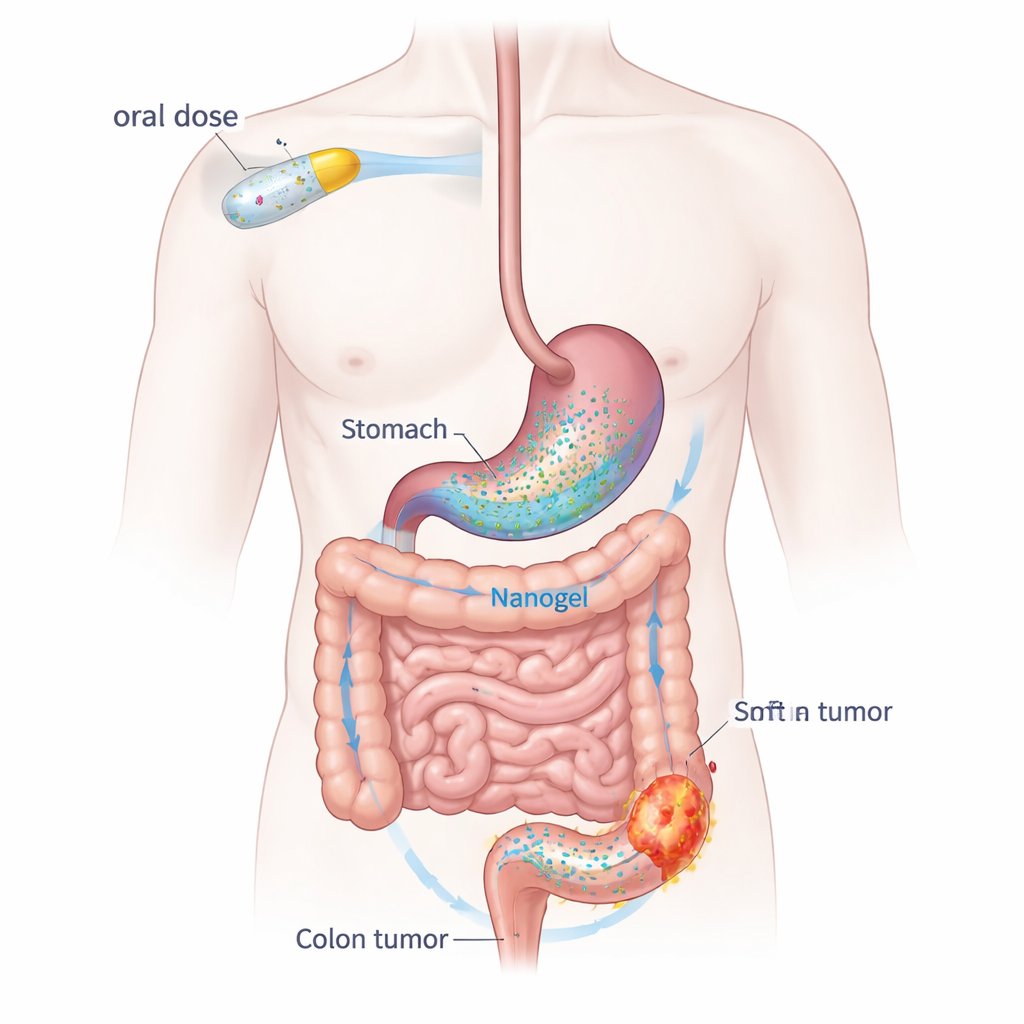
Transformer un comprimé courant en une charge ciblant le cancer
Le dapagliflozine agit normalement au niveau des reins pour abaisser la glycémie, mais il calme aussi l’inflammation et ralentit la prolifération cellulaire — deux processus dont les cancers dépendent. Pris seul, toutefois, le médicament se dissout mal dans l’eau et est éliminé rapidement de l’organisme. Pour surmonter ces limitations, l’équipe a construit un système d’administration « nanogel » utilisant deux polymères proches d’ingrédients alimentaires : l’alginate de sodium, extrait d’algues, et le polyvinylalcool, un épaississant biocompatible largement utilisé. Le médicament est piégé à l’intérieur de nanoparticules d’environ un dix-millième de millimètre de largeur. Quand ces particules rencontrent l’acide gastrique, elles se déposent et s’assemblent en une masse hydrogel douce qui persiste, puis libère progressivement le médicament au fur et à mesure de son trajet vers le côlon.
Rendre le médicament plus soluble et moins rapidement éliminé
Les scientifiques ont d’abord optimisé la fabrication des particules, ajustant le rapport des deux polymères pour que les nanoparticules restent petites, de taille homogène et stables en milieu liquide. Ils ont confirmé que le médicament était bien intégré dans la matrice polymérique et partiellement transformé d’une forme cristalline vers une forme plus amorphe, qui se dissout généralement mieux. Dans des liquides tests imitant les fluides gastrique et intestinaux, la formulation en nanogel a augmenté la solubilité apparente du dapagliflozine d’environ 1,7–1,8 fois par rapport au médicament brut. Lorsqu’ils ont suivi la vitesse de libération, le nanogel a montré un profil de « libération lente » sur plusieurs heures, plutôt que l’éclair de libération rapide observé avec le médicament simple. Une recette particulière, nommée F2, a formé un gel compact et durable qui est resté cohérent pendant au moins deux heures en conditions acides tout en libérant régulièrement le médicament.
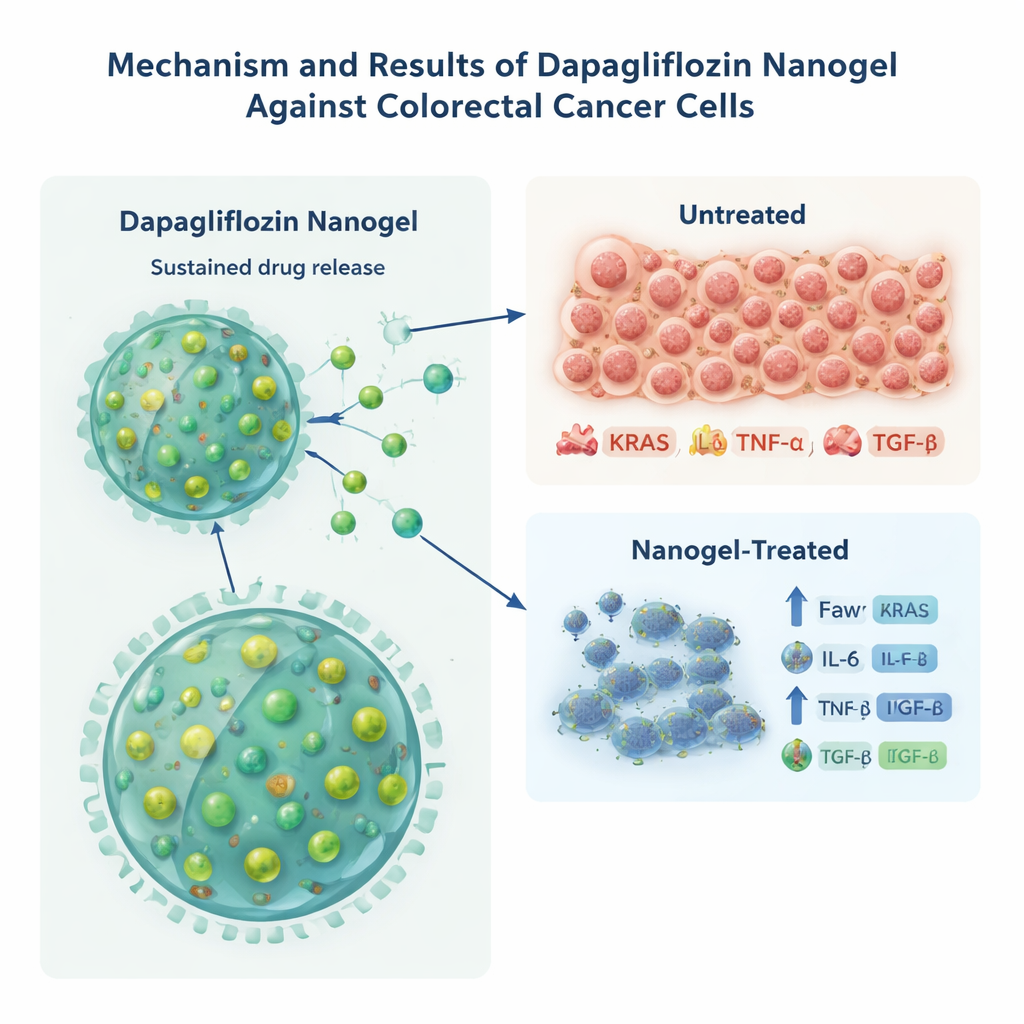
Soumettre les cellules cancéreuses à un stress en laboratoire
Pour évaluer si cette nouvelle forme de dapagliflozine pouvait réellement nuire aux cellules cancéreuses, l’équipe l’a testée sur des cellules de cancer colorectal HCT-116 cultivées en boîte de Pétri. Comparée à la même quantité de médicament libre, la version en nanogel a tué les cellules cancéreuses à des concentrations plus faibles, réduisant la dose nécessaire pour diminuer de moitié la croissance cellulaire d’environ un tiers. Les chercheurs ont ensuite examiné des molécules associées à un comportement tumoral agressif et à l’inflammation chronique, notamment KRAS (une protéine clé promotrice de cancer) et les protéines de signalisation IL-6, TNF-α et TGF-β. Les cellules traitées par le nanogel chargé ont montré des niveaux bien plus faibles de tous ces marqueurs que les cellules traitées par le médicament libre ou par des particules vides, ce qui suggère qu’une exposition soutenue via les nanoparticules réduisait plus efficacement les signaux liés au cancer et à l’inflammation. Comme la lignée cellulaire porte déjà une mutation fixe de KRAS, les auteurs soulignent que cette diminution de la protéine KRAS pourrait refléter des réponses au stress plutôt qu’une correction génétique directe, mais elle appuie néanmoins un impact biologique marqué.
Modifier la façon dont l’organisme gère le médicament
L’équipe est ensuite passée aux études animales, administrant à des rats soit une suspension simple de poudre de dapagliflozine, soit le nanogel optimisé, tous deux par voie orale à dose identique. Dans le groupe nanogel, les concentrations maximales du médicament dans le sang sont apparues plus tard et étaient plus faibles, mais le médicament est resté en circulation plus longtemps. L’exposition globale (mesurée comme aire sous la courbe) a augmenté modestement d’environ 7 %, et la demi-vie apparente a été à peu près doublée. Ces changements signifient que l’organisme perçoit une dose plus lisse et plus étendue dans le temps, au lieu d’un pic net suivi d’une chute rapide. Ce comportement correspond à ce que les chercheurs ont conçu pour le gel : retenir le médicament dans l’intestin, le libérer lentement et, potentiellement, maintenir des niveaux plus élevés dans le bas de l’intestin et le côlon où apparaissent les tumeurs.
Ce que cela pourrait signifier pour les soins oncologiques futurs
Concrètement, cette étude prend un médicament antidiabétique bien connu et lui donne un « costume de livraison » afin qu’il atteigne mieux et reste à proximité des tumeurs colorectales. Le nanogel rend le médicament plus facile à dissoudre, ralentit sa fuite hors de l’intestin et semble augmenter sa toxicité pour les cellules de cancer colorectal tout en réduisant des signaux clés d’inflammation et de prolifération. Chez le rat, il prolonge en douceur la présence du médicament dans la circulation sans augmenter de façon spectaculaire la dose totale. Le travail en est encore à un stade précoce — limité à une seule lignée cellulaire et à des tests animaux de courte durée — et n’a pas encore démontré une régression tumorale directe chez des animaux vivants ou des humains. Néanmoins, il établit une base détaillée pour le repositionnement du dapagliflozine comme composant potentiel des traitements futurs du cancer colorectal, en utilisant des nanogels oraux intelligents pour transformer un comprimé familier en un outil anticancéreux plus ciblé.
Citation: Abdullah, S., Thiab, S., Altamimi, A.A. et al. A repurposing Dapagliflozin via polymeric nanogels for colorectal cancer therapy. Sci Rep 16, 5625 (2026). https://doi.org/10.1038/s41598-026-36232-8
Mots-clés: cancer colorectal, repositionnement de médicament, nanoparticules, administration orale de médicaments, dapagliflozine