Clear Sky Science · fr
Surveillance génomique nationale des isolats de Klebsiella pneumoniae résistants aux carbapénèmes et à la colistine issus d’hémocultures en Thaïlande (2020–2024)
Augmentation des infections sanguines mortelles
Les hôpitaux du monde entier font face à une tendance inquiétante : des bactéries courantes qui cédaient autrefois à nos antibiotiques les plus puissants deviennent quasi impossibles à traiter. Cette étude se concentre sur Klebsiella pneumoniae, un microbe capable d’envahir la circulation sanguine et de provoquer des infections potentiellement mortelles, et retrace son évolution à travers la Thaïlande pour résister même aux traitements de dernier recours. Comprendre où ces super‑bactéries se propagent et comment elles contournent les médicaments est crucial pour protéger les patients, orienter les choix thérapeutiques des médecins et informer les politiques de santé publique.
Suivre un super‑germe hospitalier à l’échelle nationale
Les chercheurs ont analysé 227 échantillons de Klebsiella pneumoniae prélevés dans le sang de patients hospitalisés à travers la Thaïlande entre 2020 et 2024. Ces prélèvements proviennent d’un réseau national de surveillance qui collecte régulièrement des données sur les infections résistantes aux médicaments. Les tests de laboratoire ont montré que plus de 93 % de ces isolats sanguins étaient résistants aux carbapénèmes, une puissante classe d’antibiotiques souvent utilisée quand d’autres traitements échouent. Fait préoccupant, près d’un tiers des souches résistantes aux carbapénèmes résistaient également à la colistine, l’une des dernières options dont disposent les cliniciens lorsque tout le reste échoue. En associant les tests de sensibilité classiques au séquençage complet du génome, l’équipe a pu identifier non seulement quels médicaments échouaient, mais aussi quels procédés génétiques les bactéries utilisaient pour survivre.
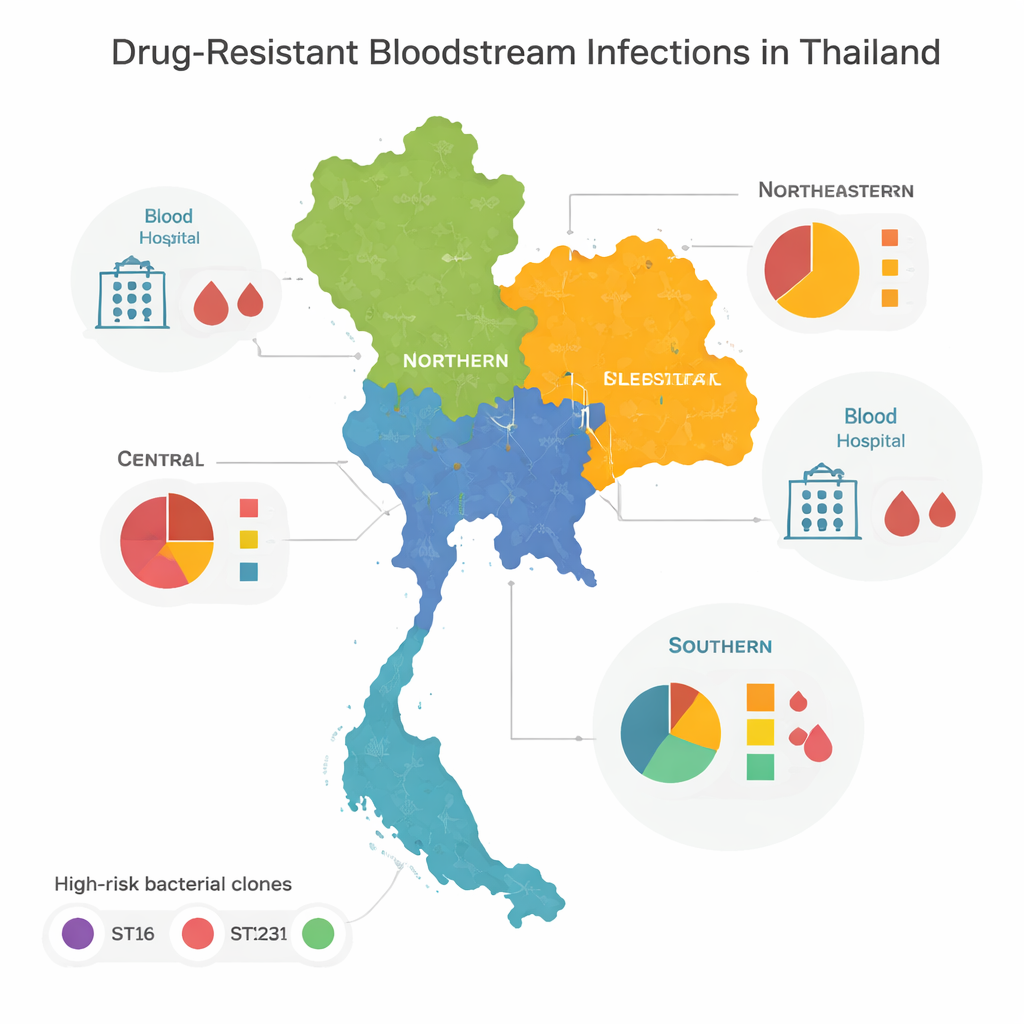
Clones à haut risque et répartitions régionales
En comparant les génomes, l’équipe a constaté que la plupart des bactéries résistantes appartenaient à quelques familles « à haut risque », ou clones, reconnues mondialement pour provoquer des flambées en milieu hospitalier. Trois d’entre elles — appelées ST16, ST147 et ST231 — dominaient respectivement le centre, le nord et le nord‑est de la Thaïlande. Ces clones se sont largement répandus entre les régions, ce qui suggère des déplacements fréquents de patients, de personnel ou des échanges bactériens entre établissements. Le sud du pays présentait un tableau différent : plutôt que d’être dominé par quelques types, il hébergeait une grande diversité de lignées bactériennes, souvent observées une seule fois. Cette diversité laisse penser à un mélange plus complexe d’éclosions locales, de sources environnementales et de mouvements transfrontaliers plutôt qu’à un ou deux clones en expansion incontrôlée.
Comment les bactéries déjouent les antibiotiques
L’étude a montré que ces bactéries accumulent plusieurs mécanismes de résistance. De nombreuses souches ST16 et ST231 portaient des gènes appelés blaNDM et blaOXA, qui produisent des enzymes détruisant les carbapénèmes avant qu’ils n’agissent. Certaines présentaient aussi des altérations de leur membrane externe réduisant l’entrée des médicaments, une combinaison conduisant à une résistance de très haut niveau. Les souches ST231 portaient souvent un gène additionnel, rmtF1, qui neutralise un groupe important d’antibiotiques, les aminosides, réduisant encore les options thérapeutiques. ST147 se distinguait par sa flexibilité génétique : elle recombinait différents gènes de résistance et plasmides — de petits anneaux d’ADN mobiles — ce qui en fait un vecteur potentiel de diffusion des traits de résistance vers d’autres bactéries.
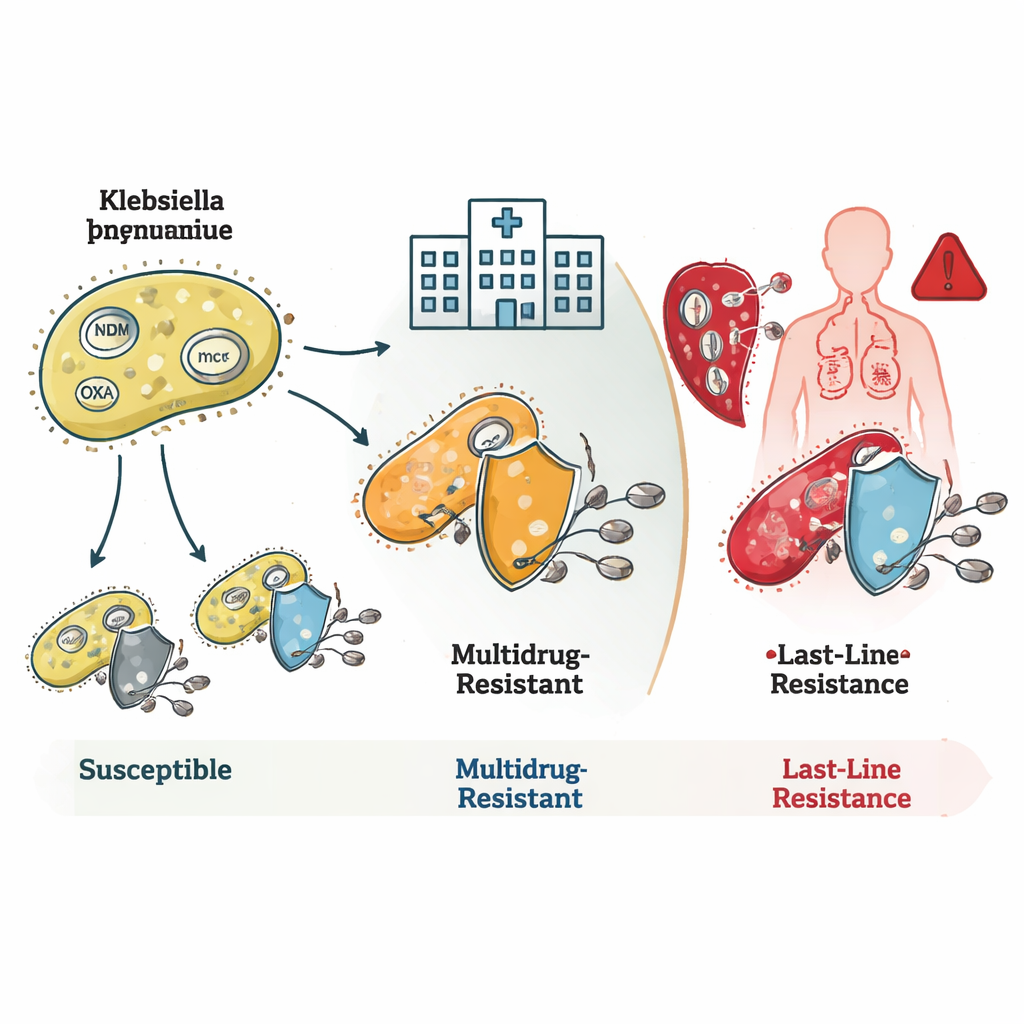
Échecs des traitements de dernier recours et dangers cachés
Le résultat le plus alarmant concernait la résistance à la colistine, un antibiotique réservé aux situations désespérées. Certaines familles bactériennes rares portaient des gènes mcr, qui peuvent sauter d’une espèce à l’autre via des plasmides et conférer directement la résistance à la colistine. D’autres, en particulier au sein du clone ST16, étaient résistantes à la colistine alors qu’elles n’avaient aucun marqueur connu de résistance ou mutation identifiée. Cela suggère que les mécanismes permettant de neutraliser ce traitement de dernier recours n’ont pas encore été entièrement cartographiés. L’équipe a également identifié des souches hypervirulentes — des bactéries particulièrement aptes à provoquer des maladies graves — dont une lignée combinant une forte virulence et une résistance à l’ensemble des carbapénèmes testés, un mélange particulièrement dangereux.
Pourquoi la surveillance génomique est essentielle
Pour relier les changements génétiques aux échecs thérapeutiques observés en laboratoire, les chercheurs ont utilisé des modèles statistiques liant des gènes de résistance précis aux résultats des tests. Des gènes tels que blaNDM‑1 et ses apparentés ont montré des associations très fortes avec la résistance aux carbapénèmes, confirmant leur rôle central dans l’échec des traitements. En revanche, pour la colistine, la plupart des bactéries résistantes ne présentaient aucun marqueur de résistance reconnu, indiquant l’existence de mécanismes cachés encore à découvrir. Les auteurs soutiennent que l’utilisation systématique du séquençage génomique complet dans la surveillance hospitalière peut fonctionner comme un radar d’alerte précoce, repérant les clones à haut risque émergents, suivant leur déplacement à travers régions et frontières, et guidant des réponses rapides de contrôle des infections.
Ce que cela signifie pour les patients et les politiques
Pour le grand public, le message est net : certaines infections sanguines en Thaïlande sont désormais causées par des bactéries résistantes à presque tous les antibiotiques disponibles, et quelques familles dangereuses de ces microbes se répandent largement. Dans le même temps, l’étude montre qu’avec les bons outils — échantillonnage national, analyses génétiques et partage rapide des données — les systèmes de santé peuvent anticiper ces menaces et s’adapter. Étendre la surveillance génomique, développer des tests moléculaires rapides et renforcer le contrôle des infections pourraient contribuer à ralentir la progression de ces super‑bactéries et gagner du temps pour mettre au point de nouveaux traitements et vaccins.
Citation: Krobanan, K., Kamjumphol, W., Leethongdee, P. et al. Nationwide genomic surveillance of carbapenem- and colistin-resistant Klebsiella pneumoniae bloodstream isolates in Thailand (2020–2024). Sci Rep 16, 5853 (2026). https://doi.org/10.1038/s41598-026-36228-4
Mots-clés: résistance aux antimicrobiens, Klebsiella pneumoniae, infection sanguine, surveillance génomique, soins de santé en Thaïlande