Clear Sky Science · fr
Nanoparticules cubosomales de lycopène : une nouvelle plate-forme pour améliorer les propriétés antioxydantes et anticancéreuses avec une étude de docking moléculaire
La puissance de la tomate dans un tout petit emballage
Beaucoup de gens savent que consommer des tomates peut aider à protéger contre le cancer, grâce à un pigment rouge appelé lycopène. Mais le lycopène seul est mal absorbé par l’organisme et n’atteint pas efficacement les tumeurs. Cette étude explore une solution ingénieuse : encapsuler le lycopène dans de très petites particules lipidiques appelées cubosomes pour vérifier si ce « concentré de tomate » peut mieux combattre des cellules de cancer du côlon en laboratoire.
Pourquoi le lycopène ordinaire montre ses limites
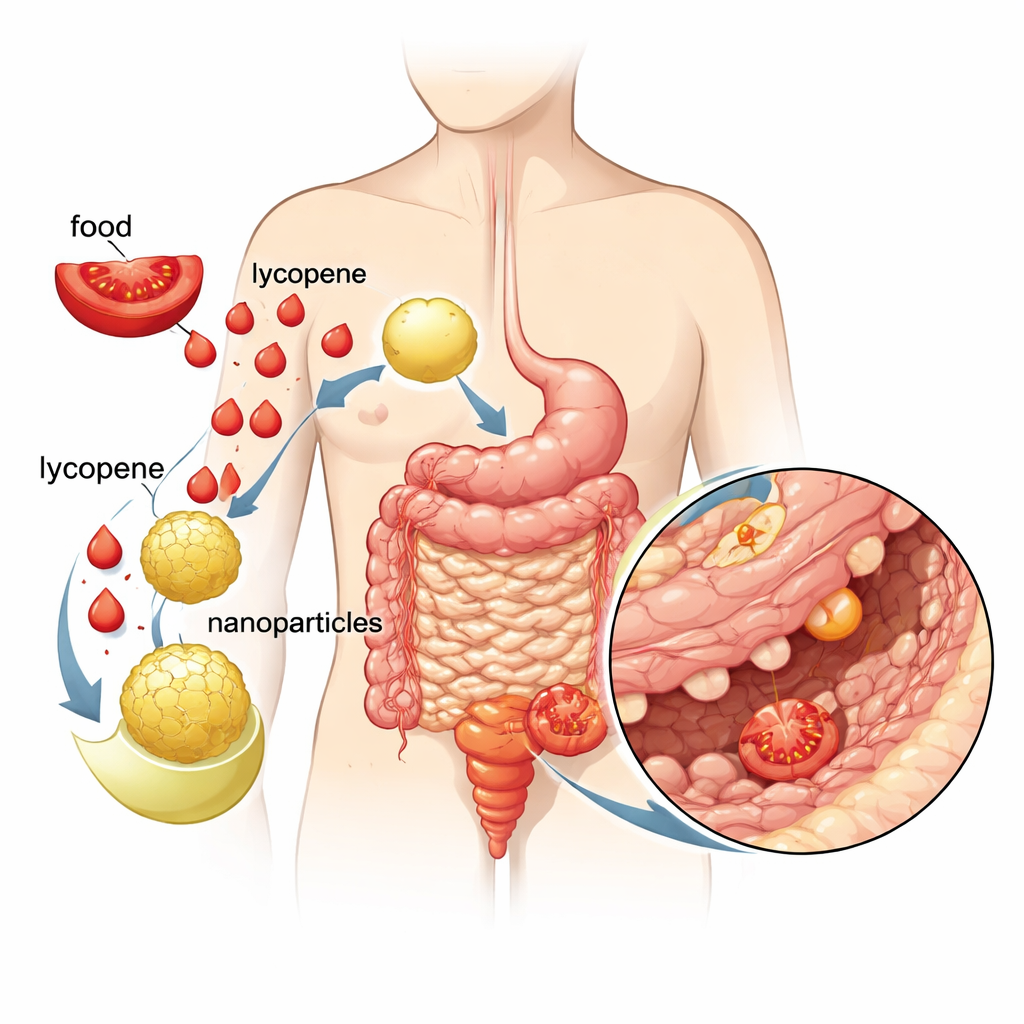
Le lycopène est un puissant antioxydant naturel présent dans les tomates, les pastèques et d’autres fruits rouges. Il peut neutraliser des molécules nocives appelées radicaux libres, qui endommagent l’ADN, les protéines et les lipides de nos cellules et favorisent des maladies chroniques comme le cancer et les maladies cardiaques. Cependant, le lycopène est extrêmement lipophile et se dissout mal dans les fluides à base d’eau, comme ceux de notre système digestif. Par conséquent, seule une petite fraction de ce que nous consommons parvient réellement dans le sang et aux tissus cibles. Cette faible solubilité et cette instabilité limitent l’intérêt thérapeutique du lycopène, malgré son potentiel protecteur bien documenté.
Concevoir un vecteur amélioré
Pour surmonter ces obstacles, les chercheurs ont créé des nanoparticules cubosomales — de minuscules particules souples fabriquées à partir de lipides biocompatibles et de stabilisants qui s’organisent en une structure intérieure spongieuse, en nid d’abeille. Ces structures peuvent piéger des molécules lipophiles comme le lycopène, les protéger de la dégradation et les libérer progressivement. Dans ce travail, l’équipe a chargé avec succès du lycopène dans des cubosomes d’environ 150 nanomètres de diamètre, la majeure partie du lycopène étant efficacement encapsulée. Les tests ont montré que plus des trois quarts du lycopène étaient libérés en solution en 15 minutes, une amélioration spectaculaire par rapport au lycopène seul, qui se dissout à peine dans l’eau.
Évaluer la puissance antioxydante et anticancéreuse
Les scientifiques ont ensuite comparé le lycopène libre et le lycopène en cubosomes de deux manières. D’abord, ils ont mesuré la capacité de chacun à neutraliser les radicaux libres à l’aide de tests antioxydants standard. Dans les deux tests, le lycopène nano‑emballé nécessitait des quantités bien plus faibles pour obtenir le même effet antioxydant, indiquant une activité nettement renforcée. Ensuite, ils ont exposé des cellules humaines de cancer du côlon (HT‑29) à l’une ou l’autre des formes. À l’aide d’un test de viabilité standard, ils ont constaté que le lycopène en cubosomes tuait les cellules cancéreuses plus efficacement que le lycopène libre, c’est‑à‑dire que des doses plus faibles suffisaient à réduire de moitié la croissance cellulaire. Des expériences par cytométrie en flux ont révélé que la forme nanoparticulaire poussait beaucoup plus de cellules dans une phase de repos où elles cessent de se diviser, et déclenchait une augmentation marquée de la mort cellulaire programmée (apoptose) par rapport aux cellules non traitées.
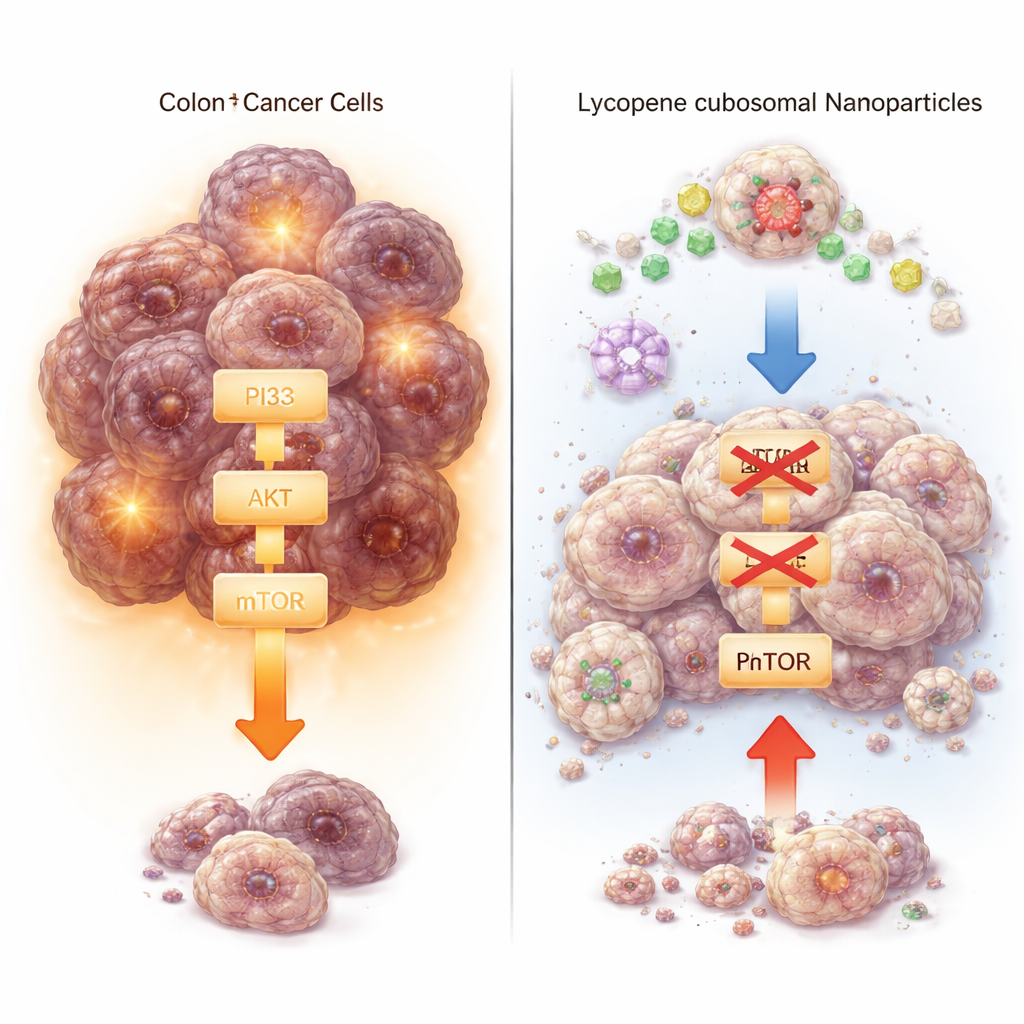
Un regard sur les circuits de contrôle intracellulaires
Au‑delà du simple comptage des cellules survivantes, l’équipe a examiné des interrupteurs moléculaires clés qui contrôlent la croissance et la mort. Ils se sont focalisés sur la voie PI3K–AKT–mTOR, une chaîne de signaux que les cellules cancéreuses utilisent souvent pour rester en vie et se multiplier, et sur des protéines qui favorisent ou empêchent le suicide cellulaire. À l’aide de tests d’expression génique et de mesures protéiques, ils ont constaté que le lycopène libre et les cubosomes de lycopène réduisaient l’expression de PI3K, AKT, mTOR et de la protéine de survie Bcl‑2, tout en augmentant l’enzyme exécutrice de la mort caspase‑3. Ces changements étaient systématiquement plus prononcés avec la forme cubosomale. Des simulations de docking informatique ont soutenu l’idée que le lycopène peut s’insérer dans le site actif de PI3K, suggérant un mécanisme direct par lequel il pourrait perturber cette voie de croissance.
Ce que cela pourrait signifier pour les traitements futurs
En résumé, encapsuler le lycopène dans des nanoparticules cubosomales a facilité sa dissolution, amélioré sa stabilité et rendu la molécule bien plus puissante dans les tests en laboratoire. La forme nano n’a pas seulement neutralisé plus efficacement les molécules dommageables, elle a aussi bloqué les signaux de croissance des cellules cancéreuses et favorisé leur autodestruction. Bien que ces résultats proviennent de cultures cellulaires et de modèles informatiques — et non de patients — ils suggèrent une stratégie prometteuse : utiliser des nanoparticules lipidiques intelligentes pour transformer un composé alimentaire familier en un assistant ciblé contre le cancer du côlon. Si des études animales et cliniques futures confirment ces avantages et la sécurité, les cubosomes de lycopène pourraient compléter les thérapies existantes en offrant une façon plus douce et plus naturelle de soutenir les défenses antioxydantes et d’affaiblir les cellules tumorales.
Citation: Alsunbul, M., El-Masry, T.A., El-Bouseary, M.M. et al. Cubosomal nanoparticles of lycopene as a novel platform for enhancement in antioxidant and anticancer properties with a molecular docking study. Sci Rep 16, 5941 (2026). https://doi.org/10.1038/s41598-026-36217-7
Mots-clés: lycopène, nanoparticules, cancer du côlon, antioxydants, libération de médicament