Clear Sky Science · fr
Pigments distyryl-BODIPY substitués par du pyridinium et du brome pour la photothérapie mitochondrie-ciblée
Illuminer les cellules cancéreuses de l’intérieur
La thérapie photodynamique est un traitement du cancer qui utilise des médicaments activés par la lumière pour tuer les cellules tumorales tout en épargnant largement les tissus sains. Cette étude explore une nouvelle famille de colorants fluorescents conçus pour se diriger vers les centrales énergétiques de la cellule — les mitochondries — et, lorsqu’ils sont éclairés par une lumière rouge profond, générer des espèces d’oxygène toxiques capables de détruire les cellules cancéreuses. Les travaux montrent à la fois les promesses et les limites de l’ingénierie moléculaire de tels colorants.
Pourquoi cibler les centrales énergétiques de la cellule ?
Les mitochondries sont essentielles à la production d’énergie et influencent la décision d’une cellule de survivre ou de mourir. Les cellules cancéreuses tendent à présenter une membrane mitochondriale plus fortement chargée que les cellules normales, ce qui leur permet d’attirer beaucoup plus fortement des molécules chargées positivement. Les chercheurs ont tiré parti de ce phénomène en greffant un groupe pyridinium chargé positivement sur un échafaudage de colorant fluorescent bien connu appelé BODIPY. Cette conception aide à diriger les colorants vers les mitochondries, où des réactions chimiques déclenchées par la lumière peuvent infliger un maximum de dégâts aux cellules cancéreuses tout en limitant les dommages ailleurs.
Concevoir des colorants photoactivés plus intelligents
L’équipe a créé trois colorants étroitement apparentés, nommés PyBHI, PyBMI et PyBBrI, qui diffèrent principalement par le nombre d’atomes de brome qu’ils portent (aucun, un ou deux). Ils partagent tous une structure longue et étendue qui décale leur absorption et leur émission vers le proche infrarouge — une fenêtre utile où la lumière peut pénétrer plus profondément dans les tissus. En théorie, ces colorants pourraient emprunter deux voies internes différentes pour atteindre un état excité de type « triplet » produisant l’oxygène singulet réactif : l’une favorisée par les atomes lourds de brome et l’autre par un déplacement temporaire de charge électrique au sein de la molécule. 
Quand la théorie rencontre la réalité expérimentale
Malgré une conception élégante, des tests détaillés ont montré que les colorants ne généraient pas l’oxygène singulet aussi efficacement qu’espéré. À l’aide de sondes chimiques qui perdent leur couleur en réagissant avec l’oxygène singulet, les chercheurs ont mesuré des rendements de production d’oxygène très faibles pour les trois colorants, avec seulement une amélioration modeste lorsque le nombre d’atomes de brome augmentait. Des expériences par laser ultrarapide ont révélé la raison : après absorption de la lumière, les colorants passent rapidement dans des états décalés de charge qui se relâchent principalement sous forme de chaleur plutôt que de se convertir en l’état triplet souhaité. Dans les versions bromées, les atomes lourds ouvrent toujours une voie vers l’état triplet, mais cette route est beaucoup plus lente que la perte d’énergie concurrente, limitant l’efficacité globale.
Cibler les mitochondries tumorales dans des cellules vivantes
L’histoire change en contexte biologique. Dans des cellules cancéreuses humaines en culture, de sein (MCF-7) et du col de l’utérus (HeLa), les trois colorants se sont révélés, par imagerie confocale, s’accumuler fortement dans les mitochondries, se co-localisant avec un marqueur mitochondrial standard. Les tests de toxicité à l’obscurité ont indiqué que les colorants sont largement inoffensifs sans lumière. Sous irradiation par une lumière rouge, cependant, le colorant dibromé PyBBrI a provoqué une mortalité importante des cellules cancéreuses, des doses en faible nanomolaire réduisant de moitié la viabilité cellulaire. Les deux autres colorants étaient beaucoup moins efficaces. 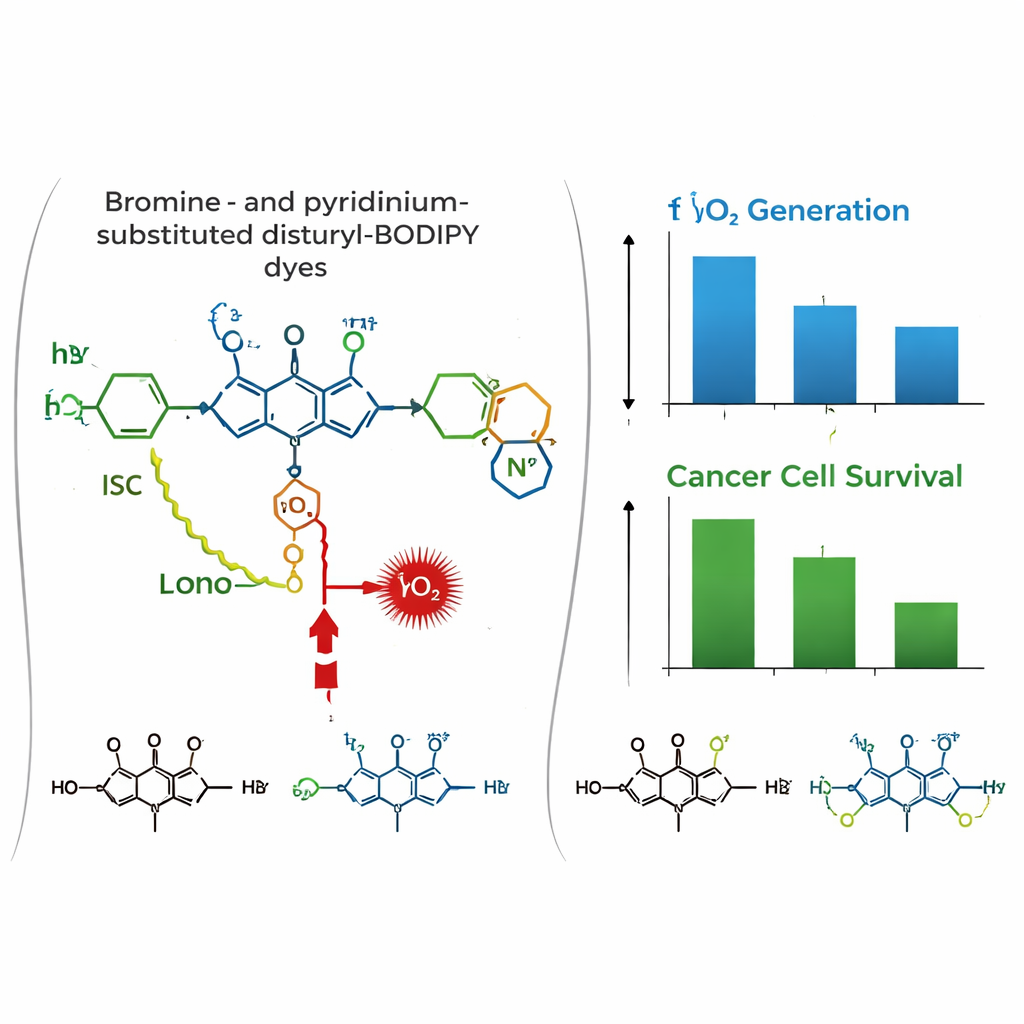
Ce que cela implique pour les thérapies anticancéreuses futures
Pour un non-spécialiste, le message clé est que de petites modifications chimiques peuvent modifier drastiquement le comportement des médicaments photoactivés contre le cancer, et que leurs performances dans de véritables cellules peuvent être meilleures — ou pires — que celles prévues par des mesures de base. Dans ce cas, le colorant le plus modifié, PyBBrI, n’a montré qu’une production d’oxygène réactif modeste en éprouvette mais s’est avéré extrêmement puissant contre les cellules cancéreuses une fois qu’il a atteint leurs mitochondries. Le travail souligne à la fois l’importance de diriger les médicaments vers des structures vulnérables à l’intérieur des cellules cancéreuses et la complexité de la prédiction de l’efficacité photodynamique. Il ouvre la voie à des thérapies de nouvelle génération ciblant les mitochondries et utilisant la lumière proche-infrarouge pour « activer » sélectivement la chimie cytotoxique exactement là où elle est nécessaire.
Citation: Kim, C., Badon, I.W., Jo, J. et al. Pyridinium- and bromine-substituted distyryl-BODIPY dyes for mitochondria-targeted photodynamic therapy. Sci Rep 16, 6789 (2026). https://doi.org/10.1038/s41598-026-36213-x
Mots-clés: thérapie photodynamique, colorants ciblant les mitochondries, BODIPY, oxygène singulet, cellules cancéreuses