Clear Sky Science · fr
La γ‑radiation induit des altérations subcellulaires spécifiques à chaque région des marqueurs de la sclérose latérale amyotrophique et de la démence frontotemporale dans le cerveau de porc
Pourquoi de faibles doses de radiation et le cerveau de porc comptent
La plupart d’entre nous considèrent la radiation comme purement nocive, en particulier pour le cerveau. Pourtant, notre environnement est ponctué de faibles niveaux de radiation provenant d’examens médicaux, des voyages en avion et de l’environnement naturel. Parallèlement, les scientifiques cherchent encore à comprendre les causes de la sclérose latérale amyotrophique (SLA), la maladie mortelle qui a paralysé la vedette du baseball Lou Gehrig, et de sa proche cousine, la démence frontotemporale (DFT), qui affecte le comportement et la personnalité. Cette étude pose une question surprenamment optimiste : une dose unique et modeste de rayonnement gamma pourrait‑elle remodeler subtilement la chimie cérébrale d’une manière qui ne soit pas purement délétère et qui, peut‑être, serait même protectrice contre les modifications moléculaires liées à la SLA et à la DFT ?
Un examen plus attentif des signaux d’alerte de la SLA dans le cerveau
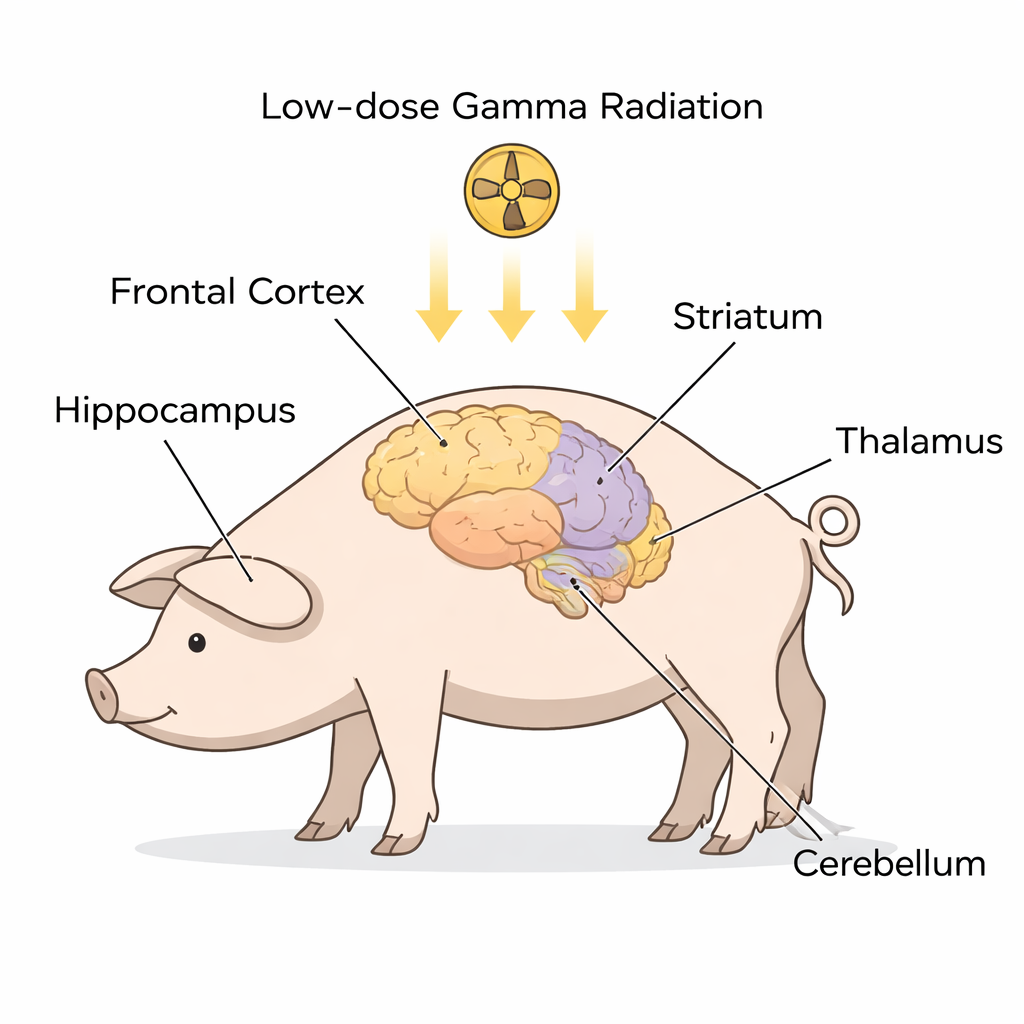
Plutôt que d’examiner des patients déjà atteints de SLA, les chercheurs ont travaillé avec des mini‑porcs de Göttingen en bonne santé, dont le cerveau présente des similitudes anatomiques avec le nôtre. Neuf animaux ont reçu une exposition corps entier unique à faible dose de rayonnement gamma, tandis que six ont été anesthésiés sans irradiation et ont servi de témoins. Environ un mois plus tard, les scientifiques ont disséqué cinq régions cérébrales clés souvent impliquées dans la SLA et la DFT — le cortex frontal, l’hippocampe, le striatum, le thalamus/l’hypothalamus et le cervelet. Dans chaque région, ils ont séparé le contenu cellulaire en deux compartiments principaux : le cytoplasme (l’intérieur liquide de la cellule) et le noyau (le compartiment contenant l’ADN). À l’aide d’une technique appelée Western blot, ils ont quantifié les niveaux de plusieurs protéines étroitement liées à la SLA et à la SLA‑DFT, notamment SOD1, FUS, C9orf72, STMN2, ubiquitine, TDP‑43 et une forme modifiée appelée TDP‑43 phosphorylé.
La radiation laisse certains marqueurs inchangés — et en déplace d’autres
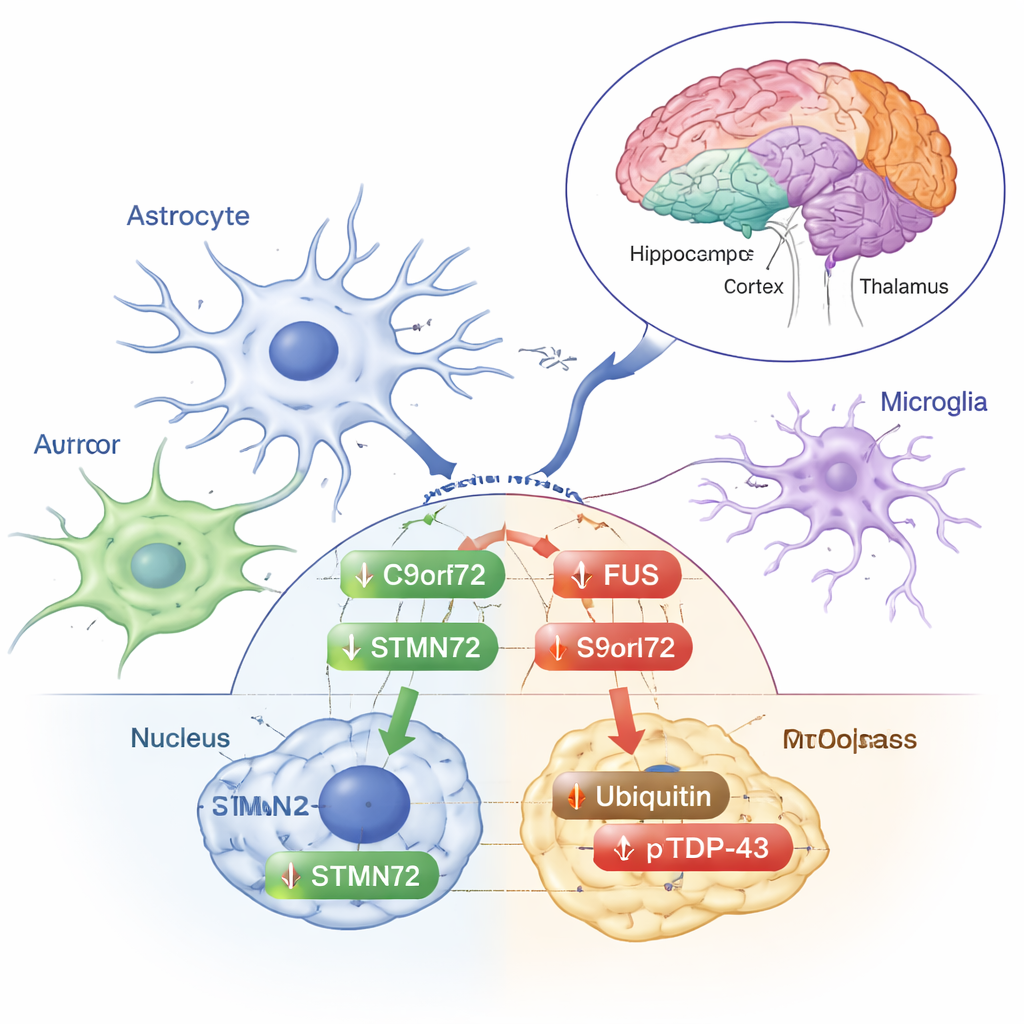
Une observation rassurante est que les niveaux totaux de SOD1, une protéine dont les mutations causent certaines formes héréditaires de SLA, n’ont pas changé dans aucune région après irradiation. De même, les formes principales de TDP‑43 — la protéine la plus souvent retrouvée dans les amas cérébraux liés à la SLA — sont restées stables dans le noyau et le cytoplasme de toutes les régions. Mais tout n’est pas resté statique. L’équipe a observé des variations spécifiques selon la région et le compartiment pour plusieurs autres protéines. Par exemple, FUS, une protéine qui réside normalement dans le noyau mais peut mal fonctionner et s’agréger dans la SLA, a diminué dans le cytoplasme du thalamus/l’hypothalamus après irradiation, tandis que ses niveaux nucléaires ont augmenté dans le cortex frontal et diminué dans l’hippocampe. La protéine liée à la SLA, C9orf72, n’a pas changé dans le fluide cellulaire mais a montré une baisse à l’intérieur des noyaux hippocampiques. STMN2, une protéine importante pour le maintien des fibres nerveuses, a également diminué dans les noyaux de l’hippocampe, suggérant une réponse coordonnée entre ces deux molécules dans cette région liée à la mémoire.
Signaux de stress ou protection précoce ?
D’autres changements ressemblaient davantage à des réponses classiques au stress. L’ubiquitine — la petite étiquette que la cellule utilise pour marquer les protéines endommagées en vue de leur élimination — a augmenté dans la fraction cytoplasmique du cortex frontal. La forme phosphorylée de TDP‑43, souvent enrichie dans les dépôts anormaux observés dans la SLA et la DFT, a augmenté dans le cytoplasme du cortex frontal, du striatum et du thalamus/l’hypothalamus, alors que le TDP‑43 total lui‑même ne changeait pas. Ces variations suggèrent que la radiation à faible dose pousse doucement la machinerie de gestion des protéines du cerveau sans déclencher les schémas complets de mal‑repliement et d’agrégation qui caractérisent la maladie. Les auteurs soulignent que ces réponses varient selon la région cérébrale et selon que la protéine se trouve à l’intérieur ou à l’extérieur du noyau, ce qui met en évidence la finesse de la réaction cérébrale au stress.
Ce que cela pourrait signifier pour le risque de SLA — et les bénéfices possibles
Est‑ce que cela signifie que la radiation à faible dose provoque la SLA ? Les données plaident contre une réponse affirmative simple. Les chercheurs n’ont pas observé la mauvaise localisation caractéristique ou l’accumulation des protéines principales de la SLA, et de nombreux changements suggèrent une régulation altérée plutôt qu’un dommage franc. De façon intrigante, ces résultats s’inscrivent dans la continuité de travaux antérieurs du même groupe et d’autres, indiquant que de petites quantités de radiation peuvent parfois déclencher une « hormèse » — un phénomène où un stress léger active des voies de réparation et réduit des protéines nocives, comme celles liées à la maladie d’Alzheimer ou de Parkinson dans des modèles animaux. L’étude actuelle laisse entendre que, du moins à court terme, une dose unique et faible de rayons gamma modifie les marqueurs liés à la SLA de façon possiblement adaptative plutôt que destructive.
Grandes questions et espoir prudent
Pour le lecteur non spécialiste, l’essentiel est que la relation entre radiation et santé cérébrale est plus nuancée que « toute radiation est mauvaise ». Dans ce modèle animal de grande taille, une exposition à faible dose de gamma a produit des variations subtiles et spécifiques à chaque région des protéines associées à la SLA et à la DFT, sans reproduire les schémas délétères observés dans les cerveaux de patients. Ces changements pourraient refléter la tentative du cerveau de faire face au stress et de réparer les dommages, et dans certains cas se révéler bénéfiques. Cependant, l’étude n’a examiné que le mois suivant une exposition unique, et uniquement le cerveau (pas la moelle épinière, où la SLA frappe le plus). Des études à long terme et avec doses répétées sont nécessaires avant d’envisager toute traduction chez l’humain. Néanmoins, ce travail ouvre une nouvelle fenêtre sur la manière dont des niveaux de radiation proches du quotidien interagissent avec les molécules à l’origine de maladies neurodégénératives dévastatrices — et soulève la possibilité qu’à l’avenir, dans des contextes strictement contrôlés, de faibles doses puissent être exploitées pour stimuler les défenses naturelles du cerveau.
Citation: Iacono, D., Murphy, E.K., Perl, D.P. et al. γ-Radiation induces region-specific subcellular alterations of amyotrophic lateral sclerosis and frontotemporal dementia markers in swine brain. Sci Rep 16, 5627 (2026). https://doi.org/10.1038/s41598-026-36208-8
Mots-clés: sclérose latérale amyotrophique, démence frontotemporale, radiation à faible dose, protéines cérébrales, modèle mini‑porc