Clear Sky Science · fr
Attrition des télomères des leucocytes après radiothérapie pour cancer de la prostate : une étude prospective
Pourquoi cette recherche importe pour les personnes ayant survécu au cancer
Les personnes vivent plus longtemps après un cancer, mais beaucoup de survivants remarquent des problèmes qui ressemblent à un vieillissement « accéléré » : fatigue, fragilité et autres affections chroniques qui semblent survenir trop tôt. Cette étude pose une question simple mais importante : le traitement par radiation du cancer de la prostate laisse-t‑il une trace durable sur l’horloge fondamentale du vieillissement du corps, cachée dans nos chromosomes ?
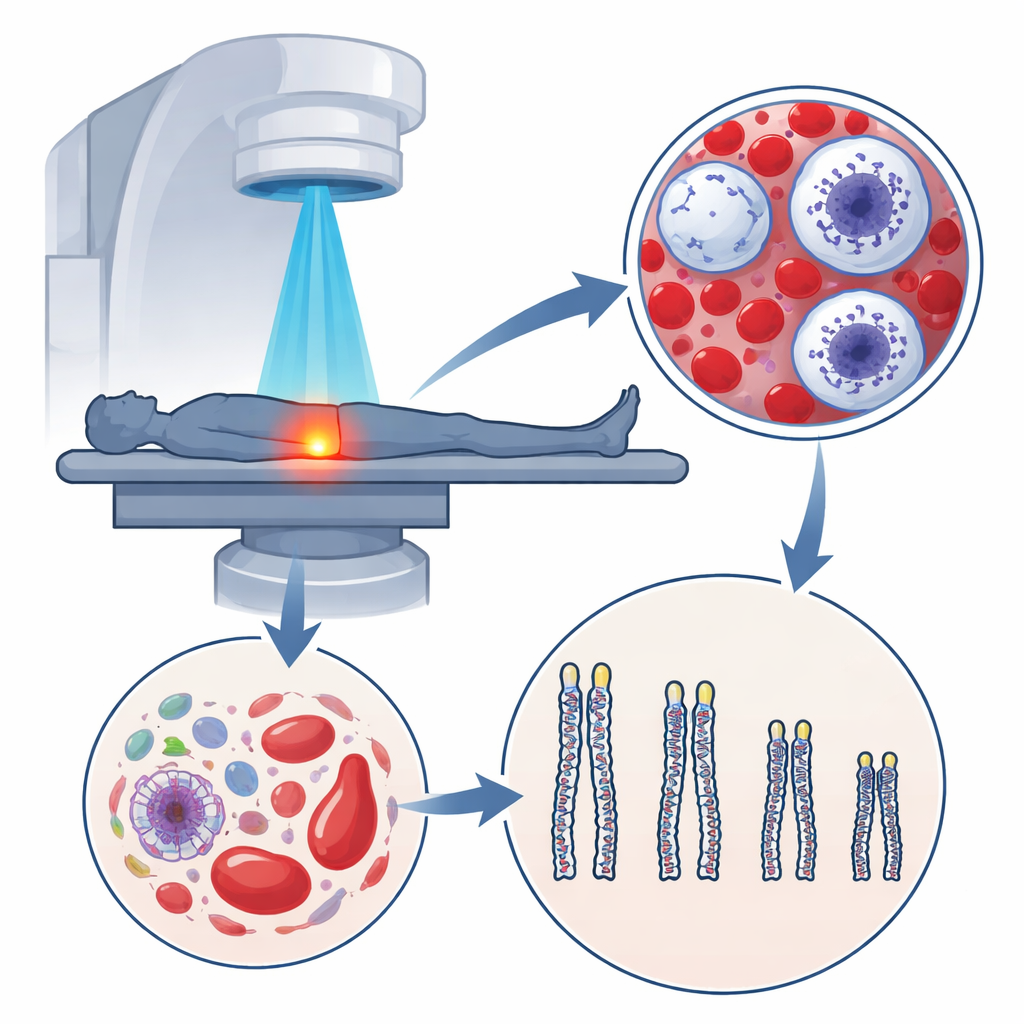
Les petites embouts qui protègent notre ADN
Aux extrémités de nos chromosomes se trouvent les télomères, de petites séquences d’ADN qui fonctionnent comme les embouts plastiques des lacets, empêchant le matériel génétique de s’effilocher. À chaque division cellulaire, ces embouts raccourcissent un peu. Lorsqu’ils deviennent trop courts, la cellule est poussée à s’arrêter ou à mourir, un processus lié au vieillissement naturel. Parce que les globules blancs sont faciles à échantillonner dans le sang et reflètent ce qui se passe dans de nombreux tissus, la longueur de leurs télomères est souvent utilisée comme jauge de « l’âge biologique », qui peut différer de l’âge chronologique.
Observer de près pendant et après le traitement
Pour voir comment la radiothérapie moderne de la prostate pourrait influencer cette jauge du vieillissement, les chercheurs ont suivi 314 hommes âgés de 65 ans et plus recevant une radiothérapie à visée curative dans un centre médical. Des prélèvements sanguins ont été réalisés quatre fois : avant le traitement, à la fin du cycle de radiothérapie de plusieurs semaines, puis 3 mois et 15 mois après. Dans chaque échantillon, l’équipe a mesuré la longueur relative moyenne des télomères des globules blancs avec un test d’ADN sensible. Ce protocole leur a permis de suivre l’évolution des télomères de chaque homme dans le temps, plutôt que de se contenter de comparer différentes personnes à un seul instant.
Ce qui est arrivé aux télomères au fil du temps
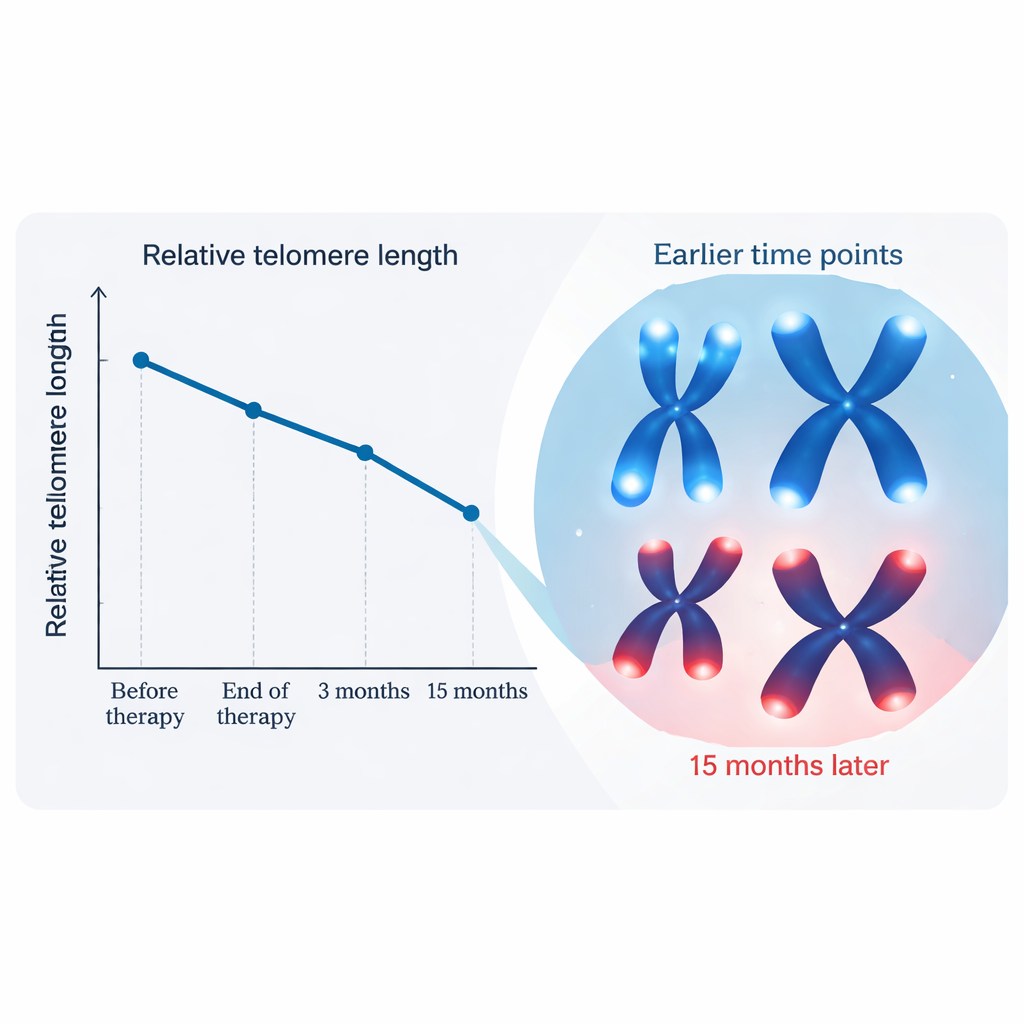
La longueur des télomères est restée globalement similaire entre l’avant‑traitement, la fin de la radiothérapie et le contrôle à 3 mois, avec de faibles variations non significatives statistiquement. Le changement marquant est apparu au terme des 15 mois : en moyenne, les télomères étaient environ 15 % plus courts qu’au départ, une baisse bien plus importante que ce que l’on attendrait du vieillissement normal sur un peu plus d’un an chez des adultes âgés. Ce schéma suggère que l’impact biologique à long terme de la radiation sur le sang peut émerger lentement, bien après la disparition des effets secondaires visibles. Les chercheurs ont aussi exploré si des facteurs comme l’âge, l’hypertension, le tabagisme, les détails du traitement ou la radiothérapie des ganglions lymphatiques voisins pouvaient influencer ces changements. L’âge et l’hypertension ont montré des liens modestes avec l’importance du raccourcissement, tandis que la plupart des variations de traitement n’ont pas modifié clairement le résultat dans ce groupe.
Comment la radiation pourrait accélérer l’usure cellulaire
Pourquoi un traitement local par radiation de la prostate affecterait‑il les télomères des cellules sanguines en circulation ? Les auteurs évoquent deux processus reliés. D’une part, les rayonnements ionisants génèrent des molécules réactives de l’oxygène qui peuvent endommager l’ADN, et les télomères sont particulièrement vulnérables à ce type d’atteinte et réparés moins efficacement que d’autres régions. D’autre part, la radiothérapie peut déclencher une réaction inflammatoire persistante dans l’organisme, poussant les globules blancs à se diviser plus souvent et libérant davantage de sous‑produits oxydants nocifs. Les deux mécanismes pourraient accélérer l’érosion progressive des télomères, poussant les cellules vers un état de sénescence — un état irréversible de « vieillesse » où elles ne se divisent plus mais continuent d’influencer les tissus environnants.
Ce que cela pourrait signifier pour les patients
Pour les hommes de cette étude, la radiothérapie de la prostate restait un traitement curatif, mais elle a aussi été associée à des signes d’un vieillissement biologique accéléré de leurs cellules sanguines un an après la thérapie. Des télomères plus courts à eux seuls ne prouvent pas qu’une personne deviendra fragile ou malade, mais ils sont liés à un risque plus élevé de problèmes liés à l’âge comme les maladies cardiaques, le diabète et le déclin cognitif. Ces résultats soulignent que le succès du traitement du cancer peut s’accompagner de coûts cachés à long terme et mettent en avant la nécessité d’un suivi prenant en compte la santé liée au vieillissement, pas seulement le contrôle tumoral. Les auteurs soutiennent que des études plus larges et plus longues — incluant des comparaisons avec des personnes non traitées par radiation — sont nécessaires pour confirmer ces résultats et tester des approches protectrices, comme cibler l’inflammation ou le stress oxydatif, qui pourraient aider à préserver la résilience biologique des patients après la thérapie.
Citation: Langsenlehner, T., Paal, K., Thurner, E.M. et al. Leukocyte telomere attrition following radiotherapy in prostate cancer: a prospective study. Sci Rep 16, 5905 (2026). https://doi.org/10.1038/s41598-026-36205-x
Mots-clés: cancer de la prostate, radiothérapie, télomères, vieillissement biologique, sénescence cellulaire