Clear Sky Science · fr
Évaluation des performances diagnostiques du dosage Elecsys anti-SARS-CoV-2 par rapport à la RT‑PCR pour la détection et la surveillance du SARS‑CoV‑2 dans des hôpitaux de référence éthiopiens : étude transversale
Pourquoi cette étude compte pour la vie quotidienne
Plus de quatre ans après l’apparition du COVID‑19, de nombreux pays peinent encore à tester rapidement et précisément les personnes, en particulier dans les contextes à ressources limitées. Cette étude menée dans la région Oromia d’Éthiopie pose une question pratique d’intérêt mondial : un test sanguin couramment utilisé pour détecter les anticorps contre le COVID‑19 peut‑il remplacer, pour repérer les infections en cours et estimer le nombre de personnes déjà exposées, le test PCR plus complexe ? La réponse a des implications importantes pour la manière dont les hôpitaux surveillent les flambées, protègent patients et personnels, et planifient les épidémies futures.
Un examen approfondi à l’intérieur des hôpitaux surchargés
Les chercheurs ont travaillé dans cinq grands hôpitaux de référence d’Oromia en août 2021, période où le COVID‑19 circulait encore activement. Ils ont inclus 1 360 patients s’étant présentés dans ces hôpitaux, quel que soit le fait qu’ils présentaient ou non des symptômes compatibles avec le COVID‑19. Chaque personne a fourni deux types d’échantillons : un prélèvement nasopharyngé pour le test RT‑PCR, qui détecte le virus lui‑même, et un prélèvement sanguin pour le test Elecsys anti‑SARS‑CoV‑2, qui recherche des anticorps témoignant d’une infection passée. Parallèlement aux analyses de laboratoire, du personnel formé a recueilli des informations sur l’âge, le lieu de résidence, les symptômes, les antécédents médicaux et les contacts avec des cas confirmés.
Quelle était la prévalence des infections actuelles et passées ?
Les résultats montrent que le COVID‑19 avait laissé une empreinte profonde chez les patients hospitalisés. Près d’un participant sur cinq (environ 18 %) avait une infection active détectée par RT‑PCR au moment de l’étude. Plus frappant encore, un peu plus de la moitié (53,2 %) présentait des anticorps, indiquant une infection antérieure — souvent sans diagnostic confirmé. Les résidents urbains étaient beaucoup plus susceptibles que les résidents ruraux d’avoir une infection active, et les symptômes classiques tels que fièvre, toux, courbatures ainsi que le contact avec des cas confirmés étaient associés à une probabilité plus élevée d’être positif en RT‑PCR. En revanche, la présence ou l’absence de symptômes et l’historique de contact ne prédisaient pas clairement qui avait des anticorps, reflétant la circulation large et souvent silencieuse du virus sur plusieurs mois.
Mettre le test d’anticorps à l’épreuve
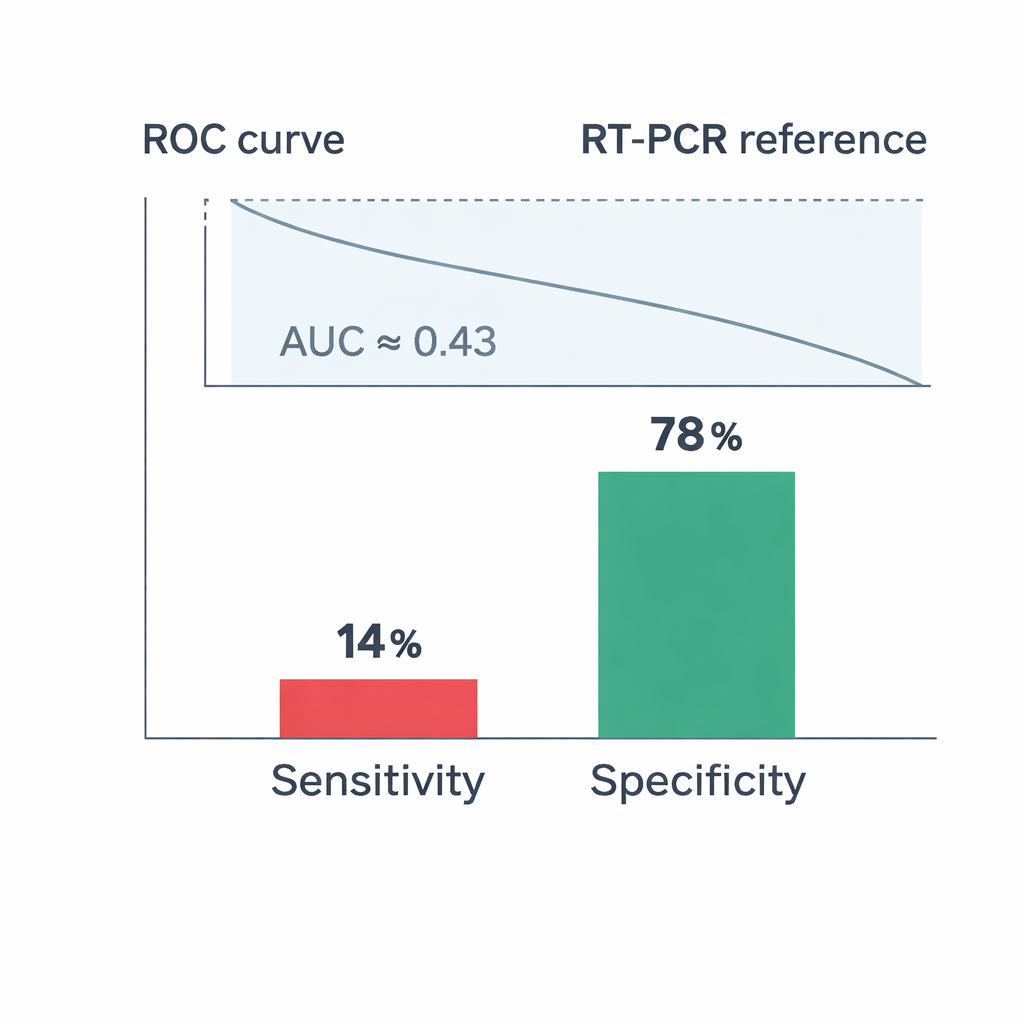
Le cœur de l’étude consistait à évaluer dans quelle mesure le test Elecsys pouvait se substituer à la RT‑PCR pour identifier les infections en cours. Les résultats sont sévères. Parmi les personnes PCR‑positives, seulement 14 % avaient simultanément un résultat Elecsys positif, ce qui signifie que le test sanguin a manqué la grande majorité des infections actives. Sa spécificité — la fréquence à laquelle il identifiait correctement les personnes sans infection actuelle — était plus élevée, autour de 78 %, mais l’accord global entre les deux tests était faible. Une mesure statistique, le kappa de Cohen, était proche de zéro, et l’aire sous la courbe ROC (AUC), qui résume la performance diagnostique globale, n’était que de 0,43 — pire que ce qu’on attendrait au hasard pour distinguer infectés et non infectés.
Ce que ces chiffres nous apprennent sur le rôle des tests
Pourquoi le test d’anticorps a‑t‑il si mal performé pour détecter les cas actifs ? Les deux tests évaluent des phases différentes de l’infection. La RT‑PCR détecte le matériel génétique viral pendant la brève fenêtre où le virus se réplique activement et où la personne est contagieuse. Les anticorps, en revanche, apparaissent généralement plus tard et peuvent persister dans le sang pendant des mois. Lorsqu’on effectue les deux tests le même jour, de nombreuses personnes réellement infectées n’ont pas encore développé suffisamment d’anticorps pour être détectées. Dans une population où plus de la moitié des personnes ont déjà été infectées, ce décalage temporel réduit fortement l’accord entre les tests. L’échantillon hospitalier de l’étude — comprenant probablement beaucoup de patients gravement malades ou déjà exposés — a encore accentué cette discordance.
Conséquences pour les patients et la santé publique
Pour les patients et les décideurs, le message est clair mais double. La RT‑PCR reste essentielle pour diagnostiquer qui est actuellement infecté et nécessite isolement ou traitement. Le test d’anticorps Elecsys, tel qu’utilisé dans ce contexte éthiopien réel, ne doit pas être utilisé seul pour détecter le COVID‑19 actif. En revanche, sa spécificité relativement élevée et sa simplicité (prélèvement sanguin) en font un outil utile pour une autre tâche : suivre l’étendue de la propagation du virus dans la communauté au fil du temps. Dans les régions où les appareils PCR et le personnel qualifié manquent, le dépistage par anticorps peut aider à estimer l’exposition totale et orienter la planification à long terme des vaccinations et des futures flambées — même s’il ne peut pas remplacer en toute sécurité la RT‑PCR au chevet.
Citation: Gobena, D., Gudina, E.K., Degfie, T.T. et al. Diagnostic performance evaluation of Elecsys anti-SARS-CoV-2 assay against RT-PCR for SARS-CoV-2 detection and surveillance in Ethiopian referral hospitals: cross-sectional study. Sci Rep 16, 5207 (2026). https://doi.org/10.1038/s41598-026-36177-y
Mots-clés: dépistage COVID-19, anticorps SARS‑CoV‑2, diagnostic RT‑PCR, hôpitaux Éthiopie, séro-surveillance