Clear Sky Science · fr
FcIgG-GE11-Melittin en tant que nouveau peptibody ciblant l’EGFR avec une puissante activité cytotoxique contre les cellules cancéreuses
Le venin d’abeille rencontre la thérapie anticancéreuse de précision
De nombreux médicaments anticancéreux prometteurs sont tout simplement trop agressifs pour être utilisés en toute sécurité. Un exemple marquant est la mélittine, la toxine principale du venin d’abeille : elle peut déchirer les cellules cancéreuses, mais elle peut aussi endommager les globules rouges et les tissus sains. Cette étude explore une solution ingénieuse — construire un « missile guidé » qui transporte la mélittine directement vers les cellules tumorales affichant un marqueur de surface spécifique, tout en épargnant largement les cellules normales.
Pourquoi cibler un commutateur courant du cancer
Un acteur clé dans de nombreuses tumeurs est une molécule appelée récepteur du facteur de croissance épidermique, ou EGFR. Ce récepteur se situe à la surface des cellules et aide à contrôler la croissance et la survie. Dans plusieurs cancers — notamment du poumon, colorectal, de la prostate, ainsi que certains cancers de la tête et du cou et du rein — l’EGFR est surexprimé, entraînant une division cellulaire incontrôlée. De ce fait, les médicaments qui se lient à l’EGFR sont devenus une classe importante de thérapies ciblées. Cependant, les traitements EGFR existants bloquent principalement les signaux ; ils ne perforent pas activement les cellules cancéreuses. Les chercheurs se sont demandé s’ils pouvaient exploiter la puissante capacité lyseuse de la mélittine et la délivrer sélectivement aux cellules tumorales riches en EGFR.
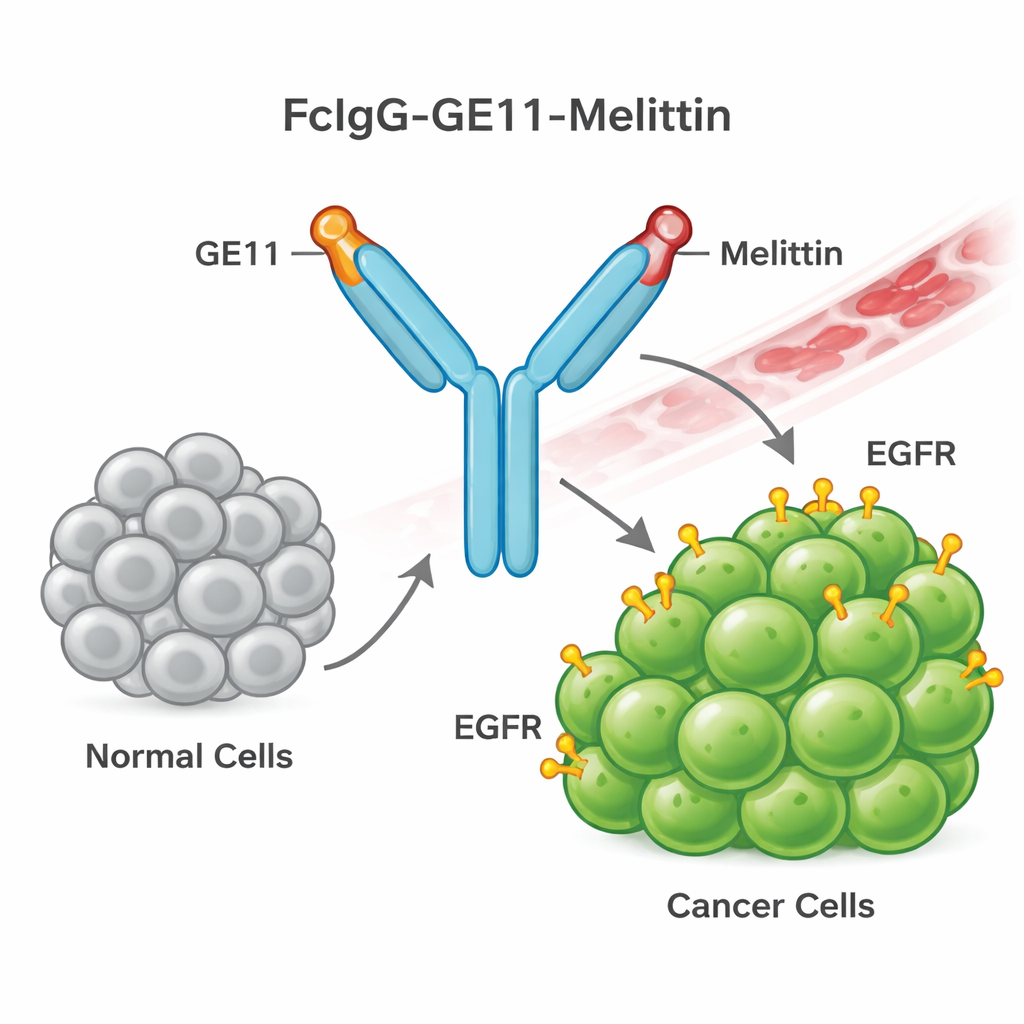
Construire une arme guidée au venin d’abeille
Pour ce faire, l’équipe a conçu une nouvelle protéine de fusion qu’ils appellent FcIgG-GE11-Melittin. Elle combine trois éléments : une « queue » d’anticorps (la région Fc de l’IgG humaine) qui améliore la stabilité dans la circulation sanguine et facilite la purification ; un petit peptide guide appelé GE11 qui reconnaît et se lie à l’EGFR sur les cellules cancéreuses ; et la mélittine, le peptide du venin d’abeille capable de rompre les membranes cellulaires. Des bactéries ont été modifiées pour produire cette protéine de fusion en grande quantité. La protéine a ensuite été repliée et purifiée, et des tests en laboratoire ont confirmé qu’elle formait la forme dimérique attendue et portait l’étiquette d’anticorps humain, montrant que le construit avait été correctement assemblé.
S’accrocher aux cellules tumorales, pas à n’importe quelle cellule
La question suivante était de savoir si cette molécule conçue trouvait réellement et se fixait aux cellules cancéreuses riches en EGFR. À l’aide de cytométrie en flux, les auteurs ont testé la fixation sur des cellules de cancer du poumon A549, connues pour surexprimer l’EGFR. Les cellules traitées avec FcIgG-GE11-Melittin ont montré une forte augmentation de la fluorescence, indiquant que de nombreuses molécules de fusion s’étaient attachées à leur surface. Un peptibody non lié, Romiplostim, a montré presque aucune fixation, servant de contrôle négatif. Le profil de liaison du nouveau construit correspondait étroitement à celui du Cetuximab, un anticorps anti-EGFR bien connu, soutenant l’idée que la composante GE11 guide correctement la protéine de fusion vers sa cible.
Tuer les cellules cancéreuses tout en épargnant les cellules sanguines
L’équipe a ensuite évalué la capacité de la protéine de fusion à tuer différentes lignées cellulaires cancéreuses en culture. La mélittine libre était extrêmement puissante mais indiscriminée, réduisant fortement la survie cellulaire même à faibles doses dans des cancers du poumon (A549), de la prostate (DU145) et colorectal (SW480). En revanche, FcIgG-GE11-Melittin a montré une cytotoxicité dépendante de la dose, la plus forte étant observée dans les cellules positives pour l’EGFR, tandis qu’une lignée de cancer du sein à faible EGFR (MDA-MB-453) était relativement résistante. Ce schéma suggère que l’attaque du construit dépend du ciblage de l’EGFR plutôt que d’un dommage membranaire aléatoire. Surtout, dans des expériences avec des globules rouges humains, la mélittine libre a provoqué une hémolyse presque complète à des doses modestes, alors que la protéine de fusion a produit moins de 5 % d’hémolyse même à des concentrations très élevées. En d’autres termes, attacher la mélittine au vecteur ciblant l’EGFR réduit drastiquement sa tendance à faire éclater les globules rouges.
Ce que cela pourrait signifier pour les soins anticancéreux futurs
Dans l’ensemble, ce travail montre que coupler une toxine puissante perturbatrice de membranes comme la mélittine à un système de ciblage précis peut la transformer d’une substance largement toxique en une arme plus sélective pour les tumeurs. FcIgG-GE11-Melittin se lie fortement aux cellules cancéreuses surexprimant l’EGFR, les tue de manière contrôlée et dépendante de la dose, et montre des dommages minimaux aux globules rouges en laboratoire. Bien que des études animales supplémentaires et des tests de sécurité soient nécessaires avant toute utilisation chez les patients, cette approche illustre comment le réaménagement de toxines naturelles en thérapies guidées pourrait ouvrir de nouvelles voies pour traiter plus efficacement les cancers EGFR-positifs et avec moins d’effets secondaires.
Citation: Hallaji, M., Fayaz, S., Allahyari, M. et al. FcIgG-GE11-Melittin as a novel EGFR targeted peptibody with potent cytotoxic activity against cancer cells. Sci Rep 16, 7047 (2026). https://doi.org/10.1038/s41598-026-36167-0
Mots-clés: thérapie ciblée du cancer, EGFR, mélittine du venin d’abeille, peptibody, toxines sélectives pour les tumeurs