Clear Sky Science · fr
Modèle de probabilité multinomiale des AMB et des amas non-DSB induits par les radiations : dommages en tandem et bistrandés
Pourquoi de petites blessures de l’ADN comptent
Quand nous pensons aux dommages causés par les radiations à notre matériel génétique, nous imaginons souvent des ruptures spectaculaires de l’hélice d’ADN. Mais la plupart des lésions liées aux radiations sont plus subtiles et plus rapprochées qu’une simple coupure nette. Cet article explore ces amas cachés de petites blessures de l’ADN qui peuvent discrètement accroître le risque de cancer lié aux radiations médicales, professionnelles ou aux rayons cosmiques en espace.
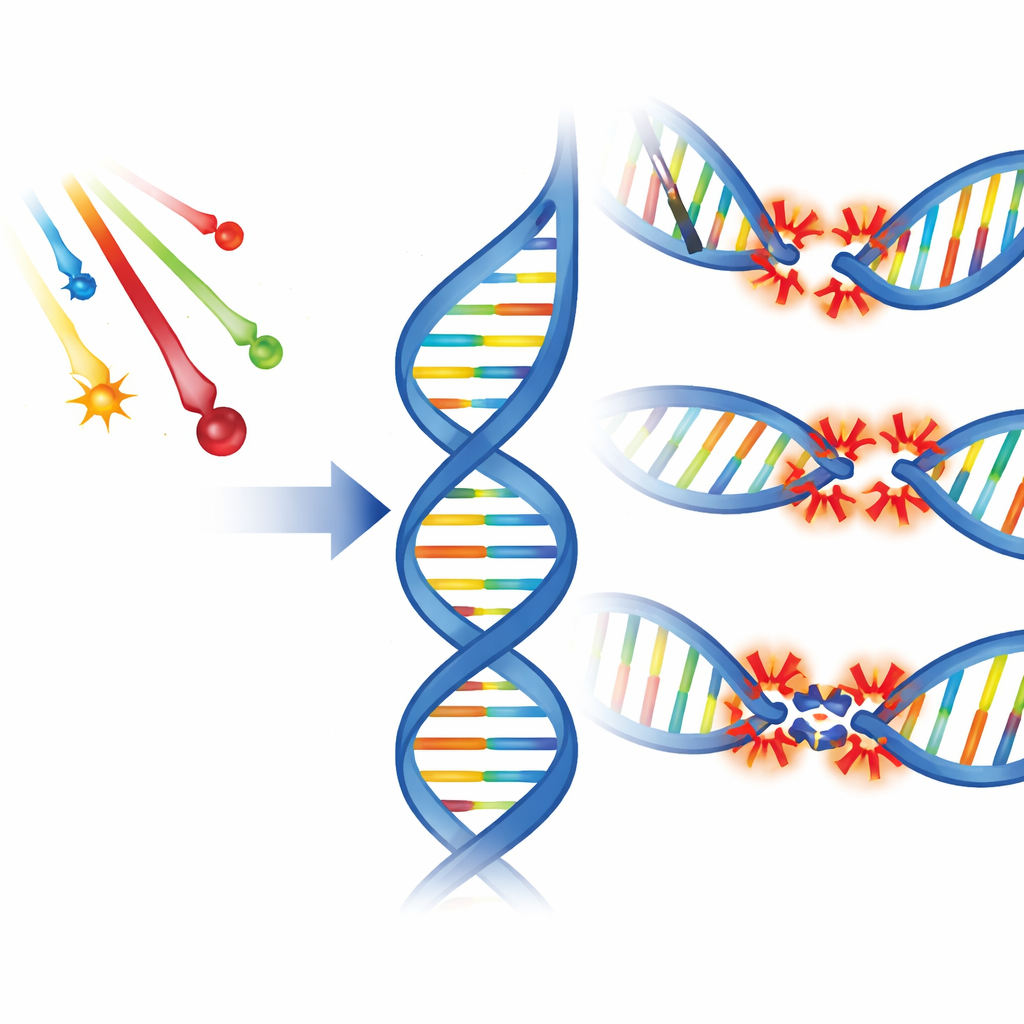
Différents types de ruptures dans l’échelle de l’ADN
Les rayonnements ionisants endommagent l’ADN de plusieurs façons fondamentales. Ils peuvent entailler un seul brin de la double hélice, sectionner les deux brins à proximité, ou altérer chimiquement les bases qui codent l’information génétique. Les scientifiques appellent cela des ruptures mono-brin, des ruptures bi-brin et des dommages aux bases. Il est important de noter que les radiations provoquent souvent plusieurs de ces lésions regroupées sur quelques tours de l’hélice. Ces sites resserrés, appelés dommages groupés, se présentent principalement sous deux formes : les amas bistrandés, où les lésions se font face sur des brins opposés, et les amas en tandem, où plusieurs lésions s’alignent le long d’un même brin. Les expériences ont montré que les amas non–bi-brin — composés majoritairement de dommages aux bases et de ruptures mono-brin — sont plus fréquents que les ruptures bi-brin nettes, en particulier à faible dose.
Combler les angles morts des expériences
Les techniques expérimentales actuelles ne montrent qu’une partie de ce tableau. Les tests enzymatiques et l’imagerie à haute résolution peuvent détecter de nombreux amas bistrandés, où les lésions sur des brins opposés se traduisent par des ruptures visibles. Mais les méthodes permettant de compter les amas en tandem, constitués de multiples lésions le long d’un seul brin, sont encore insuffisantes. Cela signifie que nos mesures actuelles sous-estiment le nombre réel d’atteintes groupées. Pour combler cette lacune, l’auteur construit un modèle théorique qui ne repose pas sur la détection directe de chaque lésion. Il utilise plutôt la quantité d’énergie déposée par les radiations dans un minuscule volume contenant de l’ADN, et la manière dont cette énergie est répartie de façon probabiliste entre différents types de lésions élémentaires.
Une carte probabiliste du chaos microscopique
Le cœur du travail est un modèle de probabilité multinomiale : un cadre mathématique qui suit comment une bouffée d’énergie incidente peut conduire simultanément à plusieurs issues. Dans un cylindre nanométrique contenant environ 73 paires de bases d’ADN, le modèle considère quatre possibilités chaque fois que de l’énergie est déposée : des impacts directs sur l’échine de l’ADN provoquant des ruptures de brin, des impacts directs sur les bases provoquant des dommages chimiques, des impacts indirects sur l’eau environnante produisant des radicaux réactifs, et de l’énergie absorbée sans effet par des protéines et autres molécules voisines. En combinant ces probabilités avec des spectres détaillés de dépôt d’énergie pour des électrons et divers ions, le modèle énumère la fréquence d’apparition des différentes combinaisons de lésions — et, surtout, leur proximité le long ou à travers les brins d’ADN.
Ce que le modèle révèle sur les trajectoires de radiation
Appliqué aux électrons et aux faisceaux d’ions utilisés en thérapie anticancéreuse et en environnement spatial, l’étude prédit plus de 30 catégories de dommages à l’ADN, dont 24 types d’amas de lésions. Les calculs reproduisent les mesures existantes des ruptures bi‑brin pour les protons, l’hélium, le carbone et le fer, ce qui renforce la confiance dans les prédictions non observées concernant les amas. Dans des conditions typiques d’usage médical et pertinentes pour l’espace, le nombre total d’amas non–bi‑brin est estimé être approximativement quatre à six fois supérieur au nombre de ruptures bi‑brin. Parmi ces amas non‑DSB, les lésions en tandem apparaissent étonnamment souvent : environ la moitié à trois cinquièmes de la fréquence des amas bistrandés, avec seulement un déclin modéré lorsque les trajectoires de radiation deviennent plus denses. Le modèle montre également que la plupart des ruptures bi‑brin elles‑mêmes sont « complexes », contenant des dommages aux bases à proximité, ce qui peut compliquer leur réparation.
Implications pour la santé, la thérapie et les vols spatiaux
Les dommages groupés non‑DSB ne sont pas qu’un détail de comptabilité. Ces lésions resserrées sont principalement traitées par les voies de réparation par excision de base, qui peuvent être lentes et sujettes aux erreurs quand de nombreuses blessures coexistent dans une petite région. Les tentatives de réparation peuvent convertir des amas non‑DSB en ruptures bi‑brin retardées ou en mutations longtemps après l’exposition initiale. Le nouveau modèle probabiliste fournit un moyen rapide d’estimer ces blessures cachées pour n’importe quel type de rayonnement, sans le coût computationnel élevé des simulations complètes de trajectoire de Monte Carlo. Ses prédictions suggèrent que les normes de protection contre les radiations, la planification de la radiothérapie anticancéreuse et les évaluations des risques pour les astronautes devraient accorder autant d’attention à ces amas subtils qu’aux ruptures bi‑brin plus évidentes.
Conclusion
En résumé, ce travail montre que les radiations produisent beaucoup plus de lésions d’ADN non–bi‑brin étroitement groupées qu’on ne le pensait auparavant — plusieurs fois plus que les ruptures bi‑brin nettes — et que les amas en tandem le long d’un seul brin sont presque aussi fréquents que les amas bistrandés. En mariant les données de dépôt d’énergie à des probabilités multinomiales, le modèle offre un outil pratique pour estimer ces lésions invisibles pour de nombreux types de rayonnements. Pour le non‑spécialiste, le message clé est que les dommages d’ADN les plus dangereux dus aux radiations ne sont peut‑être pas les ruptures rares et spectaculaires que l’on voit facilement, mais les nombreuses petites blessures groupées qui défient silencieusement les systèmes de réparation de la cellule.
Citation: Cucinotta, F.A. Multinomial probability model of radiation induced DSB and non-DSB clusters: tandem and bistranded damage clusters. Sci Rep 16, 7877 (2026). https://doi.org/10.1038/s41598-026-36157-2
Mots-clés: dommages ADN groupés, biologie des radiations, rayonnements ionisants, radiothérapie du cancer, rayonnement spatial