Clear Sky Science · fr
Le TDP-43 cytoplasmique provoque des troubles comportementaux précoces sans neurodégénérescence dans un modèle de C. elegans spécifique aux neurones sérotoninergiques
Pourquoi de minuscules vers comptent pour de grandes maladies cérébrales
Des maladies comme la sclérose latérale amyotrophique (SLA) et la démence frontotemporale (DFT) privent progressivement les personnes de la motricité, de la parole et de leur personnalité. Un coupable fréquent dans ces pathologies est une protéine appelée TDP-43, qui s’agglomère au mauvais endroit à l’intérieur des cellules nerveuses. Cette étude utilise un petit ver, Caenorhabditis elegans, pour observer ce qui arrive chez des animaux vivants lorsque le TDP-43 quitte son emplacement habituel et s’accumule dans le cytoplasme. En se concentrant sur un petit groupe bien caractérisé de neurones producteurs de sérotonine, les chercheurs montrent que le comportement peut se dérégler bien avant que les neurones ne meurent visiblement — offrant une fenêtre sur les stades précoces et les plus traitables de la maladie. 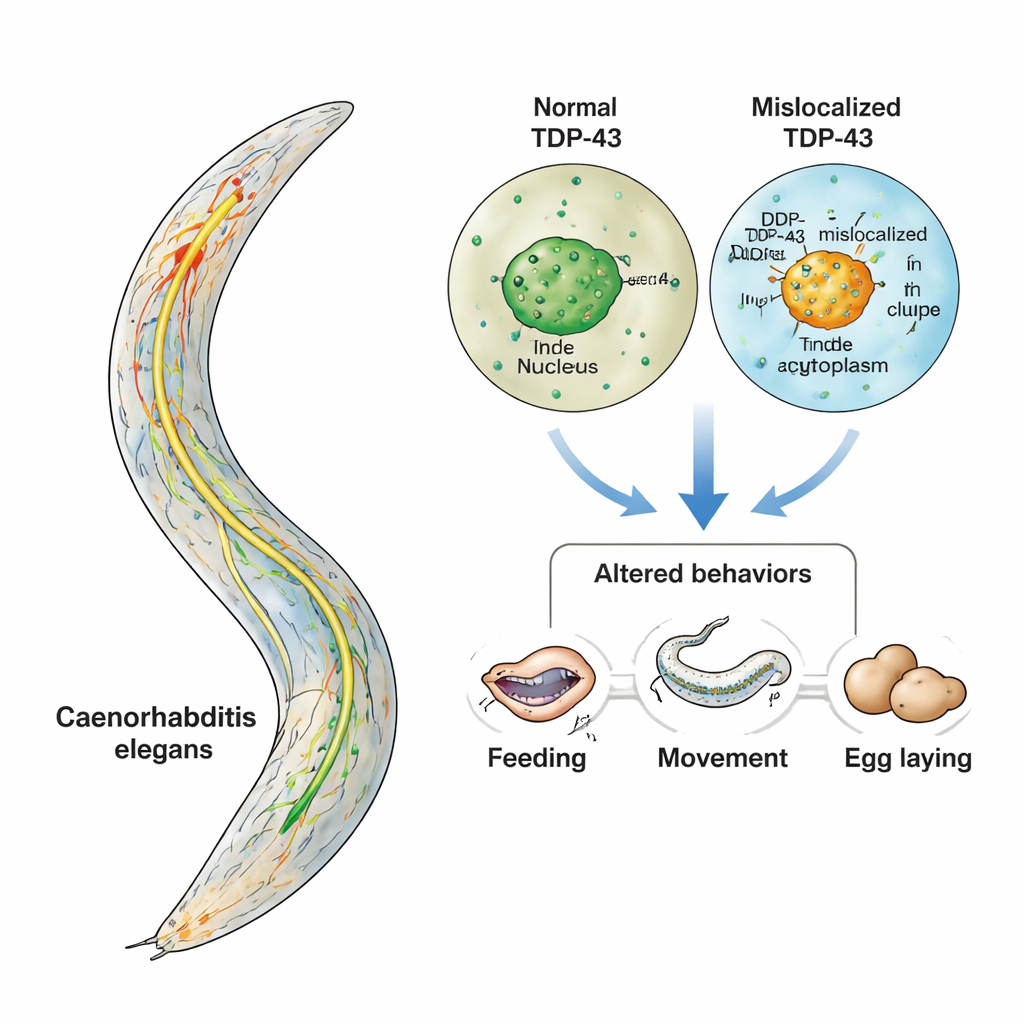
Une protéine qui s’agglomère et un messager chimique
Le TDP-43 réside normalement dans le noyau, où il aide à gérer l’ARN, les copies actives des instructions génétiques de la cellule. Dans la SLA et la DFT, toutefois, le TDP-43 quitte souvent le noyau, s’accumule dans le cytoplasme et forme des agrégats collants. Parallèlement, des données issues de patients et de modèles murins suggèrent que la sérotonine, un messager chimique mieux connu pour son rôle dans l’humeur, est également perturbée dans ces maladies. Parce que la sérotonine influence de nombreux comportements — de l’alimentation au contrôle des mouvements — les auteurs ont posé une question ciblée : si le TDP-43 est mal localisé spécifiquement dans les neurones producteurs de sérotonine, ces neurones dysfonctionnent-ils d’une manière qui modifie le comportement, même avant leur dégénérescence ?
Reconfigurer un système nerveux simple
L’équipe s’est tournée vers C. elegans, un ver microscopique dont le système nerveux complet de 302 neurones a été soigneusement cartographié. Seules trois paires de ces neurones produisent de la sérotonine, et chaque paire contrôle un comportement bien défini : l’alimentation (pompage pharyngien), le ralentissement à la découverte de nourriture et la pondeuse. À l’aide d’outils génétiques, les chercheurs ont conçu des vers de sorte que seules ces cellules sérotoninergiques produisent le TDP-43 humain. Une souche exprimait la forme normale, localisée dans le noyau ; une autre exprimait une forme mutante dépourvue de son « adresse » nucléaire, forçant le TDP-43 à s’accumuler dans le cytoplasme. Comme tous les autres neurones restaient intacts, tout changement de comportement pouvait être attribué directement à un problème dans ce circuit minuscule et unique.
Le comportement se dégrade avant la mort neuronale
Au travers de plusieurs tests, les vers modifiés se comportaient de manière anormale, de façon très similaire à une perte partielle ou complète de sérotonine. Les vers exprimant la forme cytoplasmique de TDP-43 présentaient un pompage de l’organe alimentaire plus lent et rythmique, une moindre propension à ralentir lorsqu’ils rencontraient de la nourriture après jeûne, et une réduction de la ponte. Les vers exprimant le TDP-43 normal, nucléaire, faisaient également moins bien que les animaux non modifiés, mais pas autant que ceux avec le TDP-43 cytoplasmique, révélant un gradient clair d’altération. De façon cruciale, lorsqu’on a testé les mêmes animaux dans un contexte où la sérotonine n’est pas requise — la nage en milieu liquide — leur locomotion était normale. Cela montre que le moteur locomoteur de base était intact et que les défauts étaient spécifiques aux comportements dépendant de la sérotonine plutôt qu’à une dégradation générale de l’état de santé. 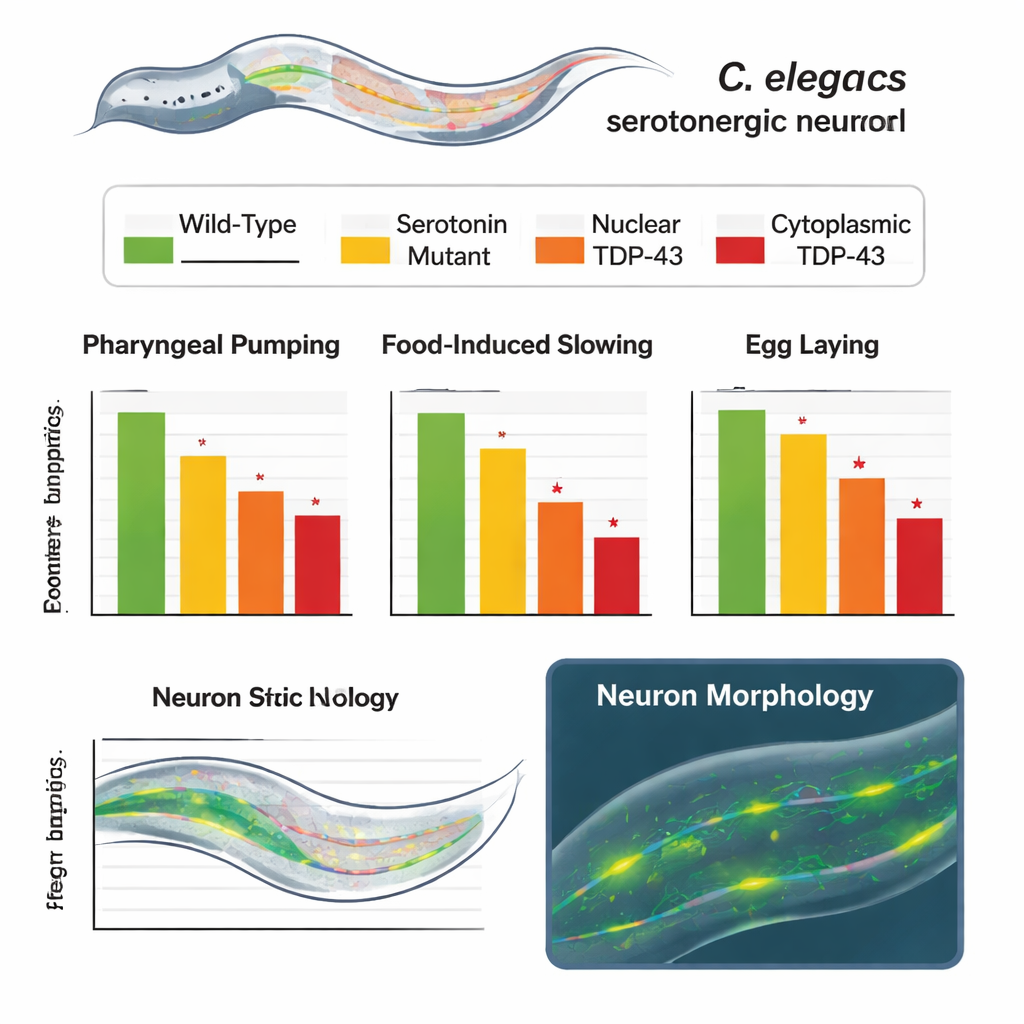
Des dommages cachés révélés par un test médicamenteux
Pour savoir si les neurones affectés étaient encore vivants et fonctionnels, les chercheurs ont utilisé la fluoxétine, mieux connue sous le nom de Prozac, un médicament qui renforce la signalisation de la sérotonine. Chez les vers normaux, la fluoxétine stimule fortement la ponte. Chez les vers génétiquement modifiés, le médicament augmentait également la ponte, mais la réponse était atténuée — surtout chez ceux portant le TDP-43 cytoplasmique. Ce profil suggère que les neurones sérotoninergiques pouvaient encore libérer des signaux, mais de façon moins efficace. L’imagerie microscopique racontait une histoire similaire : les neurones producteurs de sérotonine semblaient structurellement normaux, sans perte des corps cellulaires ni distorsions majeures de leurs branches, et leur fluorescence globale — un indicateur de santé cellulaire — était comparable à celle des vers témoins.
Signes précoces d’alerte et nouvelles opportunités
Pris ensemble, les résultats dessinent un tableau dans lequel un TDP-43 mal localisé peut perturber gravement le fonctionnement des neurones sérotoninergiques tout en les laissant apparemment intacts à l’œil. Chez le ver, le comportement se dérègle — alimentation, ajustement du mouvement et reproduction — avant toute mort neuronale visible. Cela fait écho aux observations cliniques selon lesquelles des changements subtils de comportement et d’humeur précèdent souvent l’atrophie cérébrale évidente dans les maladies neurodégénératives humaines. En offrant un système simple et génétiquement accessible où des défauts précoces et spécifiques aux circuits peuvent être mesurés précisément, ce modèle de ver pourrait aider les scientifiques à explorer comment le TDP-43 perturbe la fonction neuronale et à tester des thérapies visant à sauver les neurones durant cette fenêtre vulnérable et pré-dégénérative.
Citation: Lacour, A., Vassallu, F., Romussi, S. et al. Cytoplasmic TDP-43 leads to early behavioral impairments without neurodegeneration in a serotonergic neuron-specific C. elegans model. Sci Rep 16, 6068 (2026). https://doi.org/10.1038/s41598-026-36138-5
Mots-clés: TDP-43, neurones sérotoninergiques, C. elegans, SLA et DFT, neurodégénérescence