Clear Sky Science · fr
Le paysage transcriptionnel unicellulaire du poumon pédiatrique atteint de fibrose kystique à partir de spécimens respiratoires peu invasifs
Pourquoi cela compte pour les enfants atteints de fibrose kystique
La fibrose kystique est surtout connue pour la présence de mucus épais et les infections pulmonaires, mais derrière ces symptômes se joue une lutte complexe entre les cellules immunitaires et le revêtement fragile des voies aériennes. Cette étude s’intéresse à cette lutte chez l’enfant, cellule par cellule, à partir de petits échantillons prélevés lors de contrôles pulmonaires de routine. En cartographiant les types cellulaires présents et leur niveau d’activité, les chercheurs montrent que des schémas délétères d’inflammation s’installent tôt dans la vie et peuvent être difficiles à inverser, même avec des médicaments modernes qui corrigent le défaut génétique initial.
Observer les poumons des enfants une cellule à la fois
Pour explorer ce qui se passe à l’intérieur des poumons des enfants, l’équipe a utilisé des outils peu invasifs lors d’une bronchoscopie flexible — des procédures que ces patients subissaient déjà pour des raisons médicales. Ils ont délicatement frotté la surface interne de la trachée et des bronches et collecté le liquide de lavage provenant des régions plus profondes des poumons. Ces échantillons provenaient de deux enfants atteints de fibrose kystique (un nourrisson et un adolescent) et de trois enfants témoins appariés par âge. Grâce au séquençage ARN unicellulaire, une technique qui lit les gènes activés dans des milliers de cellules individuelles, ils ont construit une carte à haute résolution des cellules immunitaires et des cellules tapissant les voies aériennes de chaque enfant. 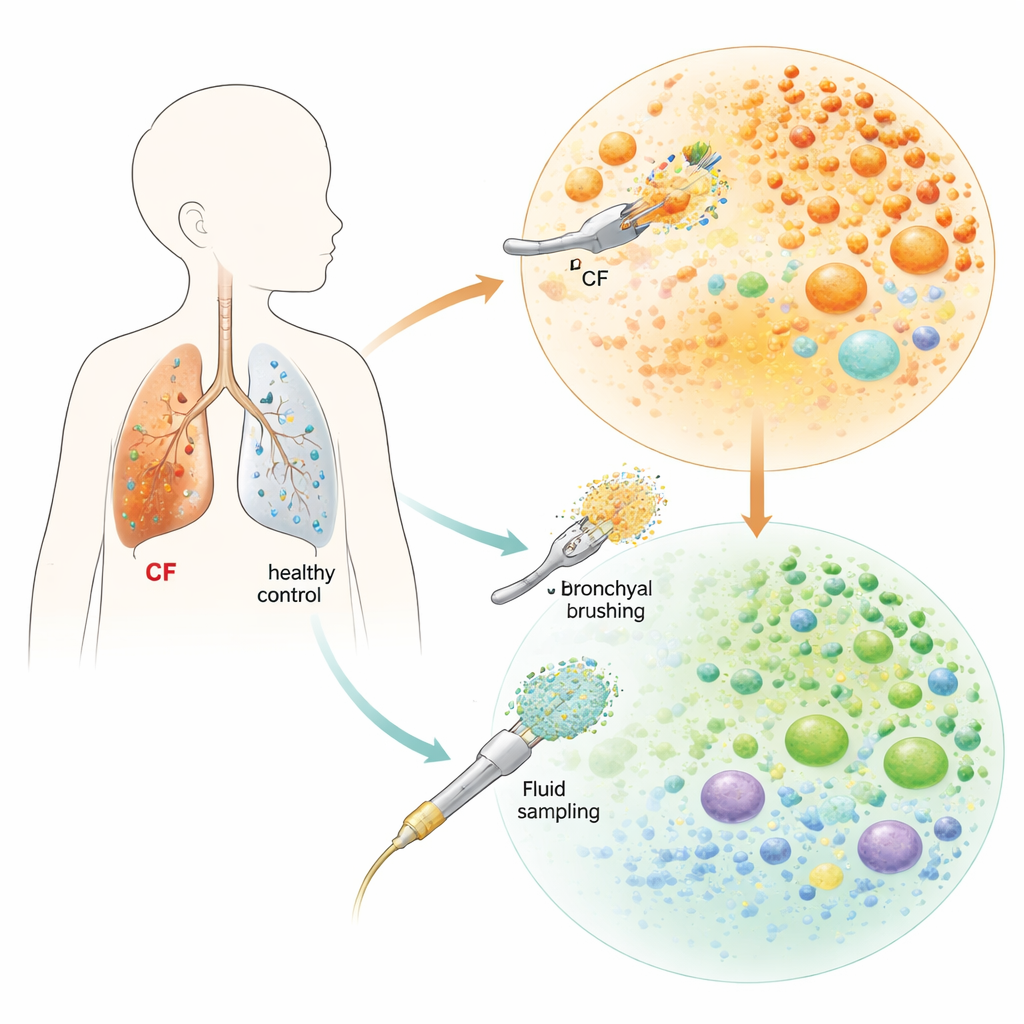
Un terrain occupé par des cellules immunitaires « premiers intervenants »
Chez les enfants sans fibrose kystique, les échantillons de lavage pulmonaire étaient dominés par des macrophages — des cellules nettoyeuses qui patrouillent les espaces aériens et contribuent au maintien de l’équilibre. En revanche, chez les enfants atteints de fibrose kystique, on observait un basculement net vers les neutrophiles, des globules blancs « premiers intervenants » très réactifs qui peuvent abîmer les tissus lorsqu’ils persistent. Non seulement les neutrophiles étaient plus nombreux, mais ils apparaissaient sous plusieurs formes distinctes. On a identifié des formes immatures, des cellules inflammatoires fortement activées et un sous-ensemble remarquable marqué par des protéines de réponse au stress connues sous le nom de protéines de choc thermique. Si ces réponses au stress peuvent débuter comme protectrices, elles risquent d’enfermer les neutrophiles dans un état agressif et durable qui entretient l’inflammation et peut provoquer les lésions des voies respiratoires observées dans la fibrose kystique.
Des défenseurs enflammés et des renforts manquants
Les macrophages restant dans les poumons atteints de fibrose kystique présentaient eux aussi des caractéristiques différentes. Plutôt qu’un mélange des types ménagers courants observés dans le groupe témoin, les échantillons de fibrose kystique étaient enrichis en macrophages produisant de forts signaux immunitaires, suggérant une orientation plus inflammatoire. Parallèlement, on trouvait relativement peu de cellules T — un autre bras clé du système immunitaire — dans le liquide des voies aériennes des enfants atteints. Des travaux antérieurs ont montré que les neutrophiles peuvent priver les cellules T des nutriments dont elles ont besoin pour fonctionner, les écartant ainsi de l’airway. Cette combinaison de neutrophiles agressifs, de macrophages activés et de cellules T rares peut aider à expliquer pourquoi les poumons des patients atteints de fibrose kystique restent enflammés et sujets aux infections pendant de nombreuses années.
Un revêtement des voies respiratoires qui prend part au combat
Les frottis ont permis aux chercheurs d’examiner les cellules qui tapissent les voies aériennes : les cellules basales (capables de régénérer l’épithélium), les cellules ciliées (munies de projections semblables à des poils qui balayent le mucus) et les cellules sécrétoires (qui produisent mucus et molécules protectrices). La répartition globale de ces types cellulaires était similaire entre enfants atteints et témoins, mais leur comportement différait. Dans la fibrose kystique, les cellules sécrétoires ont activé des gènes liés à la défense immunitaire et à l’activité antimicrobienne, suggérant qu’elles sont suractivées dans le cadre de la réponse inflammatoire. Les cellules ciliées ont également exprimé des gènes associés à l’inflammation et à la résistance à une forme de mort cellulaire liée au fer et au stress oxydatif. Ensemble, ces profils indiquent que la surface des voies aériennes n’est pas un simple spectateur, mais un participant actif et enflammé du processus pathologique. 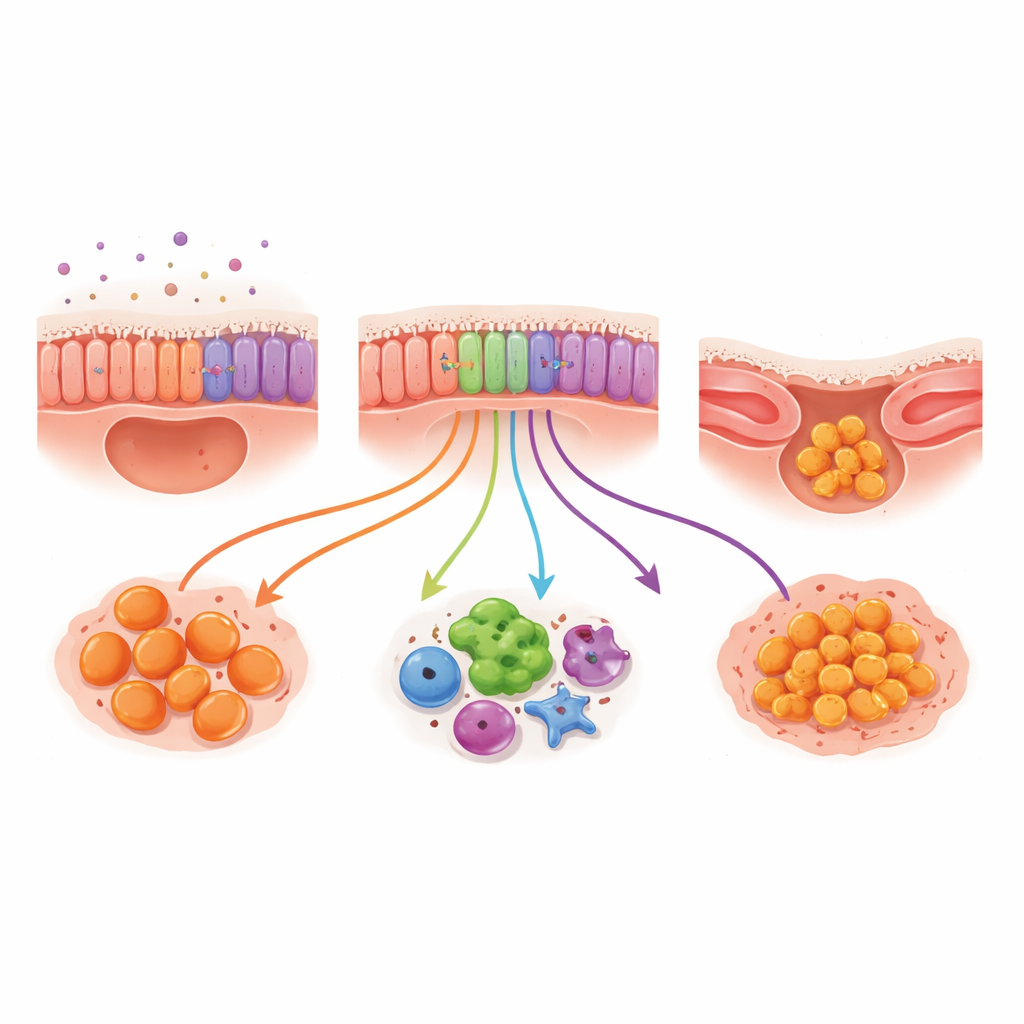
Des dialogues cellulaires qui alimentent les lésions pulmonaires
Pour comprendre comment les cellules épithéliales et les neutrophiles s’influencent mutuellement, l’équipe a analysé les « conversations » entre elles — des signaux émis par un type cellulaire et reçus par un autre. Ils ont constaté que les cellules épithéliales faisaient souvent office d’émetteurs, utilisant plusieurs systèmes moléculaires pour atteindre les neutrophiles. Certains de ces signaux contribuent probablement à calmer l’inflammation, tandis que d’autres encouragent l’afflux, l’activation et la phagocytose par les neutrophiles. Cette dynamique de poussée et de tiraillement suggère que l’épithélium tente d’équilibrer contrôle des dommages et défense, mais dans la fibrose kystique les signaux pro-inflammatoires semblent l’emporter, maintenant le poumon dans un état chronique de lésion latente.
Pourquoi les changements précoces sont difficiles à inverser
Un constat clé est que ces schémas inflammatoires étaient présents aussi bien chez le nourrisson que chez l’adolescent qui prenait un médicament avancé contre la fibrose kystique visant à améliorer la protéine défectueuse. Malgré cette thérapie ciblée, les cellules pulmonaires de l’adolescent ressemblaient davantage à celles du nourrisson non traité qu’à celles des enfants témoins. Cela laisse entendre qu’une fois que des lésions structurelles et une inflammation enracinée se sont installées, restaurer la fonction protéique sous-jacente peut ne pas suffire à réinitialiser le paysage immunitaire et épithélial. L’étude montre également que des prélèvements doux des voies aériennes, combinés au séquençage unicellulaire et à l’analyse spatiale des gènes, permettent de suivre ces changements dans le temps. Cette approche pourrait aider à concevoir et tester de nouveaux traitements anti-inflammatoires et antimicrobiens visant à préserver la structure pulmonaire dès les premiers instants de la vie.
Citation: Sun, Y., Vicencio, A.G., Beasley, M.B. et al. The single-cell transcriptional landscape of the pediatric cystic fibrosis lung from minimally invasive respiratory specimens. Sci Rep 16, 8113 (2026). https://doi.org/10.1038/s41598-026-36125-w
Mots-clés: poumon atteint de fibrose kystique, inflammation neutrophilique, séquençage ARN unicellulaire, épithélium des voies respiratoires, bronchoscopie pédiatrique