Clear Sky Science · fr
Les positions R5 et R7 sur les échafaudages fluoroquinolones provoquent la disruption des filaments F-actine
Transformer des antibiotiques en aides pour le cerveau
De nombreux troubles cérébraux courants, de la maladie d’Alzheimer à la maladie de Parkinson, partagent un coupable discret : de minuscules tiges structurelles à l’intérieur des neurones qui se bloquent et se rigidifient avec le temps. Ces tiges sont composées d’une protéine appelée actine, normalement une composante flexible du squelette intracellulaire. Cette étude explore une possibilité surprenante : qu’une classe bien connue d’antibiotiques, les fluoroquinolones, puisse être reconfigurée pour désassembler progressivement ces faisceaux d’actine nuisibles et, potentiellement, contribuer à protéger le cerveau.
Quand l’échafaudage cellulaire dysfonctionne
Les cellules cérébrales saines remodèlent en permanence leur squelette interne pour établir et ajuster leurs connexions. Les filaments d’actine sont au cœur de ce processus, se formant et se dissolvant selon les besoins. Sous stress, cependant, l’actine peut se verrouiller en agrégats en forme de tige qui bouchent la cellule, perturbent le transport de cargaisons vitales et favorisent l’accumulation de protéines liées aux maladies comme l’amyloïde et la protéine tau. Au fil des années, ces tiges peuvent évoluer en structures denses appelées corps de Hirano, fréquemment observées dans les cerveaux de personnes atteintes de diverses affections neurodégénératives. Étant donné que les médicaments actuels ciblant l’actine sont souvent extrêmement toxiques, les chercheurs cherchent des petites molécules plus sûres capables d’assouplir ces agrégats sans nuire aux cellules.
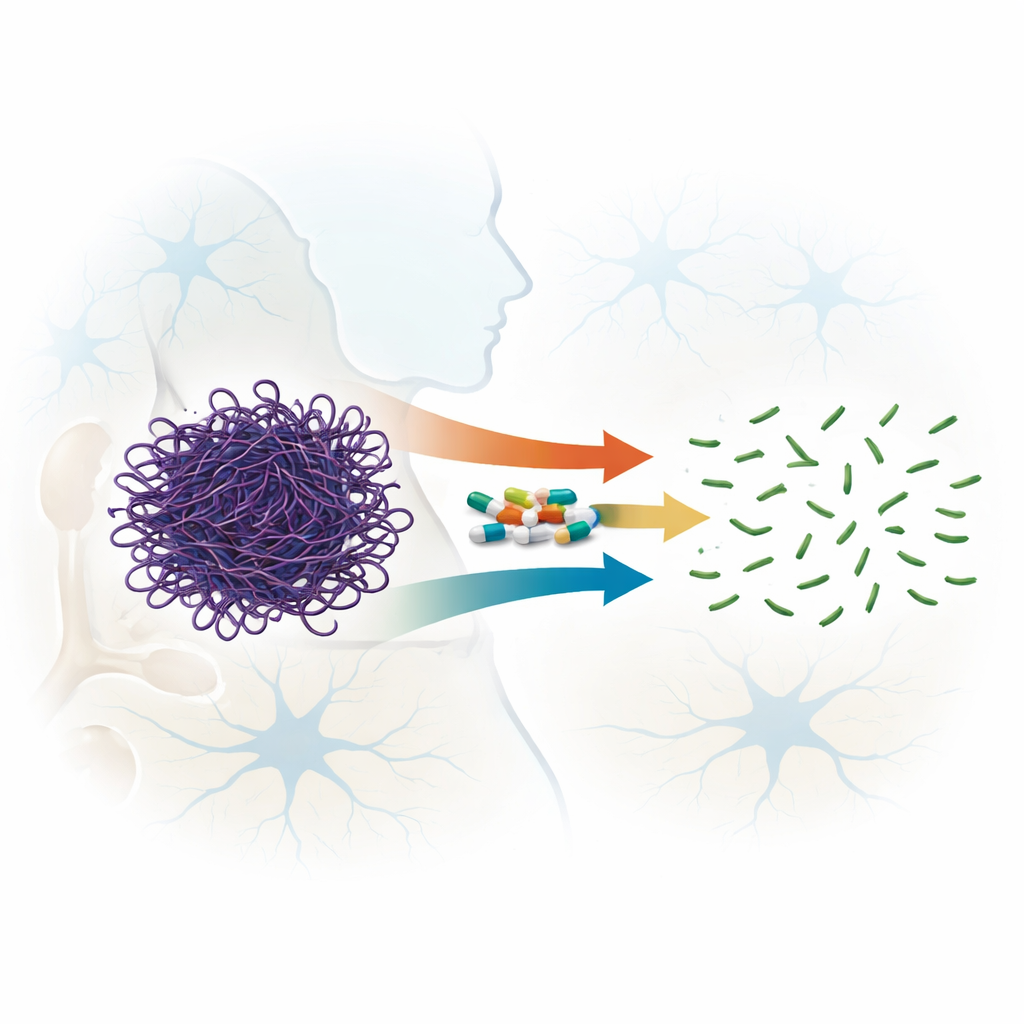
Un talent inattendu de médicaments familiers
Les fluoroquinolones sont des antibiotiques à large spectre utilisés dans le monde entier pour traiter les infections, et certains membres récents de cette famille peuvent traverser la barrière hémato‑encéphalique. Des indices antérieurs suggéraient que certaines fluoroquinolones pouvaient déstabiliser les filaments d’actine. Dans ce travail, les auteurs ont comparé systématiquement sept composés apparentés, couvrant quatre générations de la famille, afin d’évaluer leur capacité à fragmenter des filaments d’actine préformés plutôt que de simplement empêcher leur formation. À l’aide de mesures de diffusion de la lumière, de microscopie électronique et de filtration sur gel, ils ont montré que tous les médicaments testés pouvaient perturber les filaments d’actine, mais avec des intensités très variables. Deux molécules, la sparfloxacine (composé de troisième génération) et la moxifloxacine (quatrième génération), se sont distinguées en scindant rapidement et de façon irréversible de longs filaments en morceaux beaucoup plus petits, même à des rapports médicament/protéine relativement faibles.
Observer l’effondrement des filaments
Des images à haute résolution et des tests biophysiques ont révélé comment les filaments évoluent sous traitement médicamenteux. La microscopie électronique a montré que l’actine non traitée forme de longs brins continus, tandis que les fluoroquinolones efficaces les convertissent en fragments courts et dispersés. Les membres moins puissants produisaient des filaments coudés et pliés sans les rompre complètement. Des mesures thermiques de la stabilité protéique ont confirmé cette disruption physique : une fois traitée, l’actine présentait un comportement plus proche de sa forme libre et non assemblée, avec des températures de fusion plus basses, alors que sa structure de base restait pratiquement inchangée. Cela suggère que les médicaments n’entraînent pas le dépliement ni la destruction de l’actine elle‑même, mais qu’ils séparent principalement la manière dont les unités s’assemblent en filaments.
Approfondir la prise moléculaire
Pour comprendre pourquoi certaines fluoroquinolones sont plus actives que d’autres, l’équipe a combiné des expériences avancées de résonance magnétique nucléaire avec des simulations informatiques des interactions médicament–protéine. Ils ont constaté que tous les composés s’appuient sur un « noyau » en anneau partagé pour entrer en contact avec l’actine, en particulier à deux positions de ce noyau qui touchent à répétition le filament. Toutefois, des groupes chimiques additionnels attachés à des sites spécifiques — désignés R5 et R7 — influencent fortement la fermeté et la localisation de la liaison de chaque molécule. Chez les perturbateurs les plus efficaces, ces positions portent un groupe amino et des systèmes d’anneaux volumineux qui s’insinuent dans une petite poche à l’interface entre brins d’actine voisins. Là, ils perturbent des contacts stabilisateurs clés, y compris un pont salin important qui contribue normalement à maintenir les filaments ensemble.
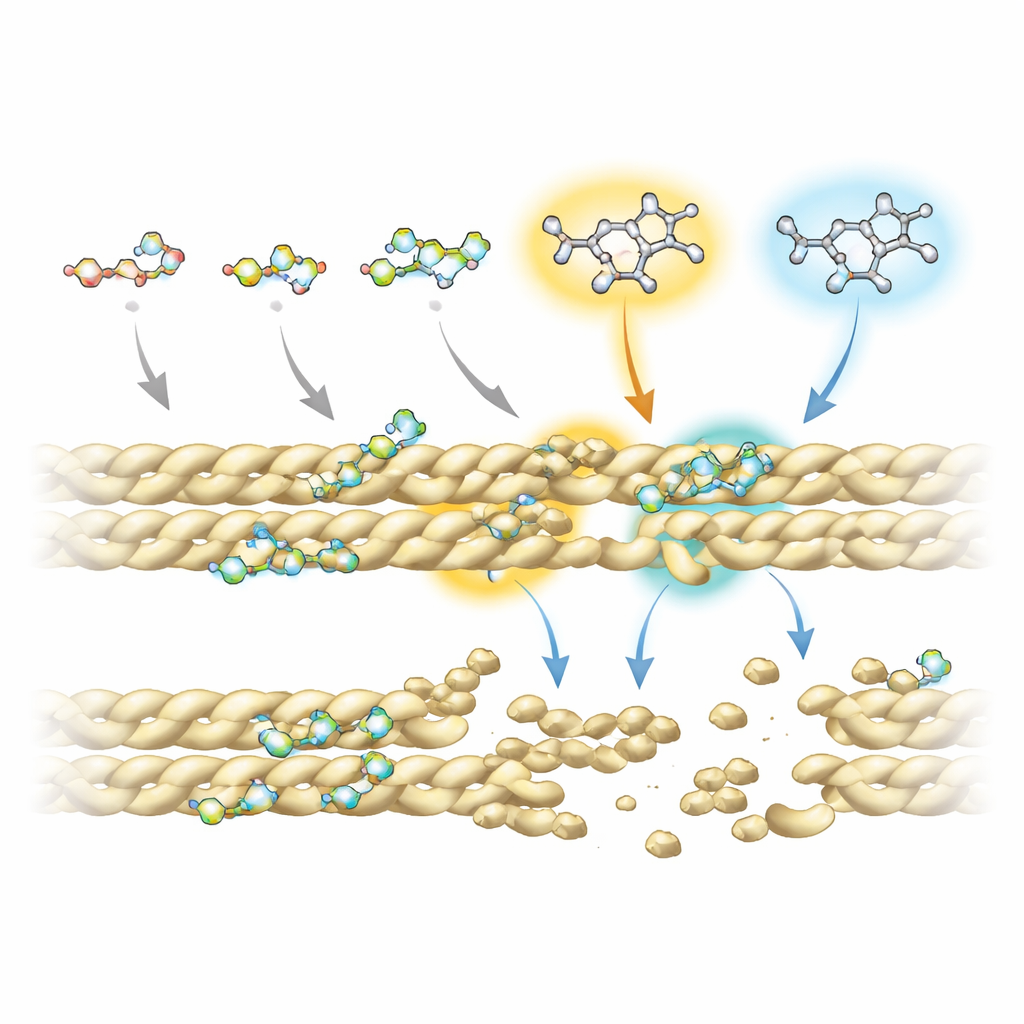
Des cellules de levure aux thérapies futures
Les chercheurs ont également testé les médicaments sur une souche de levure qui accumule naturellement des faisceaux d’actine, reproduisant certains aspects des cellules malades. Au microscope, les levures non traitées présentaient de gros agrégats d’actine lumineux, tandis que les cellules exposées aux fluoroquinolones — en particulier la sparfloxacine, la moxifloxacine et, à doses plus élevées, l’acide nalidixique — montraient des motifs beaucoup plus diffus et ponctués, indiquant que les faisceaux avaient été désassemblés. Il est important de noter que l’action des médicaments semblait relativement douce : ils affaiblissaient le compactage des filaments sans déformer grossièrement la forme sous‑jacente de l’actine, et leur liaison était moins forte que celle des toxines classiques de l’actine, ce qui pourrait réduire le risque d’effets indésirables sévères.
Concevoir des médicaments ciblant l’actine plus intelligents
Dans l’ensemble, cette étude montre que de légères modifications d’antibiotiques bien connus peuvent transformer radicalement leur interaction avec le squelette interne de la cellule. En identifiant les positions R5 et R7 comme de véritables « réglages » clés pour la disruption de l’actine et la pénétration cérébrale, les auteurs esquissent une feuille de route pour créer de nouvelles molécules inspirées des fluoroquinolones qui démantèleraient sélectivement les agrégats d’actine nuisibles. Bien que ces résultats constituent une preuve de principe précoce en laboratoire, ils ouvrent la possibilité que de futurs médicaments dérivés d’antibiotiques familiers puissent aider à éliminer l’échafaudage toxique des neurones et ralentir ou prévenir certaines formes de neurodégénérescence.
Citation: Gupta, R.J., Nair, H., Sarhadi, T.R. et al. R5 and R7 positions on fluoroquinolone scaffolds drive F-actin filament disruption. Sci Rep 16, 9517 (2026). https://doi.org/10.1038/s41598-026-36089-x
Mots-clés: agrégats d’actine, antibiotiques fluoroquinolones, maladies neurodégénératives, réaffectation de médicaments, cytosquelette