Clear Sky Science · fr
Expression du récepteur de la sphingosine-1-phosphate 1 dans le cerveau du paludisme cérébral mortel
Pourquoi ce lien cerveau–paludisme est important
Le paludisme cérébral est l’une des complications les plus mortelles de l’infection palustre, tuant de nombreux patients même lorsqu’ils reçoivent des traitements modernes. Cette étude examine le cerveau pour comprendre pourquoi les vaisseaux sanguins commencent à fuir et à défaillir chez les malades les plus graves. En se concentrant sur une molécule lipidique de signalisation appelée sphingosine-1-phosphate (S1P) et son récepteur S1PR1, les chercheurs se demandent si ce dialogue chimique entre le sang et le cerveau pourrait expliquer qui survit, qui meurt, et comment mieux protéger le cerveau dans de futures thérapies.
Ce qui arrive au cerveau dans les formes graves de paludisme
Dans le paludisme cérébral, les globules rouges infectés par le parasite Plasmodium falciparum deviennent adhésifs et se fixent à la paroi des petits vaisseaux sanguins cérébraux. L’équipe a examiné des tissus cérébraux conservés de personnes décédées du paludisme et les a comparés à des patients atteints de paludisme non cérébral plus bénin et à des témoins sans paludisme. Dans les cas cérébraux fatals, ils ont observé des vaisseaux encombrés de globules rouges remplis de parasites, de micro-hémorragies en points, des zones d’hémorragie en anneau et des amas de cellules de soutien connus sous le nom de granulomes de Dürck. Ces modifications indiquent des vaisseaux bouchés, une mauvaise oxygénation et une atteinte de la barrière hémato‑encéphalique normalement étanche qui maintient la stabilité de l’environnement cérébral. 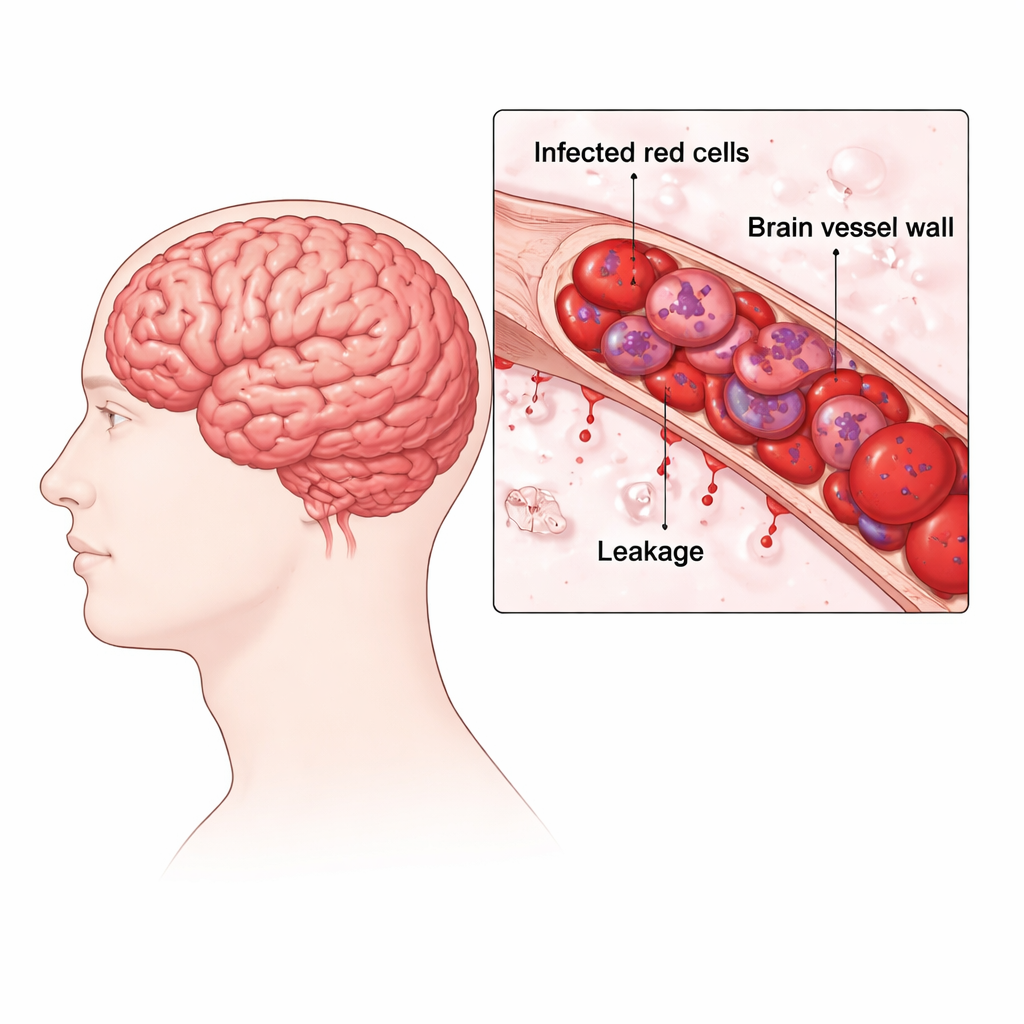
Un gardien chimique de la fermeté des vaisseaux
Dans des conditions saines, la S1P — principalement stockée dans les globules rouges et les plaquettes — aide à maintenir l’étanchéité des vaisseaux. Elle agit en se liant à des récepteurs tels que S1PR1 à la surface des cellules qui tapissent les vaisseaux et des cellules cérébrales, renforçant les jonctions entre elles. Les chercheurs ont mesuré les niveaux de S1P dans des échantillons de sang et ont constaté une chute marquée chez les patients atteints de paludisme cérébral : leurs taux de S1P étaient environ quatre fois plus faibles que chez les personnes sans paludisme, et environ la moitié de ceux des patients atteints de paludisme non cérébral. Cela suggère que, à mesure que le paludisme détruit ou déforme les globules rouges et blesse les cellules vasculaires, la réserve de cette molécule protectrice diminue justement quand elle est la plus nécessaire.
Où et comment le récepteur s’active
Ensuite, l’équipe a utilisé l’immunohistochimie — une méthode de coloration qui rend visibles des protéines spécifiques au microscope — pour cartographier S1PR1 dans le cerveau. Dans les cerveaux témoins sains et dans le paludisme non cérébral, la coloration pour S1PR1 était faible dans les neurones et les vaisseaux. En revanche, les cerveaux des patients atteints de paludisme cérébral présentaient une coloration intense de S1PR1 dans les cellules de la paroi vasculaire et dans les neurones, tandis que les cellules de soutien voisines appelées glies montraient peu ou pas de signal. Lorsque les scientifiques quantifièrent ceci, les « scores » de S1PR1 dans les vaisseaux et les neurones étaient nettement plus élevés dans le paludisme cérébral que dans les autres groupes. Plus il y avait de globules rouges remplis de parasites coincés dans les vaisseaux, plus l’expression de S1PR1 était élevée et plus le taux de S1P dans le sang était bas, révélant un lien étroit entre la charge parasitaire, l’activation du récepteur et la perte du signal protecteur. 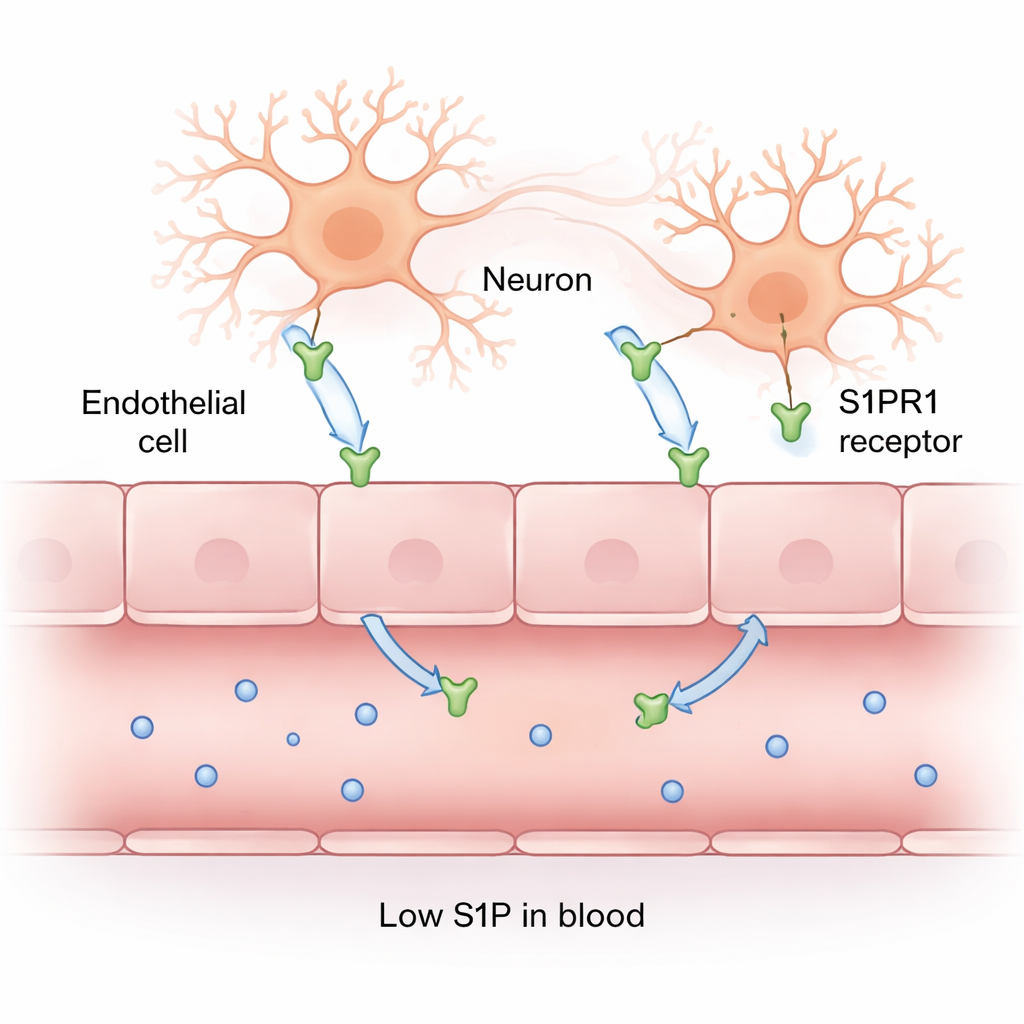
Assembler le cercle vicieux
Le schéma suggère un cercle vicieux possible. À mesure que les cellules infectées bouchent les vaisseaux cérébraux, le niveau d’oxygène diminue et l’inflammation s’amplifie. Les niveaux sanguins de S1P chutent, probablement parce que les globules rouges, les plaquettes et les cellules vasculaires endommagés ne peuvent plus maintenir les apports normaux. En parallèle, les cellules vasculaires et les neurones augmentent l’expression de S1PR1, peut‑être pour capter ce qui reste de S1P et tenter de restaurer la fonction barrière. Mais cette activation accrue du récepteur pourrait encore extraire la S1P de la circulation et même modifier la signalisation inflammatoire dans le cerveau. Le résultat est une fuite vasculaire aggravée, davantage d’hémorragies dans le tissu cérébral et une détérioration des lésions neurologiques.
Ce que cela pourrait signifier pour les traitements futurs
Pour un non-spécialiste, le message clé est que le système S1P–S1PR1 agit comme une « colle » stabilisatrice des vaisseaux sanguins cérébraux, et que cette colle semble céder dans le paludisme cérébral. Les patients qui meurent de cette affection présentent des taux de S1P très faibles dans le sang et des niveaux très élevés de son récepteur sur les vaisseaux cérébraux et les neurones. Cette étude ne prouve pas encore la causalité, mais elle renforce l’idée que des médicaments qui stimulent la signalisation de la S1P ou moduleraient finement S1PR1 — dont certains existent déjà pour d’autres maladies — pourraient un jour être utilisés en association avec des antipaludiques pour préserver l’intégrité des vaisseaux cérébraux et réduire la mortalité liée à cette maladie dévastatrice.
Citation: Srisook, C., Nintasen, R., Punsawad, C. et al. Expression of sphingosine-1-phosphate receptor 1 in the brain of fatal cerebral malaria. Sci Rep 16, 5641 (2026). https://doi.org/10.1038/s41598-026-36072-6
Mots-clés: paludisme cérébral, barrière hémato-encéphalique, sphingosine-1-phosphate, cellules endothéliales, inflammation cérébrale