Clear Sky Science · fr
Capteur métamatériau non hermitien Thue–Morse amélioré au graphène exploitant un point exceptionnel pour la détection de biomarqueurs du cancer
Pourquoi un meilleur capteur contre le cancer est important
Détecter le cancer précocement peut faire la différence entre un traitement simple et une maladie potentiellement mortelle. De nombreux tests modernes reposent sur le marquage du sang ou des tissus avec des colorants ou des molécules spéciales, ce qui peut être lent, coûteux et complexe. Cet article décrit un nouveau type de capteur optique — une puce mince et stratifiée qui utilise la lumière, des matériaux spécifiques et des couches de graphène ultrafines — pour détecter des variations subtiles liées aux cellules cancéreuses et aux biomarqueurs sans ajout d’étiquette. Le résultat est un dispositif compact qui pourrait un jour aider les médecins à repérer le cancer plus tôt et de manière plus fiable.
Empiler des couches guidant la lumière comme un puzzle
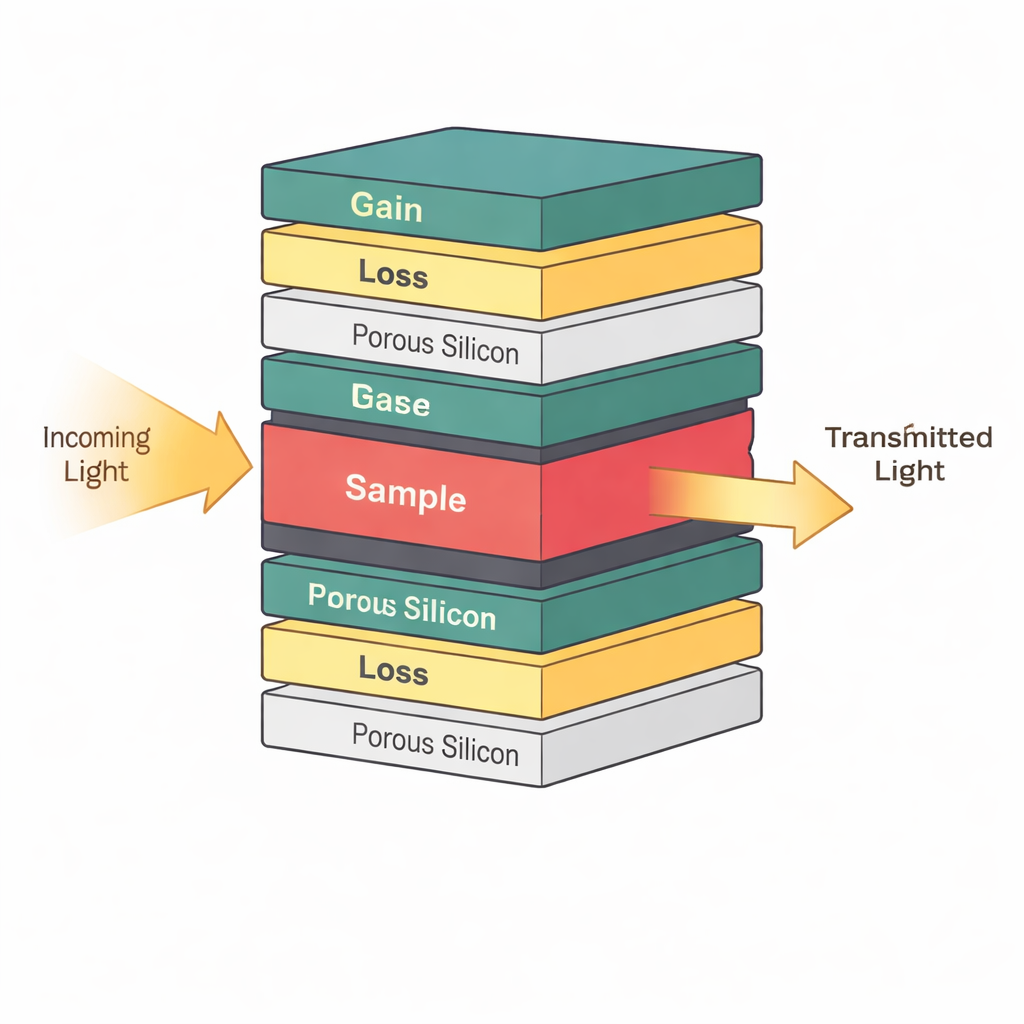
Au cœur du dispositif se trouve un empilement soigneusement conçu de couches ultrafines qui guident et piègent la lumière. Plutôt que d’ordonner ces couches selon un motif parfaitement répétitif, les auteurs utilisent une recette mathématique appelée suite de Thue–Morse, qui se situe entre l’ordre et le désordre. Cette quasi-structure crée des « zones favorables » où la lumière devient fortement confinée dans des régions étroites de l’empilement. Au centre de cette structure, ils insèrent une couche qui contient l’échantillon réel — par exemple, un fluide contenant des cellules saines ou cancéreuses. Parce que la lumière se concentre autour de cette couche centrale, même de petits changements dans les propriétés optiques de l’échantillon, comme son indice de réfraction, peuvent déplacer de façon notable la transmission lumineuse du dispositif.
Utiliser gain, perte et points exceptionnels pour amplifier les signaux
Le capteur tire également parti d’une idée puissante de la photonique moderne appelée symétrie parité-temps. En termes simples, certaines couches de l’empilement amplifient légèrement la lumière tandis que d’autres l’absorbent un peu, arrangées de manière à équilibrer gain et perte autour du centre. Quand cet équilibre est réglé précisément, le système atteint ce que les physiciens appellent un point exceptionnel, où deux modes lumineux fusionnent en un seul. Près de ce point, le dispositif devient extraordinairement sensible : une petite perturbation de l’échantillon — comme un léger changement de concentration de cellules cancéreuses — provoque un déplacement disproportionné du signal lumineux transmis. Les auteurs montrent que fonctionner à proximité de cette condition spéciale rend le pic de résonance dans le spectre beaucoup plus aigu, ce qui améliore directement la finesse avec laquelle le capteur peut distinguer différents tissus ou niveaux de biomarqueurs.
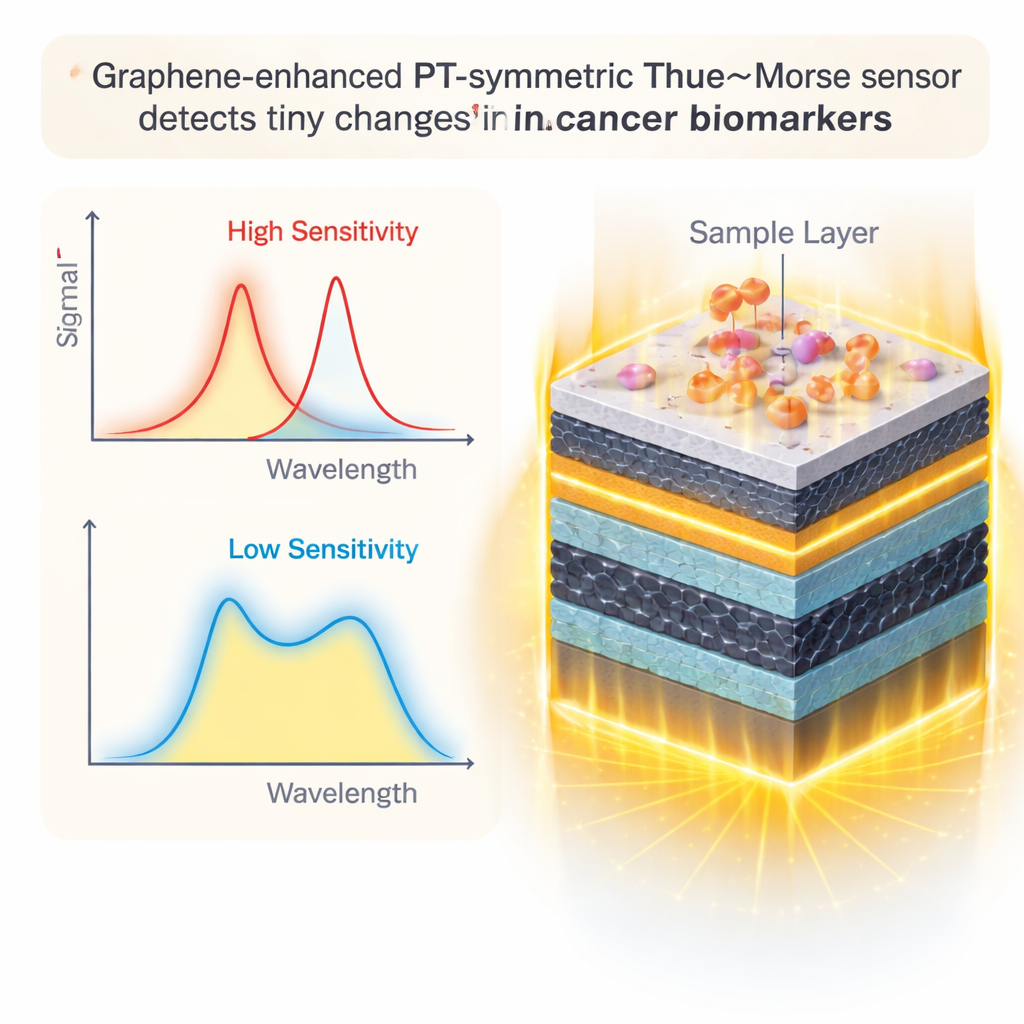
Des couches de graphène comme peau ancrant la lumière
Pour améliorer encore les performances, les chercheurs ajoutent des feuilles de graphène — des couches de carbone d’un seul atome d’épaisseur — à des interfaces clés autour de l’échantillon. Le graphène est célèbre non seulement pour sa résistance et sa conductivité, mais aussi pour la façon dont il interagit avec la lumière. En ajustant ses propriétés électriques, l’équipe peut faire en sorte que le graphène attire la lumière encore plus près de la région d’échantillonnage et réduise les pertes indésirables. Des simulations soignées révèlent que lorsque les principaux réglages du graphène — son potentiel chimique et son temps de relaxation — sont fixés à des valeurs spécifiques, la résonance devient plus étroite et plus réactive. L’ajout jusqu’à quatre couches de graphène autour de l’échantillon offre le meilleur compromis : le signal devient plus fort et plus précis sans être excessivement amorti par une absorption supplémentaire.
Équilibrer détails de conception et fabrication réelle
Le dispositif utilise aussi des couches de silicium poreux, percées de minuscules trous, pour accueillir le matériel biologique et augmenter la surface où les cellules et les biomarqueurs peuvent se fixer. Les auteurs font varier de manière systématique des paramètres de conception pratiques tels que l’épaisseur des couches, la porosité et l’angle de la lumière incidente, et ils vérifient comment de petites erreurs de fabrication pourraient affecter les performances. Ils constatent que le capteur reste stable lorsque ces paramètres varient d’environ deux pour cent, une gamme que les techniques de nanofabrication actuelles peuvent raisonnablement atteindre. À mesure que le nombre de couches de graphène augmente, la sensibilité s’améliore généralement, mais un nombre trop élevé finit par introduire une perte excessive. L’étude identifie un compromis optimal de configuration et de conditions de fonctionnement qui pourrait orienter de futurs prototypes expérimentaux.
Ce que cela pourrait signifier pour le diagnostic futur
En termes numériques clairs, le capteur proposé peut déplacer son signal optique de plus de 1000 nanomètres pour une variation unitaire de l’indice de réfraction de l’échantillon, avec une limite de détection suffisamment fine pour percevoir de très petites différences entre cellules saines et cancéreuses. Bien que certains systèmes spécialisés à base de fibres puissent atteindre des limites encore plus basses, ils sont souvent encombrants ou difficiles à intégrer. En revanche, ce design est compact, compatible avec le silicium et adapté à l’intégration sur puce avec des canaux microfluidiques et des revêtements biochimiques ciblant des marqueurs cancéreux spécifiques. En termes simples, ce travail montre comment la combinaison d’un motif de couches inhabituel, d’un équilibre gain-perte et de « peaux » de graphène autour de la région de détection peut transformer une petite puce optique en un détecteur de cancer très réactif et sans étiquette — une avancée prometteuse vers des outils diagnostiques plus rapides et plus accessibles.
Citation: Mohammadpour, A., Vala, A.S. & Barvestani, J. Graphene-enhanced non-Hermitian Thue–Morse metamaterial sensor exploiting exceptional point for cancer biomarker detection. Sci Rep 16, 6521 (2026). https://doi.org/10.1038/s41598-026-36067-3
Mots-clés: biocapteur pour le cancer, photonique au graphène, capteur optique, cristal photoniqe, détection de biomarqueurs