Clear Sky Science · fr
Analyse protéomique du secretome des cellules progénitrices endothéliales identifie Serpine 1 comme un régulateur puissant de l’ostéogenèse
Réparer un os cassé sans greffes donneuses
Lorsqu’un os est gravement fracturé ou qu’un segment manque, les chirurgiens peinent souvent à restaurer à la fois la résistance et la forme. Les options actuelles — prélever de l’os ailleurs dans le corps ou utiliser des greffes synthétiques — peuvent être douloureuses, risquées et pas toujours efficaces. Cette étude explore une autre idée : plutôt que de transplanter des cellules, peut-on délivrer uniquement les protéines naturelles adéquates pour déclencher les mécanismes intrinsèques de construction osseuse du corps ?
Pourquoi certaines blessures osseuses refusent de guérir
La plupart des fractures se consolident seules, mais les larges pertes de substance osseuse — causées par des traumatismes, des tumeurs ou une atrophie sévère de la mâchoire — ne cicatrisent souvent pas. Dans ces cas, l’organisme ne dispose tout simplement pas d’un nombre suffisant de cellules vasculaires locales et de cellules souches ostéogéniques pour reconstruire le segment manquant. Les chercheurs en ingénierie tissulaire tentent de résoudre ce problème en combinant trois ingrédients : des cellules vivantes capables de former du nouvel os, un échafaudage qui leur sert de support et des signaux qui leur indiquent quoi faire. Les greffes cellulaires peuvent fonctionner, mais elles sont coûteuses, fortement régulées et rarement pratiques pour un usage clinique courant. Cela a poussé les scientifiques à rechercher des solutions « sans cellules » basées sur des biomatériaux intelligents et des protéines choisies avec précision.
Signaux secrets des cellules bâtisseuses de vaisseaux
Les cellules progénitrices endothéliales sont des cellules rares dans le sang qui aident à former de nouveaux vaisseaux sanguins. Des travaux antérieurs ont montré que lorsqu’elles sont implantées à proximité de l’os, elles favorisent la réparation — principalement en émettant des signaux solubles plutôt qu’en se transformant elles-mêmes en tissu osseux. Dans la nouvelle étude, les auteurs ont collecté le milieu de culture dans lequel ces cellules avaient grandi et ont utilisé une analyse protéique avancée pour inventorier des centaines de molécules sécrétées. Ils se sont concentrés sur huit protéines fortement liées à la croissance vasculaire et à la formation osseuse. En utilisant des cellules souches de moelle osseuse humaines et des cellules endothéliales microvasculaires humaines en laboratoire, ils ont testé de manière systématique lesquelles de ces protéines stimulaient le mieux la prolifération cellulaire, dirigeaient la migration et déclenchaient le dépôt de minéraux similaires à l’os.
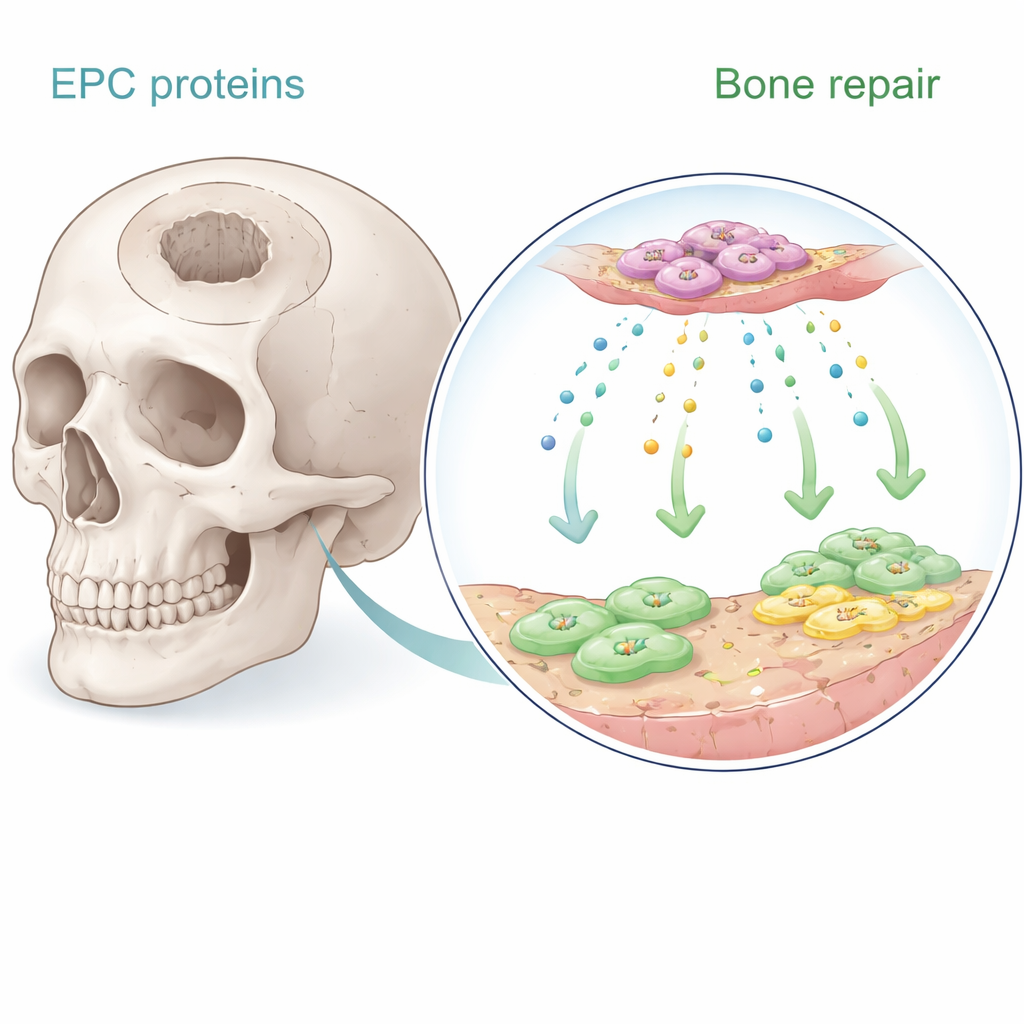
Une protéine surprenante prend la tête
Parmi les candidates, une protéine s’est distinguée : Serpine-1, mieux connue pour son rôle dans la régulation de la coagulation sanguine et la cicatrisation. En culture, la Serpine-1 a significativement augmenté la prolifération des cellules souches de la moelle osseuse et des cellules endothéliales de manière dépendante de la dose, surpassant à cet égard des facteurs de croissance bien connus tels que le BMP-2 et le SDF-1. Elle a aussi favorisé la maturation des cellules souches en ostéoblastes, comme le montrent des méthodes de coloration classiques révélant l’activité de la phosphatase alcaline et des dépôts minéraux riches en calcium. D’autres protéines, comme le facteur de croissance dérivé des plaquettes et le BMP-2, étaient plus efficaces pour encourager la migration cellulaire dans des tests de cicatrisation, mais la Serpine-1 offrait une combinaison rare : augmenter à la fois le nombre de cellules et leur comportement osteoformatif.
Transformer une protéine en implant pratique
Trouver une protéine prometteuse n’est que la moitié du défi ; il faut aussi la délivrer au site de la lésion de façon contrôlée. L’équipe a encapsulé la Serpine-1 à l’intérieur de microbilles biodégradables en un polymère médical appelé PLGA, puis a incorporé ces microsphères dans un gel de collagène souple. Cela a créé un échafaudage libérant lentement la protéine dans le temps. Ils l’ont testé chez la souris en forant un trou circulaire de 4 millimètres dans le crâne — une taille de défaut qui ne guérit pas spontanément. Certains défauts ont été remplis avec du collagène seul, d’autres avec du collagène plus des microsphères vides, et d’autres encore avec l’échafaudage chargé en Serpine-1. Après huit semaines, des micro-scanners haute résolution ont montré que le groupe Serpine-1 présentait des volumes osseux, une densité et une épaisseur nettement supérieurs à l’intérieur du défaut. Fait remarquable, seuls ces animaux ont développé du nouvel os au centre de la brèche, et pas uniquement le long des bords.
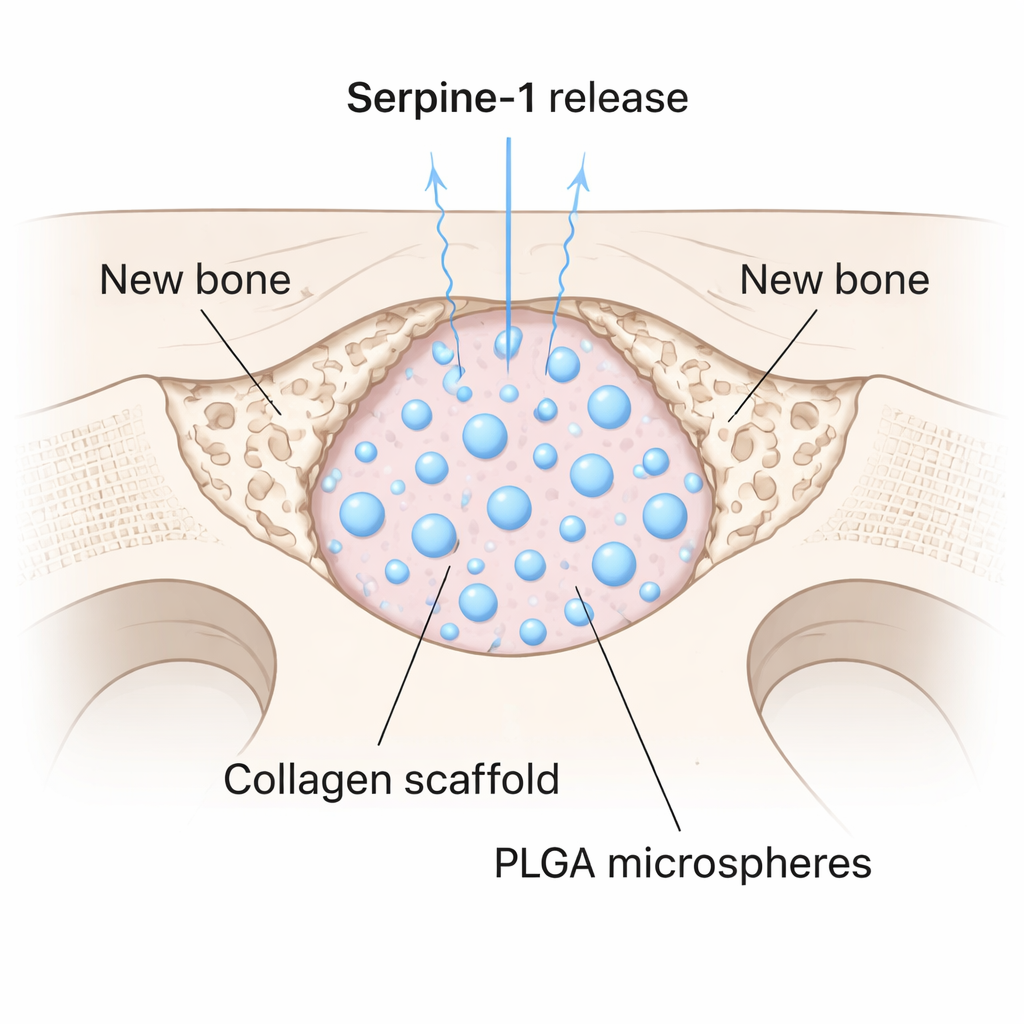
Ce que cela pourrait signifier pour les soins osseux futurs
L’étude présente la Serpine-1 comme un signal puissant et jusqu’alors sous-estimé pour la formation osseuse. En associant cette protéine à un échafaudage à libération lente, les chercheurs ont obtenu une régénération osseuse significative dans un défaut qui resterait normalement vide. Bien que la Serpine-1 n’ait pas attiré les cellules dans le défaut aussi efficacement que certains autres facteurs, sa capacité à aider les cellules existantes à se multiplier et à mûrir suggère qu’elle pourrait être combinée avec des protéines favorisant la migration pour des résultats encore meilleurs. Pour les patients, de tels matériaux sans cellules et à base de protéines pourraient un jour réduire le besoin de prélever de l’os sur leur propre corps ou de recourir à des thérapies cellulaires complexes, offrant une manière plus simple d’inciter des blessures osseuses récalcitrantes à enfin cicatriser.
Citation: Asbi, T., Tamari, T., Doppelt-Flikshtain, O. et al. Proteomic analysis of endothelial progenitor cells secretome identifies Serpine 1 as a potent regulator of osteogenesis. Sci Rep 16, 5165 (2026). https://doi.org/10.1038/s41598-026-36048-6
Mots-clés: régénération osseuse, Serpine-1, ingénierie tissulaire, cellules progénitrices endothéliales, échafaudage en collagène