Clear Sky Science · fr
Classification de la sévérité des démences liées à Alzheimer à partir d’imagerie par résonance magnétique en utilisant l’optimisation sans dérivée de réseaux de neurones convolutifs
Aider les médecins à détecter la démence plus tôt
Avec le vieillissement des populations, de nombreuses familles s’inquiètent des pertes de mémoire et de la démence. Les scanners cérébraux peuvent révéler des changements précoces associés à la maladie d’Alzheimer, mais examiner des milliers d’images à l’œil nu est lent et difficile, même pour des experts. Cette étude présente un outil informatique intelligent qui analyse des IRM cérébrales et classe les personnes en quatre niveaux de sévérité de la démence, de l’absence de démence à l’atteinte modérée. Le système est conçu pour être à la fois extrêmement précis et suffisamment léger pour fonctionner sur des ordinateurs hospitaliers ordinaires, rendant l’analyse avancée d’images plus accessible.
Un nouvel assistant intelligent pour les examens cérébraux
Les chercheurs se concentrent sur un type d’intelligence artificielle appelé réseau de neurones convolutifs, ou CNN, qui excelle à repérer des motifs dans les images. Plutôt que de se limiter à décider si quelqu’un a la maladie d’Alzheimer, leur outil distingue quatre stades : absence de démence, très léger, léger et modéré. Pour cela, l’équipe a entraîné son modèle sur de larges collections publiques d’IRM déjà étiquetées par des experts. L’objectif était double : atteindre une précision quasi parfaite et garder le modèle compact et rapide, afin qu’il soit pratique pour un usage clinique quotidien plutôt que réservé aux laboratoires de recherche bien financés.
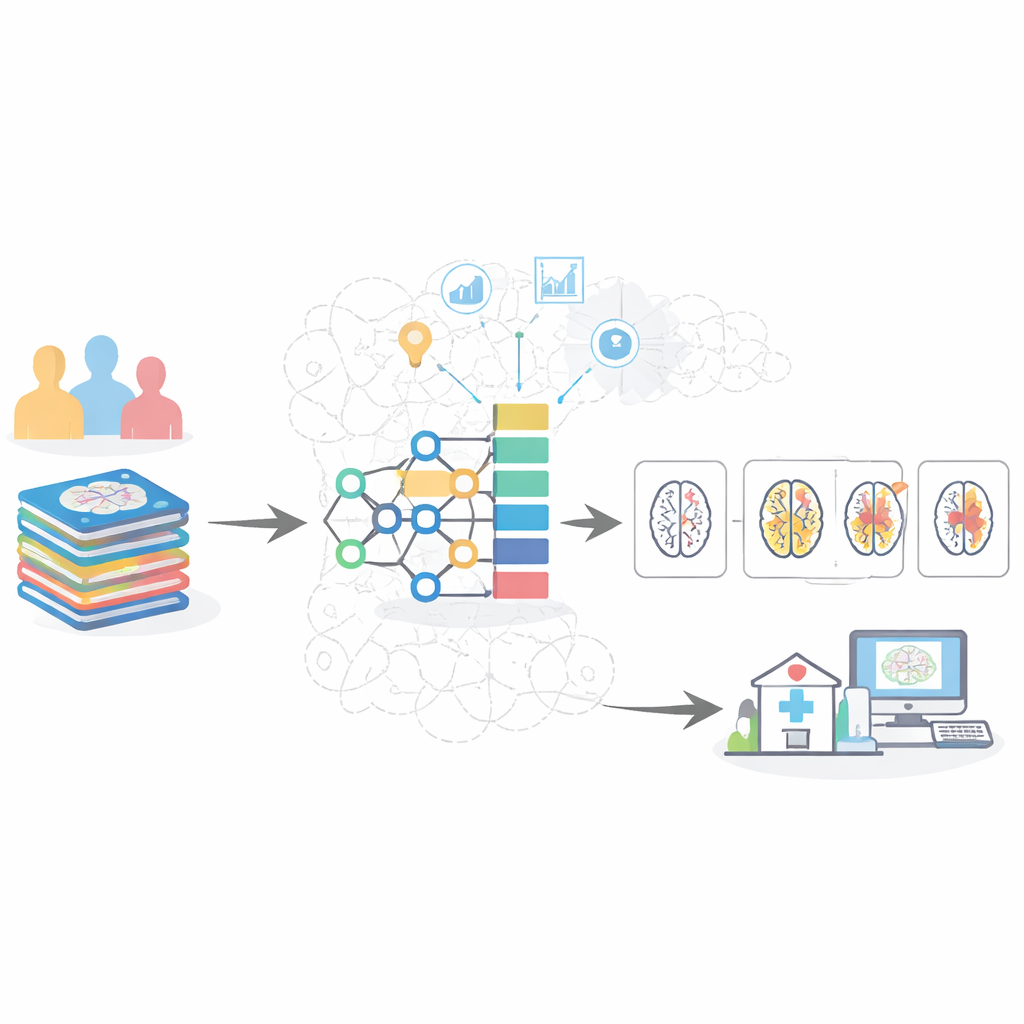
Équilibrer les données et nettoyer les images
Un défi majeur dans les données médicales est que tous les stades de la maladie ne sont pas représentés de manière équilibrée. Dans ces collections d’images cérébrales, les cas sains et très légers sont fréquents, tandis que les IRM de démence modérée sont beaucoup plus rares. Les systèmes d’IA standards ont alors tendance à « jouer la sécurité » en surprédictant les classes courantes et en manquant les cas précoces ou modérés. Pour contrer cela, les auteurs ont utilisé une stratégie en deux étapes : ils ont d’abord éliminé les images frontières confuses, puis créé des exemples synthétiques réalistes des stades sous-représentés. Parallèlement, ils ont préparé soigneusement chaque coupe d’IRM en filtrant, en isolant le cerveau des tissus environnants et en normalisant la luminosité et le contraste afin que le modèle puisse se concentrer sur des caractéristiques médicalement pertinentes comme l’atrophie des structures profondes de la mémoire et l’élargissement des espaces remplis de liquide.
Concevoir un réseau plus petit et plus intelligent
Plutôt que de s’appuyer sur des méthodes d’entraînement traditionnelles qui ajustent les paramètres en suivant des gradients mathématiques, l’équipe a utilisé une famille de techniques dites d’optimisation sans dérivée. Ils ont commencé par un CNN conventionnel plus grand, puis ont employé une recherche évolutionnaire et une recherche d’architecture neuronale pour faire évoluer une conception plus simple avec seulement trois couches convolutionnelles et bien moins de filtres. L’optimisation bayésienne a ensuite affiné les hyperparamètres d’entraînement, tandis que le recuit simulé et l’élagage ont supprimé les connexions inutiles après l’apprentissage. Le résultat final, appelé DAPA-CNN, compte environ 85 % de paramètres ajustables en moins que le modèle de départ, utilise environ un quart de la mémoire et s’entraîne en moins des deux tiers du temps, tout en capturant les motifs cruciaux des scans.
Performance quasi parfaite et explications visuelles claires
Malgré sa taille réduite, DAPA-CNN s’est avéré remarquablement précis. Sur un vaste jeu de données sur la maladie d’Alzheimer, il a correctement attribué le stade de démence dans presque tous les cas, avec une précision et d’autres métriques de performance tournant autour de 99 %. Le modèle s’est aussi bien généralisé à un jeu de données multicentrique distinct acquis sur des scanners différents, ce qui suggère qu’il est robuste aux variations réelles de l’imagerie. Pour rendre le système plus transparent pour les cliniciens, les auteurs ont généré des cartes d’activation de classe — des superpositions de type « carte thermique » qui montrent quelles régions du cerveau ont influencé une décision donnée. Aux stades précoces, ces cartes mettent en évidence des zones impliquées dans la mémoire et connues pour se détériorer en premier dans la maladie d’Alzheimer ; aux stades avancés, elles s’étendent à des régions corticales plus larges, en accord avec la compréhension clinique de la progression de la maladie.
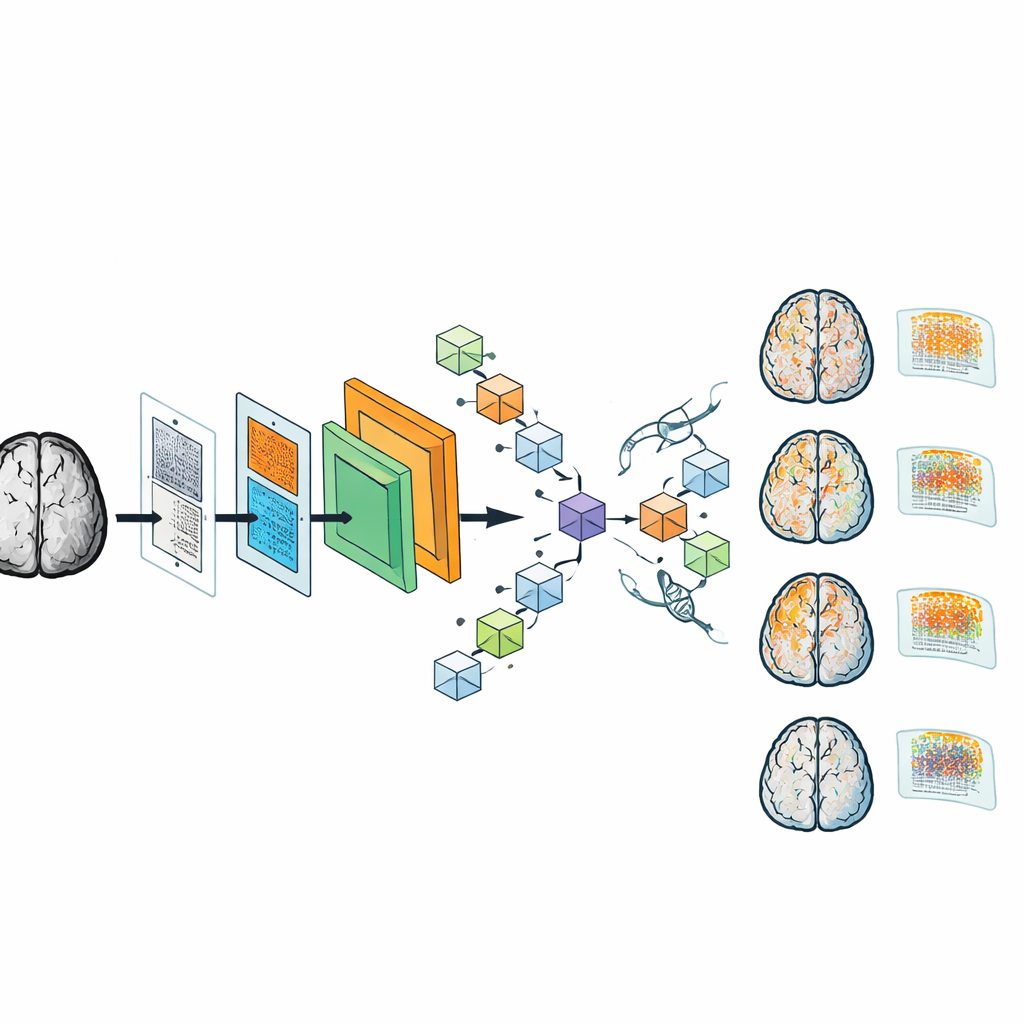
Ce que cela signifie pour les patients et les cliniques
Pour les non-spécialistes, le message principal est que l’étude propose un outil rapide, compact et interprétable pour évaluer la sévérité de la démence à partir d’IRM de routine. En équilibrant les données d’entraînement et en façonnant soigneusement le réseau avec une optimisation sans dérivée, les auteurs ont créé un modèle capable de fonctionner sur du matériel modeste tout en délivrant une précision quasi parfaite et en mettant en lumière les régions cérébrales à l’origine de ses décisions. Si cela est confirmé dans de futurs essais cliniques prospectifs, une telle technologie pourrait permettre des diagnostics plus précoces, une stadification plus homogène entre les hôpitaux et un meilleur suivi des changements cérébraux liés à la maladie d’Alzheimer au fil du temps.
Citation: Ganesan, S.K., Velusamy, P., Parthsarathy, P. et al. Alzheimer’s related dementia severity classification from magnetic resonance imaging using derivative-free optimization of convolutional neural network. Sci Rep 16, 10077 (2026). https://doi.org/10.1038/s41598-026-36037-9
Mots-clés: maladie d’Alzheimer, IRM cérébrale, stades de la démence, apprentissage profond, IA en imagerie médicale