Clear Sky Science · fr
Effets de l’encombrement moléculaire sur la stabilité des protéines dans un protéome bactérien
Pourquoi la vie « crowded » des protéines compte
À l’intérieur de chaque cellule vivante, les protéines accomplissent leurs fonctions dans un espace si rempli d’autres molécules qu’une grande partie du volume peut être occupée. Pourtant, la plupart des expériences en laboratoire étudient les protéines dans des solutions diluées, presque vides. Cet article pose une question simple mais importante : en quoi cette réalité encombrée modifie‑t‑elle la stabilité et le comportement des protéines, et qu’est‑ce que cela implique pour le fonctionnement de la vie à l’échelle moléculaire ?
Un coup d’œil dans un monde cellulaire dense
Pour explorer cela, les chercheurs ont travaillé avec une bactérie appelée Cupriavidus necator, un microbe intéressant pour des technologies vertes comme la capture du carbone et la production de bioplastiques. Ils ont ouvert les cellules en douceur, conservant des centaines de protéines proches de leurs formes naturelles. Ils ont ensuite ajouté des concentrations élevées de grands polymères hydrophiles — des « agents d’encombrement » courants nommés PEG, dextrane et Ficoll — souvent utilisés pour imiter l’intérieur dense des cellules.
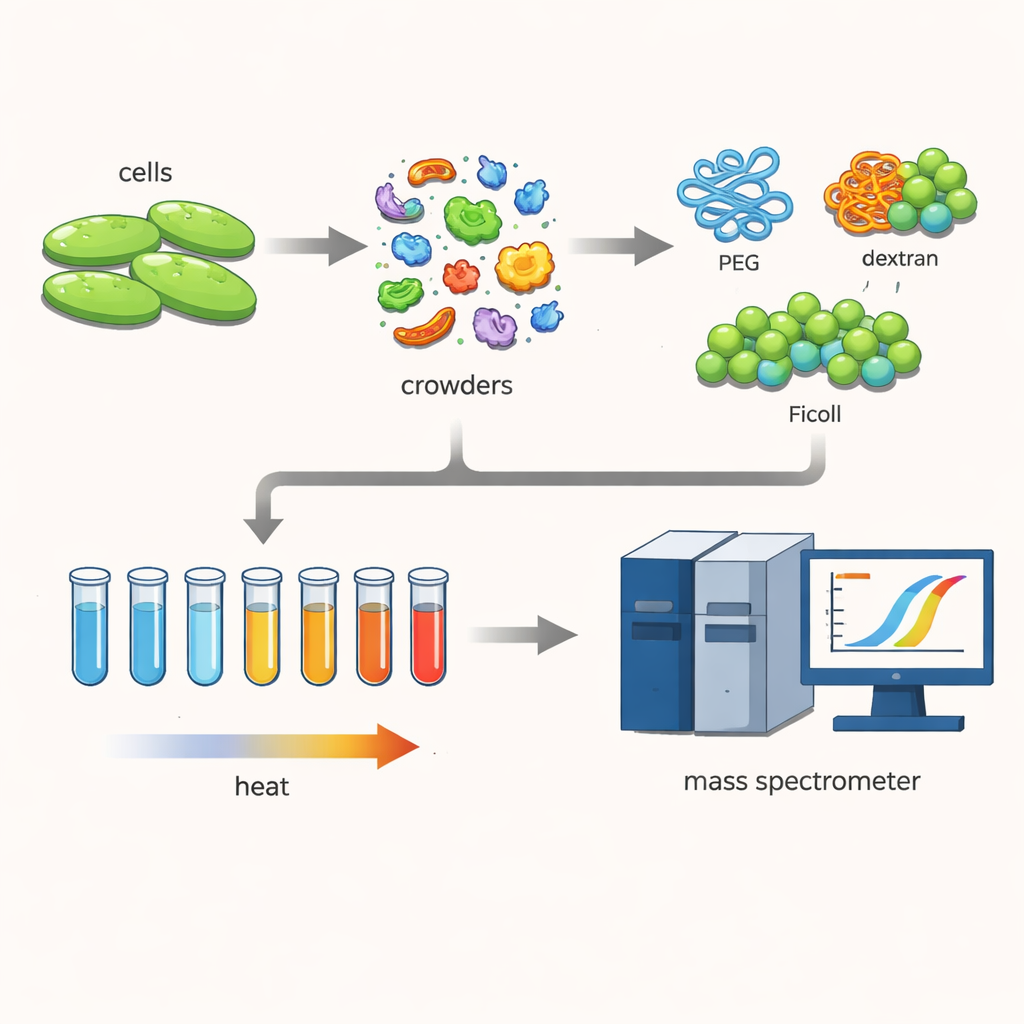
Observer la fonte des protéines
L’équipe a utilisé une technique connue sous le nom de profilage thermique du protéome. Ils ont chauffé de nombreux petits échantillons du mélange protéique par paliers de 30 à 70 degrés Celsius. À mesure que la température montait, les protéines les moins stables se dépliaient et s’agrégeaient, se retirant de la solution. En marquant les protéines encore solubles et en les mesurant avec un spectromètre de masse sensible, les scientifiques ont pu reconstruire des courbes de fusion pour chaque protéine et déterminer sa température de fusion — le point où la moitié d’entre elles a quitté l’état soluble et fonctionnel. Comparer ces températures avec et sans agents d’encombrement a révélé comment l’environnement encombré déplace la stabilité des protéines.
Un tableau contrasté : certaines protéines se renforcent, d’autres s’affaiblissent
En moyenne, l’ajout de l’un quelconque des six polymères d’encombrement a abaissé les températures de fusion à l’échelle du protéome bactérien, impliquant un léger effet global déstabilisant. Mais cette tendance globale masquait une histoire beaucoup plus nuancée. Pour des dizaines de protéines individuelles, les agents d’encombrement ont soit clairement augmenté, soit diminué la stabilité, parfois de plusieurs degrés. La plupart des protéines n’étaient affectées que par un des six réactifs, mais une poignée répondait à plusieurs, et presque toutes ces dernières étaient soit systématiquement stabilisées soit systématiquement déstabilisées, suggérant des caractéristiques communes dans leurs interactions avec les crowders.
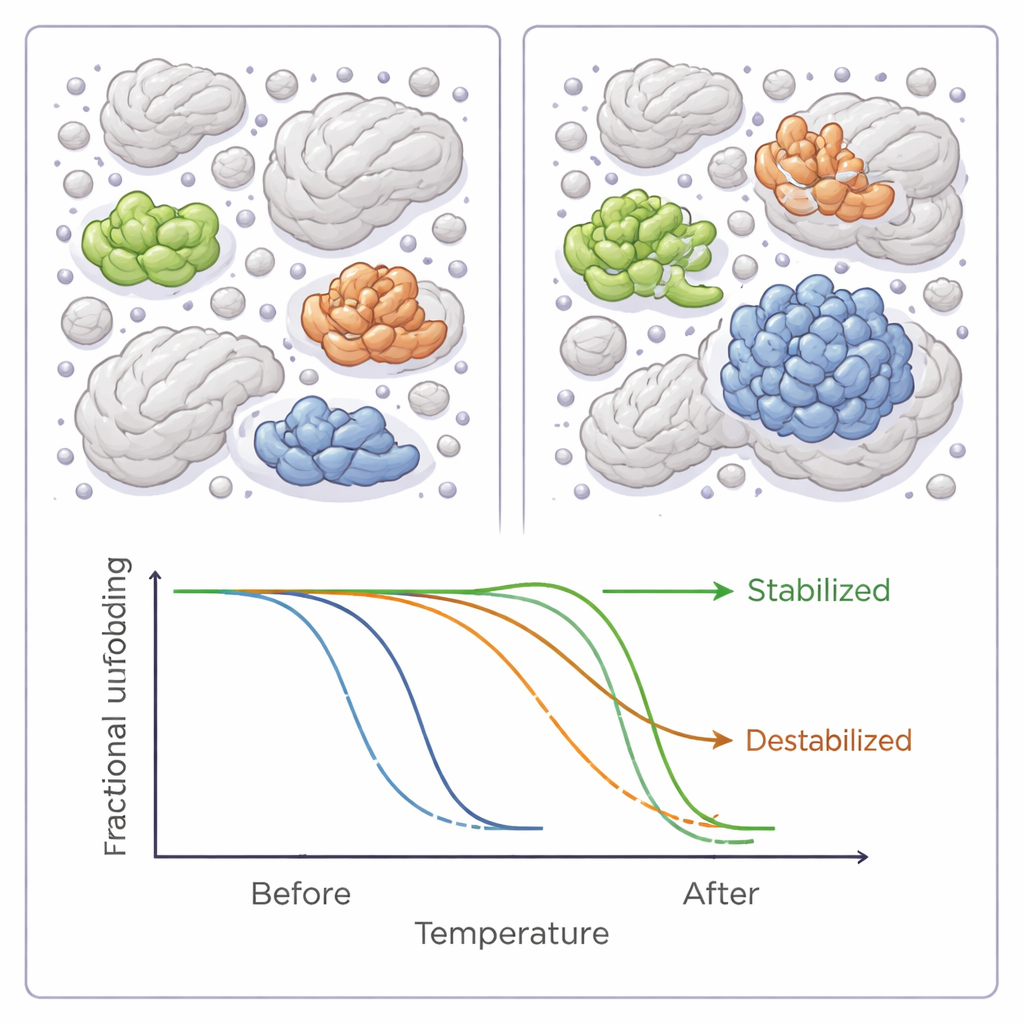
Ce qui fait gagner ou perdre une protéine dans une foule
Quand les auteurs ont examiné de plus près les propriétés de ces protéines sensibles, des motifs sont apparus. Les protéines devenant plus stables en conditions encombrées avaient tendance à être plus hydrophobes — c’est‑à‑dire qu’elles possèdent davantage de surfaces qui repoussent l’eau — et étaient plus souvent des enzymes classiques avec des sites actifs bien définis. Elles étaient aussi plus susceptibles d’être impliquées dans des interactions protéine‑protéine ou de porter des modifications chimiques modulant leur fonction. Les protéines déstabilisées, en revanche, étaient en moyenne plus petites et moins « ornées » de telles modifications. Ces résultats font écho aux modèles informatiques et à d’autres expériences suggérant que l’encombrement peut favoriser certaines protéines tout en rendant d’autres plus vulnérables, selon la taille, la forme et la manière dont elles interagissent normalement avec leurs partenaires.
Au‑delà du simple écrasement : comment les crowders agissent réellement
Les explications traditionnelles de l’encombrement moléculaire se concentrent sur le « volume exclu », l’idée que les grosses molécules laissent simplement moins d’espace, poussant les protéines à rester repliées. Si cela expliquait tout, on s’attendrait à ce que les agents d’encombrement stabilisent principalement les protéines et qu’il existe des liens forts avec l’encombrement ou la viscosité des crowders. À la place, les auteurs n’ont observé que des corrélations faibles avec la taille et l’épaisseur des polymères. Leurs données s’accordent mieux avec une image d’« exclusion préférentielle » : les crowders et les protéines s’évitent chimiquement, ce qui favorise indirectement certains états repliés mais peut aussi perturber des interactions délicates qui maintiennent d’autres protéines stables. En bref, ce n’est pas seulement un écrasement physique, mais un jeu subtil d’attirance et de répulsion chimiques qui façonne le comportement des protéines.
Ce que cela signifie pour la compréhension de la chimie du vivant
Pour les non‑spécialistes, le message clé est que les protéines dans les cellules ne peuvent pas être pleinement comprises isolément, nageant dans un tampon clair. La jungle moléculaire dense qui les entoure peut rendre certaines protéines plus robustes et d’autres plus fragiles, modifiant le comportement de réseaux entiers de réactions. Cette étude, en mesurant les changements de stabilité de centaines de protéines à la fois, montre que les effets d’encombrement sont complexes et spécifiques à chaque protéine, probablement pilotés par des interactions directes autant que par un simple empilement. Lorsque les chercheurs conçoivent des médicaments, des enzymes industrielles ou des microbes ingénierés, reconnaître cette réalité encombrée sera crucial pour prédire comment les protéines se comportent réellement dans les systèmes vivants.
Citation: McKeever, K., Dillon, E.T., Wynne, K. et al. Molecular crowding effects on protein stability in a bacterial proteome. Sci Rep 16, 5908 (2026). https://doi.org/10.1038/s41598-026-35990-9
Mots-clés: encombrement moléculaire, stabilité des protéines, profilage thermique du protéome, protéome bactérien, environnement cellulaire