Clear Sky Science · fr
La déficience en Negr1 modifie la signalisation glutamatergique et la voie du kynurénine dans un modèle murin de troubles psychiatriques
Pourquoi cette étude cérébrale est importante
De nombreuses maladies mentales courantes, de la dépression à la schizophrénie, sont liées à des modifications subtiles de la communication entre cellules cérébrales. Cette étude examine un gène de risque, appelé NEGR1, chez la souris pour voir comment sa perte modifie la chimie du cerveau et le comportement. En suivant les déplacements de ces souris après l’administration d’un médicament qui perturbe brièvement un récepteur clé du cerveau, et en mesurant les produits chimiques cérébraux associés, les chercheurs dévoilent comment la génétique, le sexe et le métabolisme cérébral peuvent se combiner pour façonner la vulnérabilité aux troubles psychiatriques.
Un gène qui maintient l’équilibre des signaux cérébraux
Le gène NEGR1 code pour une protéine de surface cellulaire qui aide les neurones à former et stabiliser leurs connexions. Des travaux antérieurs ont montré que la suppression de ce gène chez la souris modifie la structure cérébrale, réduit certaines connexions inhibitrices (GABA) et altère les réponses à des drogues liées à la dopamine comme l’amphétamine. Parce que ces changements suggèrent un basculement vers une excitation renforcée, l’équipe s’est intéressée à un autre système excitateur majeur : le glutamate et ses récepteurs NMDA, centraux pour l’apprentissage, la mémoire et la flexibilité comportementale. Ils ont aussi examiné la « voie du kynurénine », une route métabolique qui dégrade le tryptophane en composés pouvant soit renforcer soit bloquer les récepteurs NMDA.
Tester le comportement avec un médicament psychotrope
Pour sonder la fonction des récepteurs NMDA, les chercheurs ont utilisé le MK-801, un médicament bien connu qui bloque ces récepteurs de façon transitoire et peut reproduire certains aspects du déséquilibre glutamatergique observé dans les troubles psychiatriques. Des souris mâles et femelles portaient soit le gène Negr1 normal, soit en étaient totalement dépourvues. Les animaux ont reçu des injections quotidiennes de MK-801 et ont été évalués dans une arène en champ ouvert, où leurs déplacements totaux, leur temps passé dans les angles et leurs rotations de type « spinning » ont été suivis automatiquement. Chez les mâles naïfs au médicament, une dose unique de MK-801 a produit une poussée d’activité plus marquée chez les souris déficientes en Negr1 que chez les souris normales, suggérant que leurs cerveaux étaient particulièrement sensibles à cette perturbation de la signalisation glutamatergique.
Un schéma surprenant de tolérance rapide
Lorsque le MK-801 a été administré de façon répétée, le tableau a changé. Chez les mâles, l’activité a culminé certains jours mais chuté tous les deux jours, formant un motif en zigzag suggérant une tolérance rapide et partielle aux effets du médicament. Sur neuf jours, les mâles normaux ont montré une réponse en hausse cohérente avec une sensibilisation, tandis que les mâles déficients en Negr1 ont présenté une augmentation atténuée de l’activité et des variations plus douces d’un jour sur l’autre, pointant vers une sensibilité altérée des récepteurs NMDA. Les femelles des deux génotypes se sont adaptées encore plus vite : vers le cinquième jour, le MK-801 ne produisait plus d’effets comportementaux marqués, et le traitement a été arrêté. Dans l’ensemble des mesures, le sexe a eu une influence majeure, et des effets génétiques évidents sont apparus principalement chez les mâles.
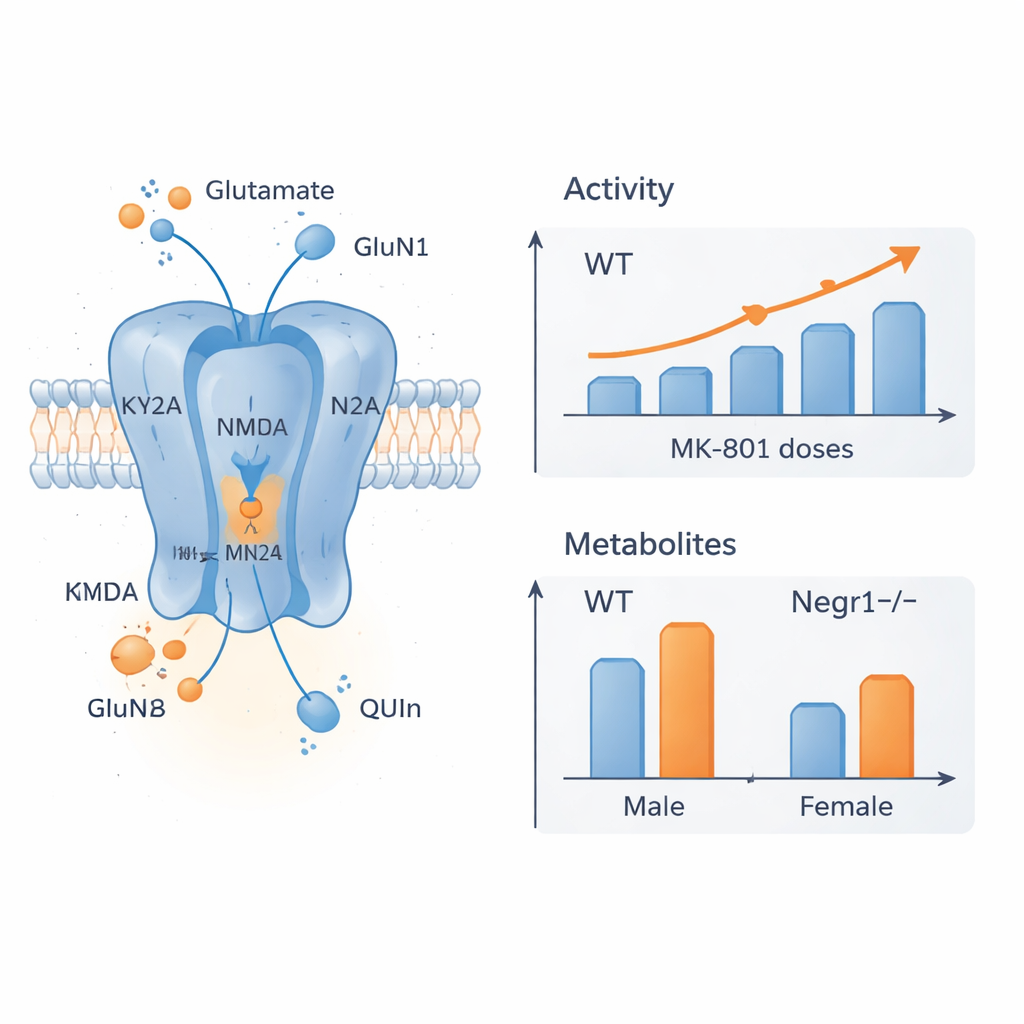
Modifications des récepteurs et des composés cérébraux
Pour comprendre l’origine de ces différences comportementales, l’équipe a mesuré l’activité génique des principales sous-unités des récepteurs NMDA et d’une enzyme qui produit la D-sérine, un co-signal pour ces récepteurs. Ils se sont concentrés sur des régions cérébrales cruciales pour l’humeur et la cognition : le cortex frontal et l’hippocampe. Dans le cortex frontal, les femelles déficientes en Negr1 traitées au MK-801 présentaient une expression réduite des sous-unités majeures du récepteur, suggérant que leur cerveau ajuste la composition des récepteurs en réponse à la fois à la mutation et au médicament. Dans l’hippocampe des mâles, les souris déficientes en Negr1 montraient une expression de base plus élevée de certaines sous-unités NMDA, en accord avec des preuves antérieures d’un plus grand nombre de récepteurs disponibles ; le traitement par MK-801 ramenait alors ces niveaux vers la normale. Parallèlement, des analyses chimiques détaillées du sang et de plusieurs régions cérébrales ont révélé que plusieurs métabolites de la voie du kynurénine et le glutamate lui-même étaient altérés d’une manière dépendante du sexe et de la région, le cortex frontal étant le plus affecté et certaines modifications devenant plus marquées avec l’âge.
Ce que cela signifie pour la compréhension des maladies mentales
Ensemble, ces résultats présentent NEGR1 comme un organisateur moléculaire qui aide à maintenir l’équilibre entre signaux excitateurs et inhibiteurs dans le cerveau, en influençant en partie la fonction des récepteurs NMDA et le métabolisme du tryptophane. Lorsque Negr1 est absent, les souris réagissent différemment au blocage des récepteurs NMDA, montrent des décalages des composés cérébraux dépendants du sexe et développent progressivement une tolérance selon des schémas inhabituels. Pour un lecteur non spécialiste, le message clé est qu’un seul gène de risque n’agit pas isolément : ses effets dépendent du sexe, de la région cérébrale et de l’état métabolique. Ce travail renforce l’idée que cibler des voies liées à NEGR1 — plutôt que seulement des récepteurs isolés — pourrait à terme aider à adapter les traitements pour des troubles mentaux marqués par des déséquilibres du glutamate.
Citation: Kuuskmäe, C., Mikheim, K., Mohammadrahimi, N. et al. Negr1 deficiency alters glutamate signalling and kynurenine pathway in a mouse model of psychiatric disorders. Sci Rep 16, 5317 (2026). https://doi.org/10.1038/s41598-026-35968-7
Mots-clés: gène NEGR1, récepteur NMDA, signalisation glutamatergique, voie du kynurénine, troubles psychiatriques