Clear Sky Science · fr
Les particules fines aggravent l’asthme infantile via la modulation par DNMT3A de la méthylation de l’ADN de GPX4
Pourquoi l’air pollué compte pour les poumons des enfants
Le smog urbain n’est pas qu’une nuisance visuelle ; il peut envoyer des enfants asthmatiques aux urgences. Cette étude pose une question pressante pour les familles vivant dans des zones polluées : comment de minuscules particules d’air appelées PM2,5 aggravent-elles réellement les crises d’asthme ? En retraçant ce qui se passe de l’air extérieur jusqu’aux cellules qui tapissent les voies respiratoires d’un enfant, les chercheurs mettent au jour une chaîne d’événements cachée à l’intérieur des cellules pulmonaires qui relie la pollution à l’inflammation et aux lésions des voies aériennes.
Petites particules, gros problèmes
PM2,5 désigne des particules en suspension dans l’air si fines qu’elles peuvent pénétrer profondément dans les poumons. Les médecins savent depuis longtemps que les jours où les concentrations de PM2,5 sont élevées coïncident souvent avec des poussées d’asthme : plus de toux, de sifflements et de difficultés respiratoires. Pourtant, les étapes biologiques reliant l’air pollué à ces crises restaient floues. Ce travail se concentre sur l’asthme chez l’enfant, utilisant à la fois des modèles animaux et des échantillons de jeunes patients pour montrer que les PM2,5 font plus qu’irriter la surface des poumons ; ils semblent déclencher une forme particulière de dommage cellulaire qui amplifie l’inflammation.
Un type particulier de dommage cellulaire dans les voies aériennes
L’équipe s’est focalisée sur un type de mort cellulaire récemment reconnu appelé ferroptose, qui est entraîné par le fer et l’oxydation incontrôlée des lipides des membranes cellulaires. Ils ont exposé des souris et des cellules bronchiques humaines à un allergène de blatte — un déclencheur courant d’asthme — et aux PM2,5. Chez la souris, l’exposition aux PM2,5 a entraîné une plus grande accumulation de cellules inflammatoires autour des voies aériennes, un mucus plus épais et des taux accrus de molécules inflammatoires IL-6 et IL-8 dans le tissu pulmonaire. Lorsque les chercheurs ont administré un médicament qui bloque la ferroptose, ces changements nocifs ont été largement réduits, suggérant que ce type spécifique de dommage cellulaire est une étape clé de l’aggravation de l’asthme par la pollution.
Le bouclier naturel de l’organisme et la façon dont la pollution l’affaiblit
Les cellules disposent de mécanismes de défense contre cette oxydation destructrice, et l’un des défenseurs les plus importants est une protéine appelée GPX4. Dans des cellules des voies aériennes en bonne santé, GPX4 aide à neutraliser les sous-produits d’oxygène nocifs avant qu’ils ne dégradent les membranes cellulaires. Dans cette étude, l’exposition aux PM2,5 a réduit les niveaux de GPX4 à la fois dans les poumons de souris et dans des cellules des voies aériennes humaines. À mesure que GPX4 diminuait, les cellules présentaient davantage d’espèces réactives de l’oxygène, plus de lésions membranaires et une perte de la fonction mitochondriale saine — autant de caractéristiques de la ferroptose. Lorsque les scientifiques ont augmenté artificiellement GPX4 dans les cellules, une grande partie du stress oxydatif, des lésions cellulaires et de la libération d’IL-6/IL-8 a été inversée, soulignant le rôle essentiel de GPX4 comme bouclier.
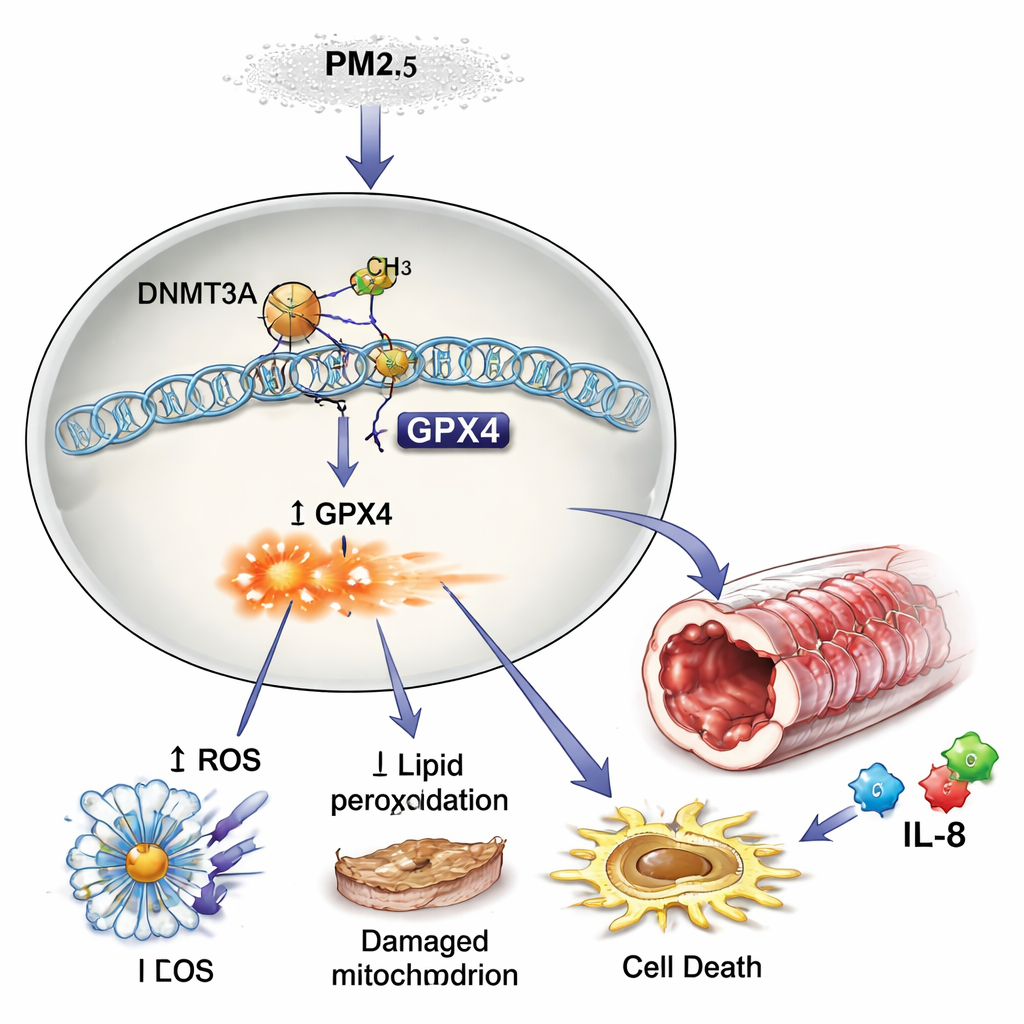
La pollution reprogramme les interrupteurs génétiques par des étiquettes chimiques
Pourquoi les niveaux de GPX4 ont-ils chuté après l’exposition aux PM2,5 ? La réponse résidait dans l’épigénétique — des étiquettes chimiques qui agissent comme des variateurs sur les gènes. Les chercheurs ont constaté que les PM2,5 augmentaient l’activité d’une enzyme appelée DNMT3A, qui ajoute des groupes méthyle à l’ADN. Ces étiquettes s’accumulaient dans la région régulatrice du gène GPX4, réduisant effectivement son expression. Bloquer DNMT3A empêchait cette méthylation supplémentaire et rétablissait l’expression de GPX4, montrant que les PM2,5 « reprogramment » les cellules des voies aériennes en resserrant ce variateur génétique. Dans des cellules sanguines d’enfants asthmatiques, ceux atteints de formes plus sévères présentaient une méthylation plus élevée de GPX4, moins de protéine GPX4 et des taux accrus d’IL-6/IL-8, reflétant les observations en laboratoire.
Ce que cela signifie pour protéger les enfants
Pour un public non spécialiste, le message est que les minuscules particules de pollution n’irritent pas seulement les poumons ; elles modifient silencieusement le fonctionnement des gènes protecteurs clés dans les cellules des voies aériennes. Les PM2,5 stimulent DNMT3A, qui ajoute des étiquettes chimiques étouffant le gène « bouclier » GPX4. Une fois ce bouclier affaibli, les cellules sont plus susceptibles de subir une ferroptose et de libérer des molécules inflammatoires qui resserrent et obstruent les voies respiratoires des enfants, aggravant l’asthme. Ces découvertes renforcent non seulement l’importance des politiques pour un air plus propre et de la protection de l’air intérieur, mais elles pointent aussi vers de futurs traitements susceptibles de protéger ou de restaurer la fonction de GPX4 — idéalement délivrés directement dans les poumons — pour aider les enfants à mieux respirer dans des environnements pollués.
Citation: Wu, X., Dai, L., Li, R. et al. Fine particulate matter exacerbates childhood asthma via DNMT3A-mediated modulation of GPX4 DNA methylation. Sci Rep 16, 5566 (2026). https://doi.org/10.1038/s41598-026-35962-z
Mots-clés: pollution de l’air, asthme infantile, PM2.5, épigénétique, inflammation pulmonaire