Clear Sky Science · fr
APOBEC3B augmente l’efficacité des inhibiteurs de PARP pour éliminer les cellules souches du cancer ovarien
Pourquoi cette recherche importe pour les patientes atteintes de cancer de l’ovaire
De nombreuses femmes atteintes d’un cancer de l’ovaire avancé répondent bien au départ aux médicaments modernes appelés inhibiteurs de PARP, qui ciblent des faiblesses du système de réparation de l’ADN des tumeurs. Pourtant, avec le temps, la maladie réapparaît souvent parce que les cellules cancéreuses apprennent à survivre à ces traitements. Cette étude met en lumière une alliée inattendue à l’intérieur des cellules cancéreuses elles‑mêmes — une enzyme modifiant l’ADN nommée APOBEC3B — et montre que, dans les bonnes conditions, elle peut en fait rendre les cellules souches du cancer de l’ovaire plus faciles à éliminer avec des inhibiteurs de PARP.
Un cancer mortel qui récidive
Le carcinome séreux de haut grade est la forme la plus fréquente et la plus létale de cancer de l’ovaire. Il est généralement diagnostiqué tard, lorsque la maladie s’est déjà étendue dans l’abdomen, et plus de 80 % des patientes atteintes d’une maladie avancée rechutent dans les cinq ans. Un suspect clé dans ces rechutes est une petite population de « cellules souches cancéreuses ». Ces cellules peuvent s’auto‑renouveler, survivre à la chimiothérapie et reconstruire les tumeurs après le traitement. Comprendre ce qui rend ces cellules de type souche résistantes — et comment les cibler — est essentiel pour améliorer la survie à long terme.
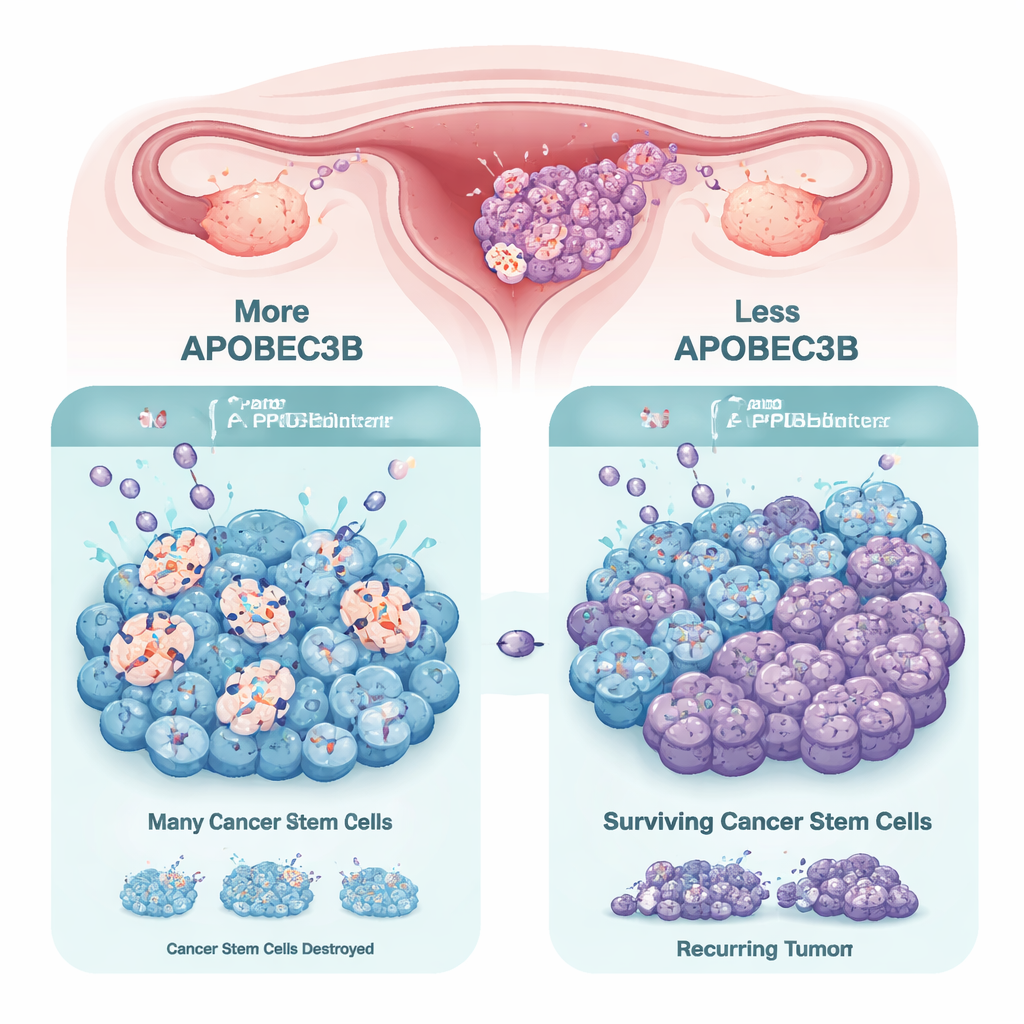
Une enzyme mutagène aux deux visages
La famille d’enzymes APOBEC3 aide normalement à protéger nos cellules contre les virus en modifiant des bases spécifiques de l’ADN, ce qui peut introduire des mutations. Dans de nombreux cancers, un membre de cette famille, APOBEC3B, est hyperactif et contribue aux dommages de l’ADN et au chaos génétique, favorisant l’évolution tumorale et la résistance aux thérapies. Dans les tumeurs ovariennes et des modèles dérivés de patientes, les chercheurs ont confirmé qu’APOBEC3B est généralement l’enzyme APOBEC3 la plus abondante. Cependant, en comparant les cellules tumorales ordinaires aux « tumorsphères » de type cellule souche cultivées en 3D, ils ont découvert que les cellules de type souche réduisent systématiquement l’expression d’APOBEC3B. Cela suggère que les cellules souches cancéreuses peuvent diminuer leur charge de mutations pour préserver leur survie et leur capacité d’auto‑renouvellement.
Réduire APOBEC3B rend les cellules souches plus résistantes
Pour tester si APOBEC3B influence réellement le caractère « stem », l’équipe a utilisé des outils génétiques pour diminuer son expression dans des modèles de cancer ovarien dérivés de patientes et dans des lignées cellulaires établies. Lorsque les niveaux d’APOBEC3B étaient abaissés, les cellules cancéreuses formaient des tumorsphères plus efficacement et exprimaient des marqueurs classiques de stemness tels que SOX2, OCT4 et NANOG à des niveaux plus élevés. La fraction de cellules aux propriétés de cellules souches a augmenté, indiquant que la perte d’APOBEC3B aide les cellules cancéreuses à passer à un état plus résilient et de type souche. Chez la souris, les tumeurs dépourvues d’APOBEC3B ne croissaient pas plus vite spontanément, mais elles se comportaient différemment lorsqu’on les traitait par des inhibiteurs de PARP.
Plus d’APOBEC3B, plus de dommages — et meilleure réponse aux médicaments
Les chercheurs ont ensuite interrogé l’effet d’APOBEC3B sur l’efficacité des inhibiteurs de PARP comme l’Olaparib, qui bloquent la réparation de l’ADN et poussent les cellules cancéreuses vers des dommages d’ADN létaux. Dans plusieurs lignées cellulaires du cancer de l’ovaire, la réduction d’APOBEC3B rendait les cellules plus résistantes aux inhibiteurs de PARP, en particulier dans des tumorsphères 3D enrichies en cellules de type souche. Inversement, augmenter APOBEC3B sensibilisait certaines cellules aux inhibiteurs de PARP, réduisant fortement leur survie. Dans des expériences chez la souris, les tumeurs avec des niveaux normaux d’APOBEC3B ont diminué ou ralenti de façon spectaculaire sous Olaparib, tandis que les tumeurs déficientes en APOBEC3B continuaient de croître malgré le traitement. Les analyses moléculaires expliquent pourquoi : des niveaux élevés d’APOBEC3B augmentaient le stress de réplication de l’ADN et les cassures double brin, activant les voies de signalisation de dommages à l’ADN. Lorsque APOBEC3B était diminué, les dommages à l’ADN induits par les inhibiteurs de PARP, l’activation des points de contrôle et le stress de réplication diminuaient, et les cellules avaient davantage tendance à se bloquer de manière sécurisée dans le cycle cellulaire plutôt qu’à mourir.
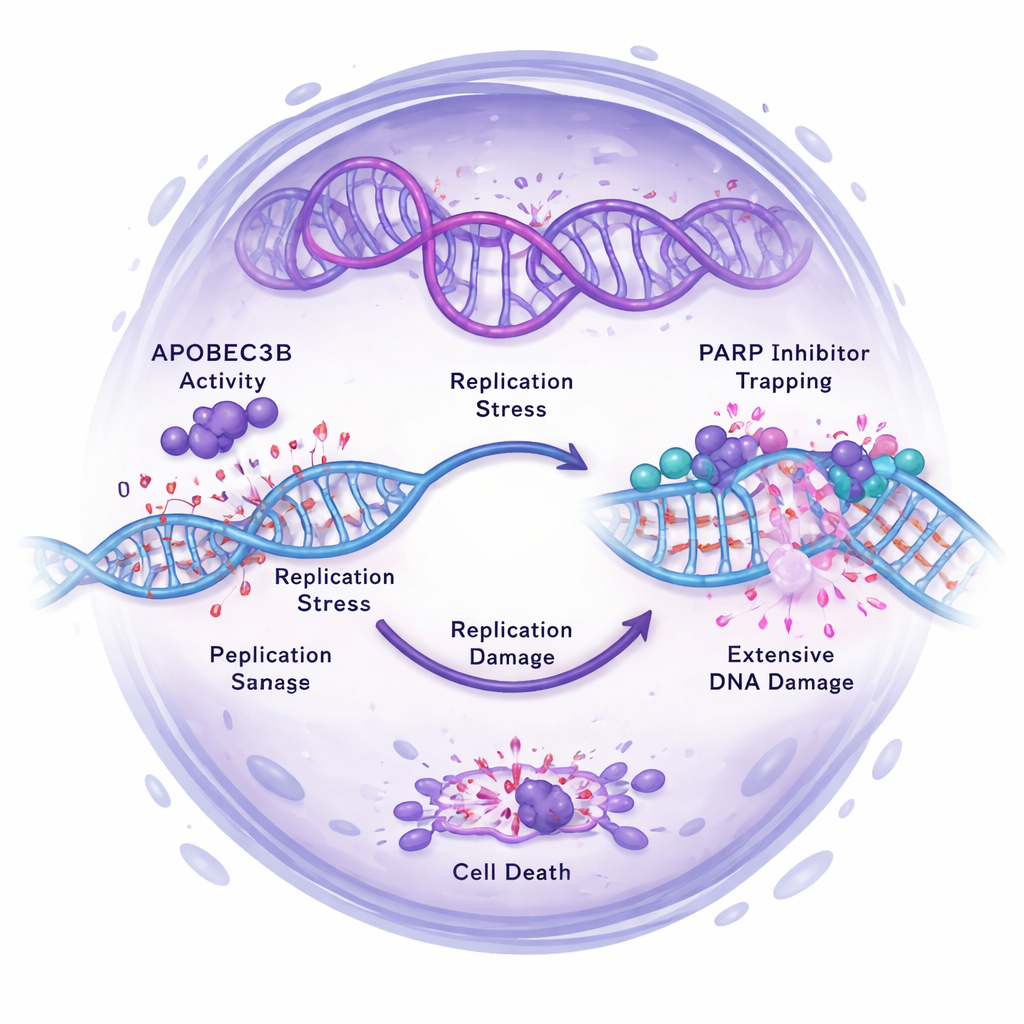
Une nouvelle façon de penser la résistance et la conception des traitements
En approfondissant par séquençage d’ARN, l’équipe a trouvé que la combinaison de la perte d’APOBEC3B et de l’inhibition de PARP réordonnait l’expression de nombreux gènes impliqués dans la réplication et la réparation de l’ADN, soutenant l’idée qu’APOBEC3B amplifie les effets délétères des inhibiteurs de PARP sur le génome des cellules cancéreuses. Ils ont également testé si une autre enzyme de réparation, UNG, était nécessaire pour cet effet et ont constaté que la sensibilité aux inhibiteurs de PARP dans les cellules à haut niveau d’APOBEC3B était largement indépendante d’UNG. Globalement, les données pointent vers le stress de réplication induit par APOBEC3B — et pas seulement son activité mutagène — comme principal facteur qui aide les inhibiteurs de PARP à tuer les cellules souches du cancer ovarien.
Ce que cela signifie pour les patientes et les thérapies futures
Pour un lecteur non spécialiste, le message est que tout le chaos génétique au sein d’une tumeur n’est pas forcément une mauvaise nouvelle. Dans cette étude, des niveaux plus élevés de l’enzyme mutagène APOBEC3B ont en réalité rendu les cellules souches du cancer de l’ovaire plus vulnérables aux inhibiteurs de PARP en surchargeant leur capacité de réparation de l’ADN. Lorsque APOBEC3B était réduit, les cellules souches cancéreuses devenaient plus « stem‑like » et mieux capables de résister au traitement. Ces résultats suggèrent que mesurer les niveaux d’APOBEC3B pourrait aider à prédire quelles patientes bénéficieront le plus des inhibiteurs de PARP, et que le moment choisi ou la combinaison d’éventuels médicaments ciblant APOBEC3B avec des inhibiteurs de PARP devra être maniée avec précaution. Exploiter l’effet « auto‑sabotage » d’APOBEC3B sur les cellules cancéreuses pourrait ouvrir de nouvelles stratégies pour prévenir les rechutes et éliminer plus efficacement les racines des tumeurs ovariennes.
Citation: Rivera, M., Liu, L., Enlund, S. et al. APOBEC3B enhances the efficacy of PARP inhibitors in elimination of ovarian cancer stem cell. Sci Rep 16, 5194 (2026). https://doi.org/10.1038/s41598-026-35939-y
Mots-clés: cancer de l’ovaire, inhibiteurs de PARP, cellules souches cancéreuses, APOBEC3B, résistance aux médicaments