Clear Sky Science · fr
Agrégation supramoléculaire de l’aquaporine‑4 module la migration collective et la mécanique des astrocytes
Comment les cellules cérébrales se déplacent ensemble pour réparer
Lorsque le cerveau est blessé ou enflammé, ses cellules de soutien — les astrocytes — affluent pour protéger, réparer ou isoler les zones endommagées. Cette étude explore un facteur surprenant qui influence la capacité de ces cellules à se déplacer collectivement : de minuscules canaux à eau appelés aquaporine‑4 (AQP4). En examinant comment les molécules d’AQP4 s’agrègent ou se répartissent dans la membrane des astrocytes, les chercheurs montrent comment la « plomberie » hydrique du cerveau aide à coordonner le mouvement collectif des cellules, et comment une inflammation chronique peut perturber ce processus.
Des portails d’eau sur les cellules cérébrales
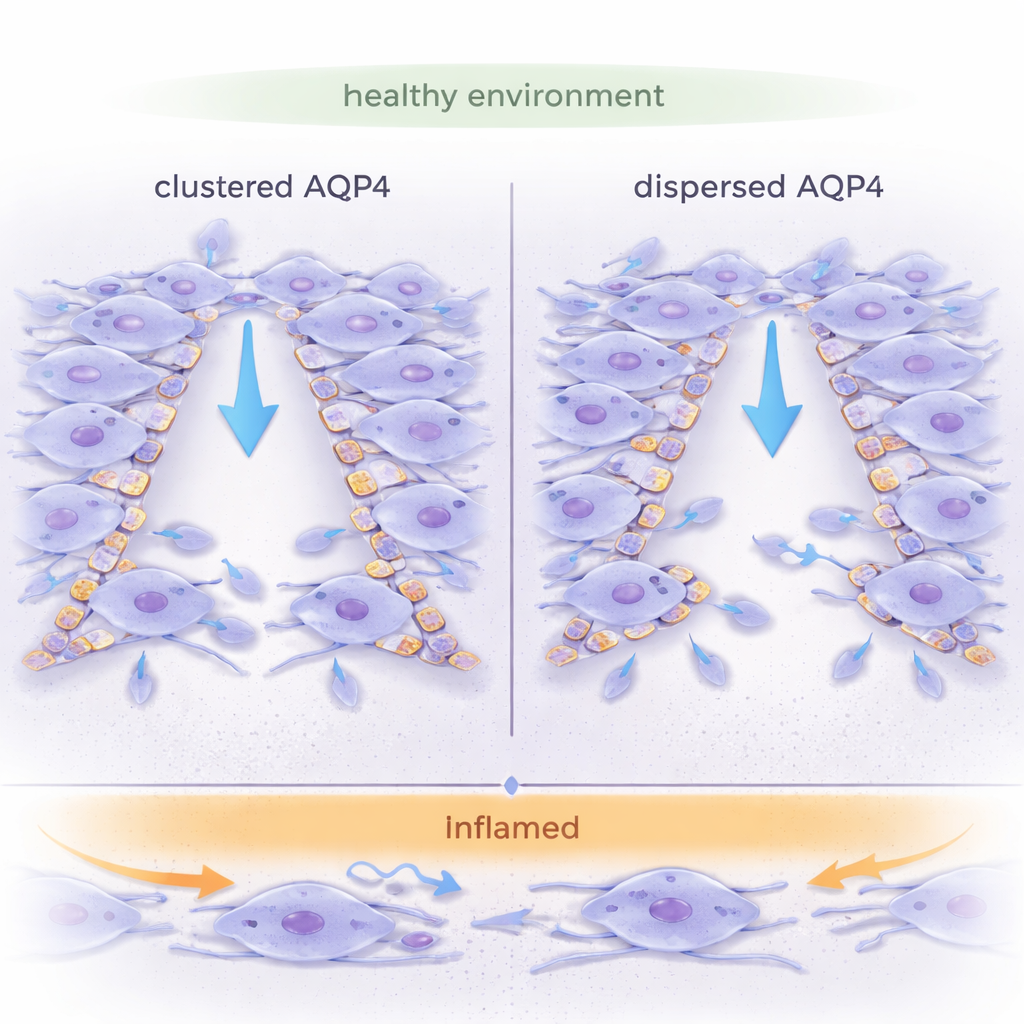
Les astrocytes sont des cellules en étoile qui contribuent à l’homéostasie cérébrale, guident le développement et répondent aux blessures. Ils sont riches en AQP4, une protéine formant des pores qui laissent l’eau entrer et sortir rapidement de la cellule. Contrairement à de nombreux autres canaux aqueux, l’AQP4 peut s’assembler en grands patchs cristallins appelés réseaux orthogonaux de particules (OAPs), ou rester sous forme d’unités plus petites et dispersées (tétramères). On pense que l’organisation de l’AQP4 influence la capacité des cellules à changer de forme et à migrer, mais la plupart des travaux antérieurs se sont concentrés sur des cellules isolées. Cette étude pose une question plus réaliste : comment l’organisation de l’AQP4 affecte‑t‑elle la migration en bloc de nappes d’astrocytes, comme lors de la fermeture d’une plaie dans le tissu cérébral ?
Tester le mouvement cellulaire en santé et en inflammation
Les chercheurs ont cultivé deux types d’astrocytes de souris : des cellules normales capables de former des réseaux d’AQP4, et des cellules génétiquement modifiées (dépourvues d’OAP) qui n’expriment pas la principale isoforme formant les réseaux et présentent donc principalement des tétramères dispersés. Ils ont ensuite créé une « griffure » dans une couche dense de cellules, simulant une plaie, et observé la rapidité et la régularité de la fermeture du vide. Pour reproduire un cerveau chroniquement blessé, certaines cultures ont été exposées pendant une semaine à deux molécules inflammatoires, l’IL‑1β et le TNF‑α, avant les tests. À l’aide d’imagerie en continu et d’une méthode de vision par ordinateur appelée vélocimétrie par images de particules, ils ont quantifié non seulement la distance et la vitesse de déplacement, mais aussi la linéarité, la coordination et les contraintes du mouvement à l’échelle de la nappe cellulaire.
Canaux dispersés, mouvement plus fluide
En l’absence d’inflammation, les astrocytes présentant une AQP4 dispersée (dépourvus d’OAP) migraient collectivement de manière nettement plus efficace : ils fermaient les plaies plus vite et se déplaçaient de façon plus directe et linéaire que les cellules avec de grands réseaux d’AQP4. Leur front d’avancée était lisse et continu, et les cellules voisines se mouvaient de façon cohésive, comme une nappe homogène. En revanche, les astrocytes avec une AQP4 regroupée (type sauvage) montraient un front plus irrégulier, avec de nombreuses protrusions individuelles et des déformations internes, suggérant que les cellules tiraient dans des directions légèrement différentes. Les mesures de déformation au sein de la couche cellulaire ont confirmé que les nappes d’OAP‑nuls subissaient moins de tensions internes et présentaient un mouvement plus uniforme et coordonné.
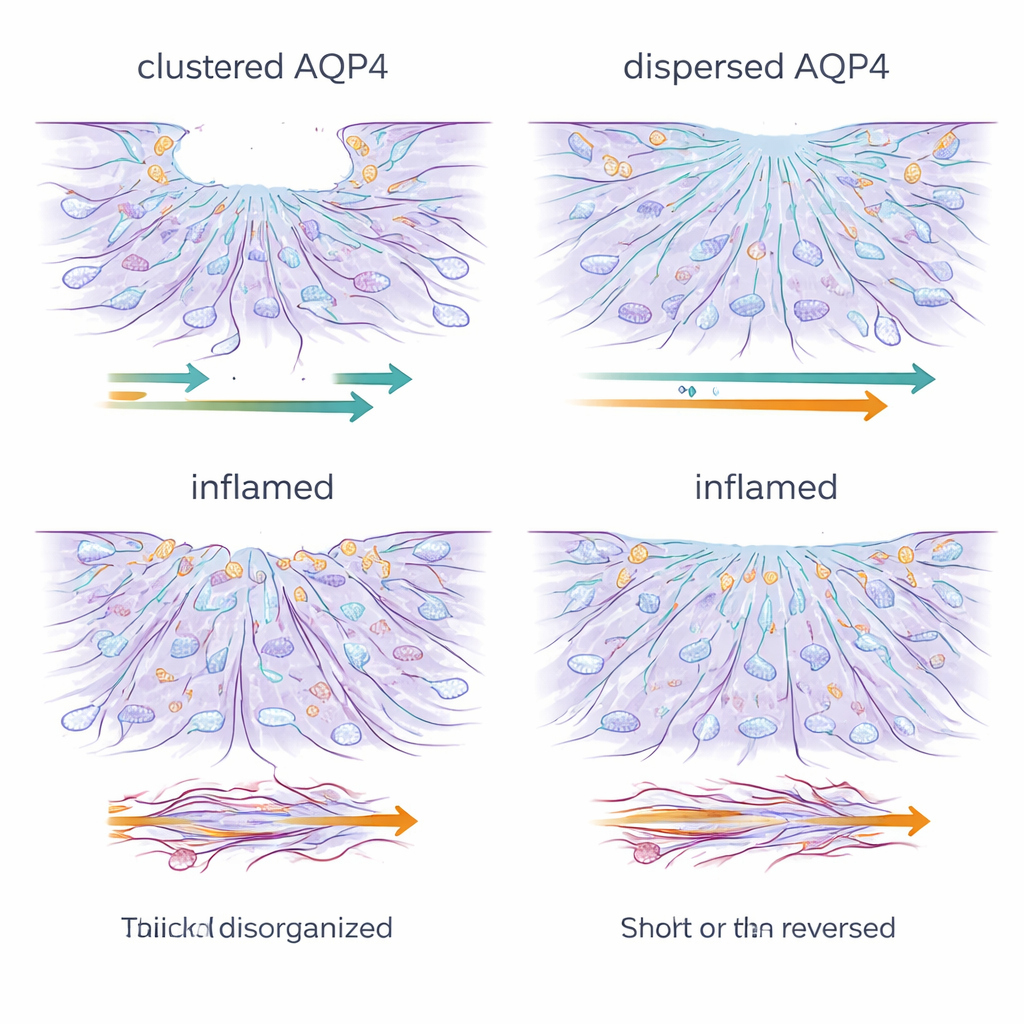
L’inflammation freine et désordonne l’équipe de réparation
Une exposition chronique aux signaux inflammatoires a profondément modifié ce tableau. Indépendamment de l’organisation de l’AQP4, les astrocytes traités sont devenus de mauvais réparateurs : ils bougeaient à peine, et dans certains cas reculèrent même, augmentant l’écart. La microscopie a montré que les structures fines et dynamiques en bord de cellule nécessaires à l’avancée — lamellipodes et filopodes — avaient disparu, remplacées par d’épais faisceaux d’actine rigides, la principale protéine de charpente cellulaire. Parallèlement, les niveaux d’AQP4 et de connexine‑43, une protéine clé formant des jonctions communicantes entre astrocytes, ont fortement chuté. Le réseau de jonctions communicantes qui aide normalement les astrocytes à agir comme une unité coordonnée a été perturbé, et des expériences de transfert de colorant ont confirmé que la communication cellulaire à longue distance était sérieusement affaiblie.
Pourquoi cela importe pour la santé cérébrale
Ces résultats suggèrent que ce n’est pas seulement la quantité d’AQP4 présente dans une cellule, mais aussi son organisation, qui permet aux astrocytes de se déplacer efficacement en groupe. Une AQP4 dispersée semble réduire la résistance interne entre cellules et favoriser un mouvement plus droit et coordonné, tandis que de grands agrégats s’associent à un style de déplacement plus erratique et soumis à des tensions. L’inflammation chronique annule en grande partie ces avantages en remodelant le cytosquelette, en diminuant les canaux d’eau et de communication, et en transformant une équipe de réparation organisée en une nappe rigide et mal connectée. Pour un public non spécialisé, la leçon est que les canaux hydriques du cerveau et les systèmes de communication intercellulaire font bien plus que soutenir passivement les neurones — ils façonnent activement la mobilisation des cellules de soutien après une blessure. Comprendre et, à terme, moduler l’organisation de l’AQP4 et les signaux inflammatoires pourrait ouvrir de nouvelles voies pour améliorer la réparation cérébrale, limiter la cicatrisation ou même influencer la propagation des tumeurs cérébrales.
Citation: Barile, B., Mennona, N.J., Mola, M.G. et al. Supramolecular aggregation of aquaporin-4 shapes astrocyte collective migration and mechanics. Sci Rep 16, 6021 (2026). https://doi.org/10.1038/s41598-026-35900-z
Mots-clés: astrocytes, aquaporine‑4, inflammation cérébrale, migration cellulaire, cicatrice gliale