Clear Sky Science · fr
Complexes lanthanides–carbamazépine : synthèse, caractérisation spectroscopique, aperçus DFT, docking moléculaire et évaluation biologique
Pourquoi ce médicament contre l’épilepsie reçoit une mise à jour high‑tech
La carbamazépine est un médicament de longue date utilisé pour traiter l’épilepsie et les troubles de l’humeur, mais il présente des limites : il se dissout mal dans l’eau, peut persister comme polluant dans les cours d’eau et n’a pas été conçu pour des traitements modernes contre le cancer ou les infections. Dans cette étude, les chercheurs ont « mis à niveau » chimiquement la carbamazépine en l’attachant à des métaux particuliers appelés lanthanides, puis ont testé si ces nouveaux composés pouvaient agir comme des agents puissants et ciblés contre les microbes et les cellules cancéreuses.
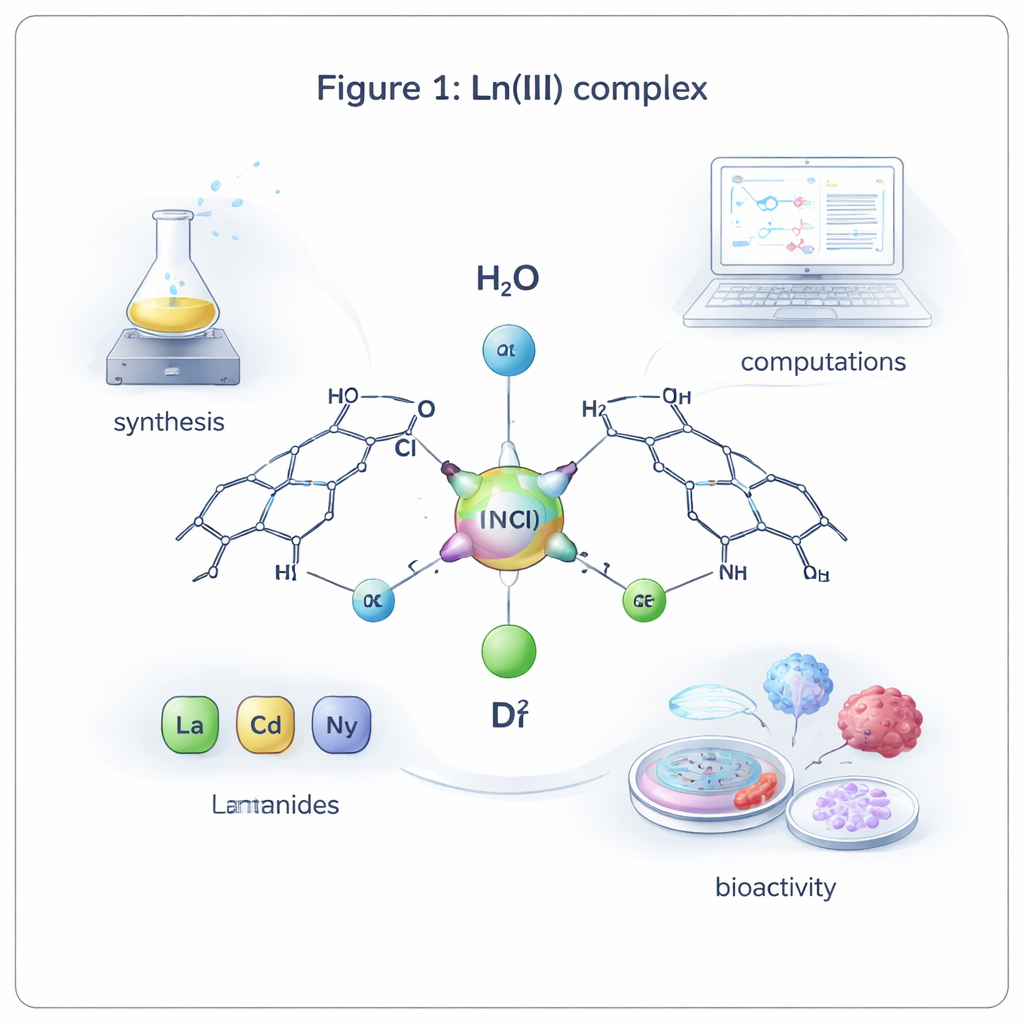
Construire de nouvelles molécules à partir d’un comprimé familier
L’équipe s’est concentrée sur quatre métaux lanthanides — le lanthane, le cérium, le néodyme et le dysprosium — choisis pour leurs propriétés magnétiques et optiques utiles et leurs applications médicales croissantes. Ils ont réagi chaque métal avec la carbamazépine dans une solution alcoolique chauffée, formant quatre complexes métal‑médicament étroitement apparentés dans un rapport 1:2 (un ion métallique lié à deux molécules de carbamazépine). Des mesures de laboratoire précises ont montré que chaque complexe présente une formule globale similaire et se comporte comme un électrolyte, ce qui signifie que des parties de la molécule peuvent se dissocier en espèces chargées en solution, une caractéristique susceptible d’influencer son transport dans l’organisme.
Regarder la forme et la structure
Pour comprendre ce qu’ils avaient obtenu, les scientifiques ont utilisé un ensemble de méthodes spectroscopiques et structurelles, notamment la spectroscopie infrarouge et la résonance magnétique nucléaire, la diffraction des rayons X et l’analyse thermique. Ces tests convergent vers la même image : dans les nouveaux composés, la carbamazépine se lie au métal via deux atomes de son groupe amide — un azote et un oxygène — de sorte que chaque métal se retrouve entouré de six partenaires dans une géométrie octaédrique légèrement déformée. Des calculs informatiques basés sur la théorie de la fonctionnelle de la densité (DFT) ont confirmé cette géométrie et montré que, une fois liée au métal, les propriétés électroniques de la carbamazépine se modifient de façons qui peuvent rendre les complexes plus réactifs et plus stables que le médicament libre, une combinaison prometteuse pour un usage médical.
Des éprouvettes aux microbes et aux cellules cancéreuses
La question suivante était biologique : ces molécules conçues ont‑elles un effet utile sur des cellules vivantes ? Dans des tests en boîte de Pétri, les complexes ont été confrontés à plusieurs bactéries et champignons pathogènes. La carbamazépine seule montrait peu ou pas d’effet, mais les quatre complexes métalliques ont inhibé au moins certains microbes, la version au lanthane produisant les plus larges zones d’inhibition visibles, rivalisant voire dépassant un antifongique standard contre une espèce de moisissure. Les chercheurs ont ensuite exposé des lignées cellulaires cancéreuses humaines du foie (Hep‑G2) et du sein (MCF‑7) aux mêmes composés. Là encore, les complexes métal‑médicament ont surpassé la carbamazépine seule, endommageant ou tuant les cellules cancéreuses à des concentrations bien plus faibles. Parmi eux, le complexe au lanthane s’est distingué, montrant la plus forte activité cytotoxique tout en restant dans une gamme comparable à un agent chimiothérapeutique largement utilisé.
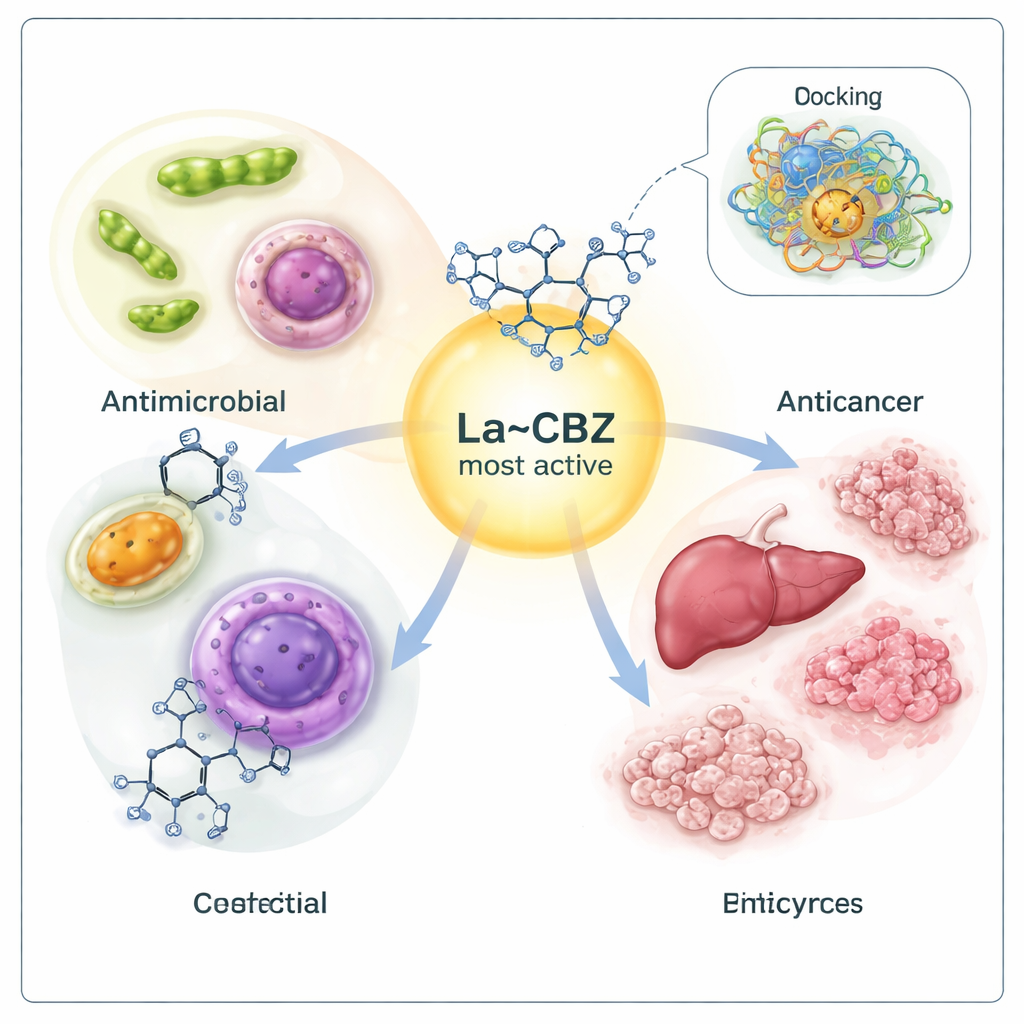
Comment les molécules pourraient se lier aux cibles pathologiques
Pour explorer pourquoi le complexe au lanthane était si puissant, l’équipe a eu recours à des simulations de docking moléculaire — des modèles informatiques montrant comment une petite molécule pourrait s’emboîter dans les recoins d’une protéine. Ils ont examiné des protéines bactériennes et des enzymes clés liées aux cancers du foie et du sein. Les simulations suggèrent que le complexe lanthane–carbamazépine s’insérait le plus fermement dans ces poches de liaison protéiques, créant des interactions fortes susceptibles de perturber leur fonction normale. En termes d’énergie, des énergies de docking plus basses (plus négatives) indiquent une liaison plus étroite, et le complexe au lanthane a systématiquement fourni les valeurs les plus favorables, en accord avec sa supériorité observée dans les tests de laboratoire.
Ce que cela pourrait signifier pour les médicaments de demain
Globalement, ce travail montre qu’un médicament bien connu contre l’épilepsie peut être transformé en une nouvelle classe de composés à base de métal présentant un comportement antimicrobien et anticancéreux prometteur. En reconfigurant la carbamazépine autour de centres lanthanides, les chercheurs ont créé des complexes cristallins stables qui interagissent plus fortement avec des cibles biologiques que le médicament original. Bien que ces résultats en soient encore à un stade préclinique précoce, ils ouvrent la voie à la possibilité d’utiliser de tels hybrides métal‑médicament comme futurs agents chimiothérapeutiques ou anti‑infectieux, et peut‑être même comme outils d’imagerie ou de délivrance exploitant les propriétés optiques et magnétiques uniques des lanthanides.
Citation: Mohamed, N.S., Mohamed, M.M.A., Shehata, M.R. et al. Lanthanide–carbamazepine complexes: synthesis, spectroscopic characterization, DFT Insights, molecular docking, and biological evaluation. Sci Rep 16, 6340 (2026). https://doi.org/10.1038/s41598-026-35893-9
Mots-clés: carbamazépine, complexes de lanthanides, médicaments à base de métaux, agents anticancéreux, activité antimicrobienne