Clear Sky Science · fr
La gonadotrophine chorionique humaine réduit l’encéphalomalacie kystique cérébrale et la dégénérescence des interneurones à parvalbumine dans un modèle pro-inflammatoire d’hypoxie-ischémie néonatale chez la souris
Pourquoi une hormone de la grossesse compte pour le cerveau des nouveau-nés
Lorsqu’un nouveau-né manque d’oxygène autour de la naissance, les dégâts peuvent entraîner des troubles à vie comme la paralysie cérébrale, l’épilepsie ou des difficultés d’apprentissage. Les médecins tentent de limiter ces lésions par l’hypothermie thérapeutique, mais cette approche est moins efficace en présence d’une infection ou d’une inflammation. Cette étude pose une question surprenante : la gonadotrophine chorionique humaine (hCG) — la même hormone mesurée dans les tests de grossesse — peut-elle protéger le cerveau du nouveau-né lorsque la perte d’oxygène et l’inflammation surviennent simultanément ?
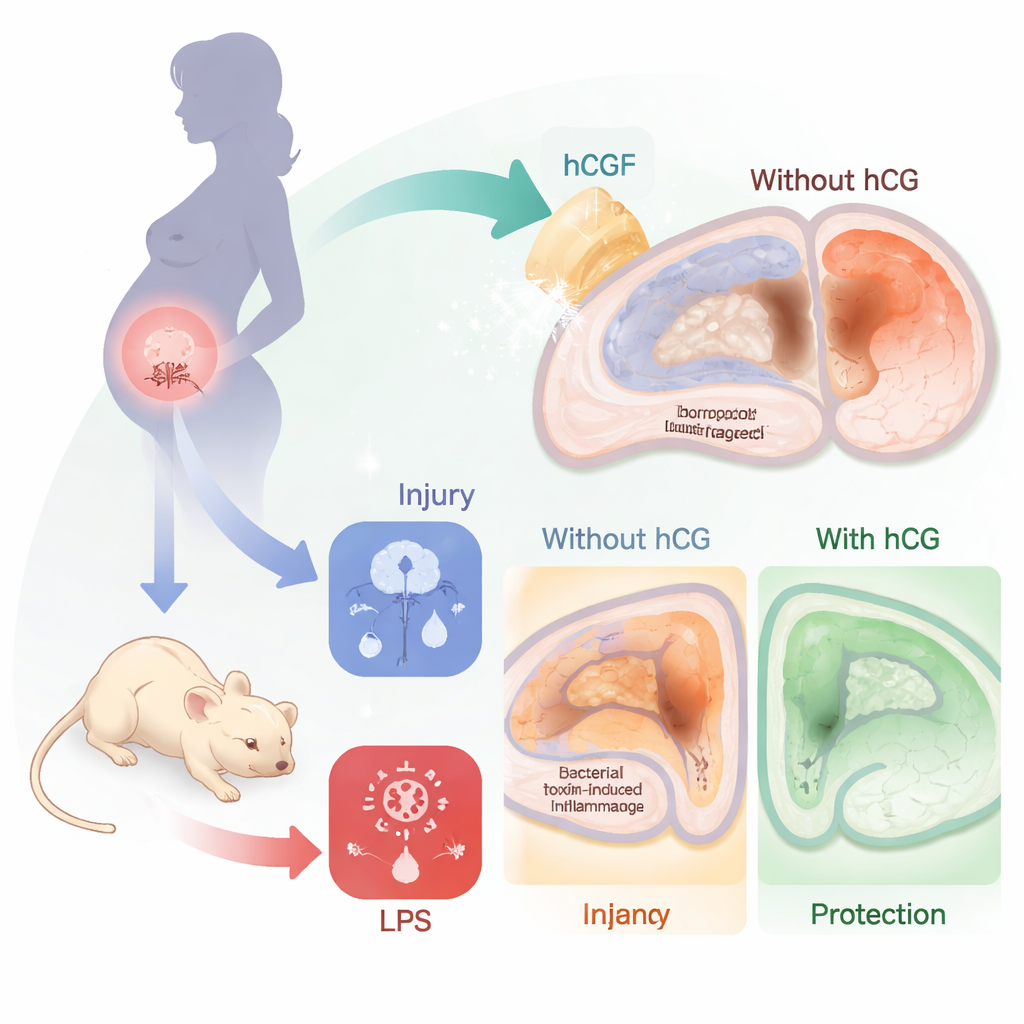
Manque d’oxygène, infection et double impact sur le cerveau
Dans la réalité clinique, les nouveau-nés très malades cumulent souvent plusieurs problèmes. Un manque d’oxygène et de flux sanguin vers le cerveau, appelé hypoxie-ischémie, peut déjà provoquer œdème, mort cellulaire et cicatrisation à long terme. L’infection ou une forte inflammation aggrave la situation en activant les cellules immunitaires dans et autour du cerveau. Des travaux antérieurs chez l’animal et l’humain ont montré que le principal traitement actuel, l’hypothermie, apporte des bénéfices limités lorsque des signaux inflammatoires puissants sont présents. Les auteurs ont donc cherché à modéliser ce « double impact » — perte d’oxygène plus inflammation — et à tester si la hCG pouvait atténuer les lésions cérébrales qui en résultent.
Recréer une lésion cérébrale néonatale chez la souris
Les chercheurs ont utilisé des souriceaux à un âge grossièrement comparable à celui des nouveau-nés humains à terme. Ils ont d’abord injecté aux souriceaux du lipopolysaccharide (LPS), une molécule de paroi bactérienne qui active fortement le système immunitaire. Dix-huit heures plus tard, ils ont brièvement interrompu l’apport sanguin sur un côté du cerveau et exposé les animaux à une faible oxygénation, reproduisant un épisode court mais délétère d’hypoxie-ischémie. Cette combinaison a produit des lésions cérébrales plus sévères que la seule hypoxie, incluant des cavités visibles remplies de liquide dans l’hippocampe et le cortex cérébral, des régions essentielles à la mémoire et aux fonctions supérieures. L’équipe a également observé une perte marquée d’un groupe particulier de cellules nerveuses inhibitrices marquées par la protéine parvalbumine, qui contribuent à maintenir l’équilibre de l’activité cérébrale et sont souvent perturbées dans les troubles du développement et du mouvement.
Tester la protection par une hormone naturelle de la grossesse
Pour vérifier si la hCG pouvait atténuer ces dommages, un autre groupe de souriceaux a reçu une dose unique de hCG deux heures avant le déclenchement de l’inflammation. À l’examen des cerveaux quelques jours plus tard, la différence était nette. Les souriceaux ayant reçu de la hCG présentaient moins de cavités de type kystique et de plus petites lésions dans l’hippocampe et le cortex, et la perte tissulaire globale dans ces régions était clairement réduite par rapport aux animaux traités uniquement par solution saline. Fait important, le traitement par hCG n’a pas entravé la croissance ni provoqué d’effets secondaires évidents, ce qui suggère que la dose protectrice était bien tolérée dans ce modèle.
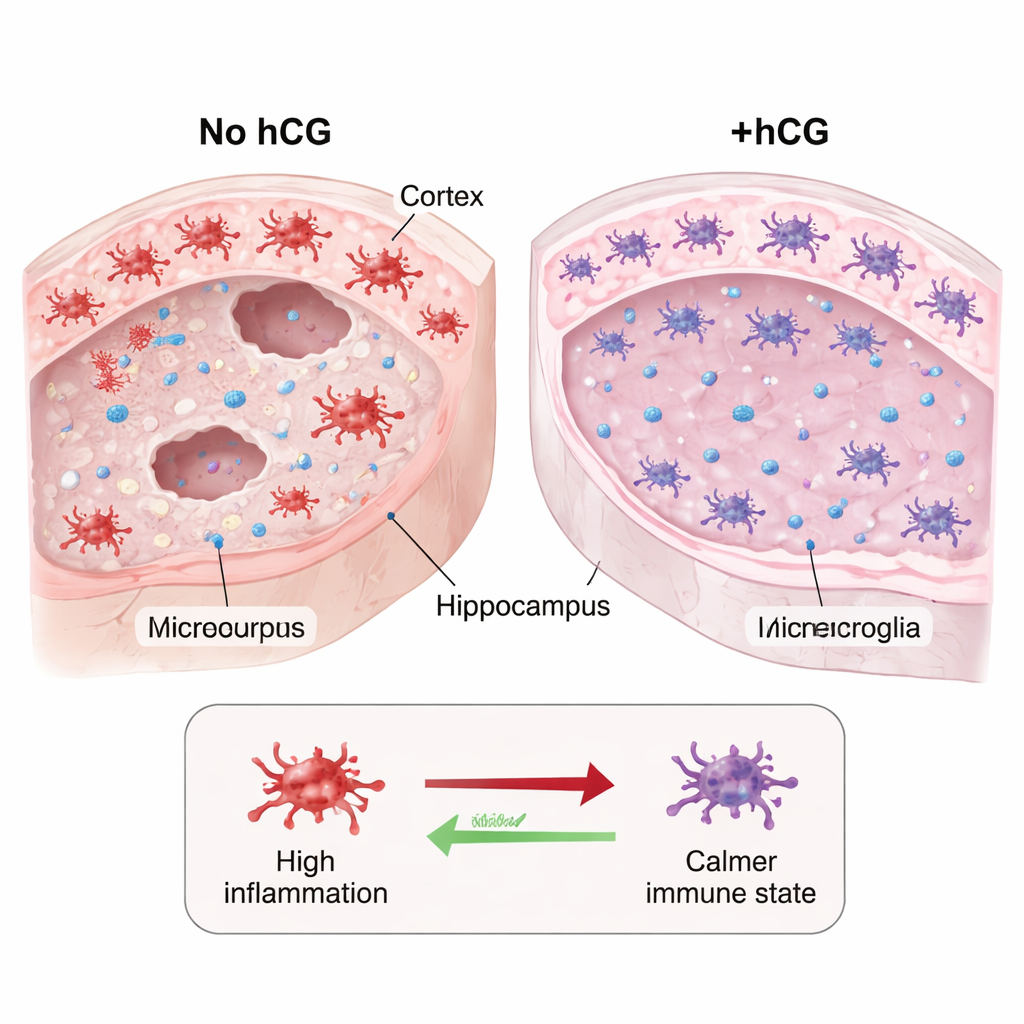
Sauver des cellules vulnérables et calmer l’activité immunitaire cérébrale
L’étude a ensuite examiné de plus près quelles cellules cérébrales étaient préservées. Chez les animaux non traités, de nombreux interneurones contenant de la parvalbumine ont été perdus dans le cortex, le striatum et l’hippocampe après la lésion combinée. Avec la hCG, bien plus de ces cellules restaient présentes, comme l’indiquait une conservation du marquage à la parvalbumine. Parallèlement, le nombre de microglies activées — les cellules immunitaires résidentes du cerveau, repérées par le marqueur Iba1 — était plus faible dans des régions clés chez les animaux traités à la hCG. Étant donné que la hCG est déjà connue pour orienter les réponses immunitaires vers un état moins inflammatoire et pour soutenir la survie neuronale dans d’autres contextes, ces résultats suggèrent qu’elle pourrait protéger le cerveau néonatal à la fois en calmant l’inflammation délétère et en nourrissant directement les neurones vulnérables.
Ce que cela pourrait signifier pour les soins futurs
Pour un lecteur non spécialiste, le message central est qu’une hormone naturellement produite pendant la grossesse peut, au moins chez la souris, réduire les lésions cérébrales causées par la combinaison dangereuse de perte d’oxygène et d’inflammation. Bien que ce travail soit encore à un stade préclinique et ait utilisé une administration préventive avant la lésion, il met en évidence la hCG — ou des médicaments agissant de façon similaire — comme candidats prometteurs pour renforcer les traitements actuels des nouveau-nés à haut risque. Si des études ultérieures confirment que la hCG est sûre et efficace lorsqu’elle est administrée après la lésion et en association avec l’hypothermie, elle pourrait un jour aider davantage de bébés à éviter les incapacités à long terme qui suivent souvent des complications sévères autour de la naissance.
Citation: Miller, B., Crider, A., Aravamuthan, B. et al. Human chorionic gonadotropin decreases cerebral cystic encephalomalacia and parvalbumin interneuron degeneration in a pro-inflammatory model of mouse neonatal hypoxia-ischemia. Sci Rep 16, 6851 (2026). https://doi.org/10.1038/s41598-026-35852-4
Mots-clés: lésion cérébrale néonatale, encéphalopathie hypoxique-ischémique, inflammation, gonadotrophine chorionique humaine, interneurones à parvalbumine